
【题目】氯吡格雷是一种用于抑制血小板聚集的药物,合成线路如图:
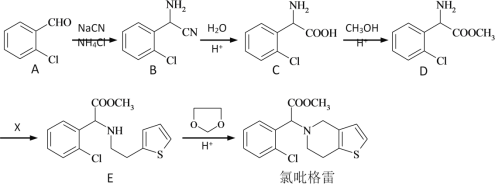
(1)C→D的反应类型____,X的化学式是(C6H7BrS),X的结构简式___。
(2)写出C聚合成高分子化合物的结构简式___。
(3)E合成氯吡格雷的反应中,另一个有机产物的结构简式___。
(4)物质A的同系物G,比A多一个碳原子且苯环上一溴代物只有两种的可能结构有___种。
(5)已知①同一个碳原子上连有两个羟基是不稳定的,极易脱水转变为![]() ,②
,②![]() 中氯原子在水溶液中不水解,写出2-氯甲苯(
中氯原子在水溶液中不水解,写出2-氯甲苯( )经两步反应合成A的化学方程式。____,合成A时产生的有机副产物可能是____。
)经两步反应合成A的化学方程式。____,合成A时产生的有机副产物可能是____。
【答案】酯化(或取代) ![]()
 HOCH2CH2OH 2
HOCH2CH2OH 2 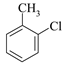 +2Cl2
+2Cl2![]()
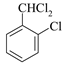 +2HCl、
+2HCl、 +2NaOH
+2NaOH![]()
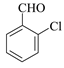 +2NaCl+H2O
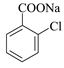
+2NaCl+H2O 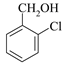 、
、
【解析】
(1)对比C、D的结构,D、E的结构得结论;
(2)C中含有氨基、羧基,二者发生缩聚反应生成高分子化合物;
(3)E合成氯吡格雷的反应为取代反应,可以知道生成另外有机物为乙二醇;
(4)物质A的同系物G,比A多一个碳原子且苯环上一溴代物只有两种,含有2个不同的取代基且处于对位;
(5)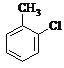 与氯气在光照条件下甲基上氢原子被取代,在水解即可;
与氯气在光照条件下甲基上氢原子被取代,在水解即可;
(1)对比C、D的结构可以知道,C中羧基与甲醇发生酯化反应,也属于取代反应;由D、E的结构可以知道,D→E发生取代反应,对比D、E的结构确定X的结构简式为:![]() ;
;
答案: 酯化(或取代);![]() ;
;
(2)C中含有氨基、羧基,二者发生缩聚反应生成高分子化合物,高分子化合物结构简式为:  ;
;
答案: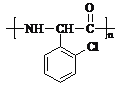 ;
;
(3)E合成氯吡格雷的反应为取代反应,可以知道生成另外有机物为HOCH2CH2OH;
答案:![]()
(4)物质A的同系物G,比A多一个碳原子且苯环上一溴代物只有两种,含有2个不同的取代基且处于对位,取代基为-Cl、-CH2CHO或-CH2Cl、-CHO符合条件的G共有2种;
答案:2;
(5) 与氯气在光照条件下得到
与氯气在光照条件下得到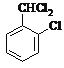 ,然后在氢氧化钠水溶、加热条件下水解得到
,然后在氢氧化钠水溶、加热条件下水解得到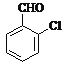 ,合成反应方程式为:
,合成反应方程式为:  +2Cl2
+2Cl2![]()
 +2HCl、
+2HCl、 +2NaOH
+2NaOH![]()
 +2NaCl+H2O,与氯气发生取代反应时可能得到
+2NaCl+H2O,与氯气发生取代反应时可能得到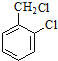 、
、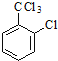 ,前者水解引入羟基,后者水解后脱水形成羧基,羧基与氢氧化钠反应,则产生的有机副产物可能是:
,前者水解引入羟基,后者水解后脱水形成羧基,羧基与氢氧化钠反应,则产生的有机副产物可能是:  、
、 ;
;
答案:  +2Cl2
+2Cl2![]()
 +2HCl、
+2HCl、 +2NaOH
+2NaOH![]()
 +2NaCl+H2O ;
+2NaCl+H2O ;  、
、 。
。


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
【题目】用除去表面氧化膜的细铝条紧紧缠绕在温度计上(如图),将少许硝酸汞溶液滴到铝条表面,置于空气中,很快铝条表面产生“白毛”,且温度明显上升。下列分析错误的是

A.Al和O2化合放出热量B.硝酸汞是催化剂
C.涉及了:2Al+3Hg2+→2Al3++3HgD.“白毛”是氧化铝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将水分解制得氢气的一种工业方法是“硫﹣碘循环法”,依次涉及下列三步反应:
I.SO2+2H2O+I2=H2SO4+2HI
II.2HI(g)H2(g)+I2(g)
III.2H2SO4=2SO2+O2+2H2O
(1)一定温度下,向5L恒容密闭容器中加入1molHI,发生反应II,H2物质的量随时间的变化如图所示。0~2min内的平均反应速率v(HI)=___。相同温度下,若起始加入的HI改为2mol,反应达平衡时H2的量为___mol。
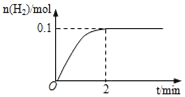
(2)分析上述反应,下列判断错误的是___(填写选项编号,只有一个正确选项)。
a.三步反应均为氧化还原反应
b.循环过程中产生1molH2,同时产生1molO2
c.在整个分解水的过程中SO2和I2相当于催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,某一密闭且体积不变的容器内有可逆反应:A(g)+2B(g) ![]() 2C(g)。该反应进行到一定限度后达到了化学平衡,不能作为判断该化学平衡标志的是
2C(g)。该反应进行到一定限度后达到了化学平衡,不能作为判断该化学平衡标志的是
A.容器内气体A的物质的量不再随时间而改变
B.容器内气体C的浓度不再随时间而改变
C.单位时间内生成amol物质A,同时生成2amol物质B
D.单位时间内生成amol物质A,同时生成2amol物质C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸(H2C2O4)是最简单的有机二元酸,具有较强的还原性,工业上主要用于生产药物以及提炼稀有金属。
工业上可由以下反应制取草酸(两步反应均为液相反应):
①4CO+4C4H9OH+O2![]() 2(COOC4H9)2+2H2O
2(COOC4H9)2+2H2O
②(COOC4H9)2+2H2O![]() H2C2O4+2C4H9OH-Q(Q>0)
H2C2O4+2C4H9OH-Q(Q>0)
(1)反应①选择13~15MPa的高压条件下进行,最主要的原因是为了___。若5min内水的质量增加了7.2g/L,则用水表示的反应速率为____。
(2)对于反应②,下列能够说明其已经达到平衡的是____。
a.平衡常数K保持不变 b.反应液的pH保持不变
c.丁醇的浓度保持不变 d.反应液的总质量保持不变
下列措施既能加快该反应速率,又有利于提高产率的是___。
a.合理升高反应温度 b.合理增大反应压强
c.增大水的用量 d.加入稀硫酸作为催化剂
(3)将物质的量浓度相同的草酸溶液与次氯酸钠溶液等体积混合,产生大量无色无味的气体,写出反应的化学方程式____。
(4)已知草酸氢钠溶液显酸性,下列措施能使草酸氢钠溶液中![]() 减小的是___。
减小的是___。
a.通入HCl气体 b.加入草酸晶体 c.通入NH3 d.加入草酸钾晶体
(5)已知:物质的量浓度相同的草酸溶液与亚硫酸钠溶液等体积混合,反应的化学方程式为:①H2C2O4+Na2SO3→NaHC2O4+NaHSO3;草酸溶液与过量的亚硫酸钠溶液混合,反应的化学方程式为:②H2C2O4+2Na2SO3→Na2C2O4+2NaHSO3;过量的草酸溶液与亚硫酸钠溶液混合,反应的化学方程式为:③2H2C2O4+Na2SO3→2NaHC2O4+H2O+SO2↑
根据以上信息判断草酸的两级电离常数(记为K1、K2)与亚硫酸的两级电离常数(记为K3、K4)由大到小的顺序____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校研究性学习小组用相同大小的铜片和锌片为电极研究水果电池,得到的数据如下表所示:

实验编号 | 水果种类 | 电极间距离/cm | 电流大小/μA |
① | 西红柿 | 1 | 98.7 |
② | 西红柿 | 2 | 72.5 |
③ | 苹果 | 2 | 27.2 |
(1)该实验的目的是探究水果种类和________对水果电池电流大小的影响。
(2)上图所示的装置中,做负极的材料是______(填“锌片”或“铜片”),该装置给将_________转变为电能。
(3)能表明水果种类对电流大小有影响的实验编号是____和_______。
(4)请你再提一个可能影响水果电池电流大小的因素:______________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO和H2在一定条件下可以合成乙醇:2CO(g)+4H2(g)![]() CH3CH2OH(g)+H2O(g),下列叙述中能说明上述反应在一定条件下已达到最大限度的是( )
CH3CH2OH(g)+H2O(g),下列叙述中能说明上述反应在一定条件下已达到最大限度的是( )
A.CO全部转化为乙醇B.正反应和逆反应的化学反应速率均为0
C.CO和H2以1∶2的物质的量之比反应生成乙醇D.反应体系中乙醇的物质的量浓度不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列有关实验装置进行的相应实验中,能达到实验目的的是
A.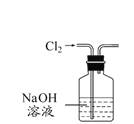 所示装置除去Cl2中含有的少量HCl
所示装置除去Cl2中含有的少量HCl
B.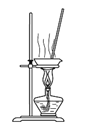 所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
C. 所示装置制取少量纯净的CO2气体
所示装置制取少量纯净的CO2气体
D.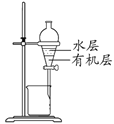 所示装置分离CCl4萃取碘水后已分层的有机层和水层
所示装置分离CCl4萃取碘水后已分层的有机层和水层
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨基甲酸铵(NH2COONH4)是重要的氨化剂,在潮湿的空气中能转化为碳酸铵,受热易分解、易被氧化。实验小组对氨基甲酸铵的性质进行了如下探究。请回答下列问题:
(1)氨基甲酸铵在潮湿的空气中转化为碳酸铵的化学方程式为____________________________。
(2)用下图装置探究氨基甲酸铵的分解产物(夹持装置略去,下同)。

①点燃A处的酒精灯之前,需先打开k,向装置中通入一段时间的N2,目的为_________________。
②仪器B的名称为_________________。
③装置D的作用为________________________________________________________。
④能证明分解产物中有NH3的现象为_________________________________________。
⑤试剂A用于检验分解产物中的CO2,该试剂的名称为_______________________。
(3)已知:CuO高温能分解为Cu2O和O2。若用上述装置和下列部分装置进一步检验分解产物中是否有CO,装置E后应依次连接_________________(按从左到右的连接顺序填选项字母)。
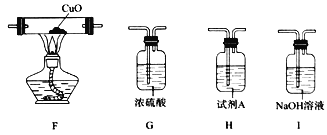
(4)通过实验得出结论:氨基甲酸铵受热分解为NH3和CO2。该反应的化学方程式为_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com