
【题目】为了测定某有机物A的结构,做如下实验:
①将2.3 g该有机物完全燃烧,生成0.1 mol CO2和2.7 g水;
②用质谱仪测定其相对分子质量,得如图1所示的质谱图;
③用核磁共振仪处理该化合物,得到如图2所示图谱,图中三个峰的面积之比是1∶2∶3。
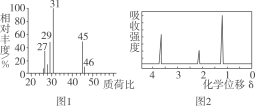
试回答下列问题:
(1)有机物A的相对分子质量是________。
(2)有机物A的实验式是________。
(3)能否根据A的实验式确定其分子式________(填“能”或“不能”),若能,则A的分子式是________(若不能,则此空不填)。
(4)写出有机物A的结构简式:________。
【答案】(共8分) (1)46 (2分) (2)C2H6O (2分)
(3)能(1分) C2H6O(1分) (4)CH3CH2OH(2分)
【解析】
试题(1)在A的质谱图中,最大质荷比为46,所以其相对分子质量是46。
(2)在2.3 g该有机物中,n(C)=0.1 mol
m(C)=0.1 mol×12 g·mol-1=1.2 g
n(H)=![]() ×2=0.3 mol
×2=0.3 mol
m(H)=0.3 mol×1 g·mol-1=0.3 g
m(O)=2.3 g-1.2 g-0.3 g=0.8 g
n(O)=![]() =0.05 mol
=0.05 mol
则n(C):n(H) :n(O)=0.1 mol:0.3 mol:0.05 mol=2:6:1,A的实验式是C2H6O。
(3)因为实验式是C2H6O的有机物中,氢原子数已经达到饱和,所以其实验式即为分子式。
(4)A有如下两种可能的结构:CH3OCH3或CH3CH2OH;在核磁共振氢谱中有三个峰,而且三个峰的面积之比是1:2:3,根据图三知,A中含有C—H、C—O、O—H,显然A为乙醇。


科目:高中化学 来源: 题型:
【题目】石油是工业的血液,与我们的生产、生活息息相关。
完成下列填空:
(1)可用来衡量一个国家石油化工发展水平的是__________的产量。
A.乙烷 B.乙烯 C.甲烷
(2)乙烯能使溴水褪色,说明乙烯能发生__________反应。
A.取代 B.加成 C.氧化还原
(3)甲烷和氯气在光照条件下能发生反应,反应的其中一个方程式如下:
CH4 + Cl2 → CH3Cl + HCl ,该反应属于__________反应。
A.取代 B.加成 C.氧化还原
(4)下列与异戊烷如图,互为同分异构体的是(_______)
![]()
A.  B.
B.![]() C.
C.
(5)聚乙烯安全无毒,可用于生产食品包装袋。聚乙烯的结构简式为(_______)
A.CH2=CH2 B.![]() C.
C. ![]()
(6)同系物结构相似,在分子组成上相差一个或若干个CH2原子团,请写出任意一个甲烷的同系物的结构简式。_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的转化关系如下图所示(有的反应可能在水溶液中进行)。其中A是一种能使红色石蕊试液变蓝的气体,甲为淡黄色固体化合物,乙为金属单质,G为酸,乙在G的浓溶液中发生钝化,用两根玻璃棒分别蘸取化合物A、G的浓溶液并使它们接近,有大量白烟生成。请回答下列问题:
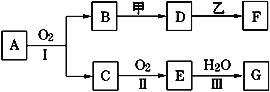
(1)写出甲的电子式是___________;
(2)写出反应Ⅰ的化学方程式__________;
(3)A溶于水得到溶液X,在25℃下,将a mol·L-1的X与b mol·L-1的G溶液等体积混合,溶液显中性,则所得溶液中离子浓度由大到小的顺序为______________;用含a和b的代数式表示出该混合溶液中X的电离平衡常数_______________________。
(4)工业上采用的一种污水处理方法是:保持污水的pH在5.0~6.0之间,通过如图装置处理污水。
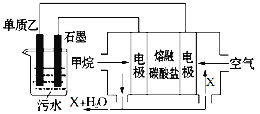
① 电解池阳极发生了两个电极反应,其中一个反应生成一种无色气体,则阳极的电极反应式分别是:Ⅰ.___; Ⅱ.______。
② 为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分X物质参加循环,X物质的化学式是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属及金属材料在生产、生活中有广泛的应用。
(1)我省多地开展文明城市创建工作,垃圾分类回收是一项重要举措。某市街道垃圾桶如图所示,请回答下列问题:

①图中标识的物质,属于金属材料的是__________(写出一种即可)。
②使用铝合金做内筒的优点是____ (写出一点即可)。某品牌饮料的空易拉罐应收入_____(填“可回收”或“不可回收”)筒中。
③铁制品锈蚀的过程,实际上是铁跟空气中的________发生化学反应的过程:除去铁制品表面的铁锈可用稀盐酸,反应的化学方程式为________________________________
(2)将甲、乙、丙三种金属分别投入稀硫酸中,甲、丙表面有气泡产生,乙无明显现象:若将甲放入丙的硫酸盐溶液中,一段时间后,甲的表面有丙析出。由此推断这三种金属的活动性由强到弱的顺序是________________。
(3)将一定质量的铁粉加到Al(NO3)3、Cu(NO3)2、AgNO3三种物质的混合溶液中,充分反应后过滤,得到滤液和滤渣。下列说法正确的是________ (垃字母)。
A.若滤液为蓝色,则滤渣中一定有银,可能有铜
B.若滤液中含有银、铜、铁,则滤液中一定含有Al3+、Fe3+、NO3-
C.若滤液为浅绿色,则滤渣中一定含银、铜、铝
D.若滤渣中加稀盐酸无气泡产生,则滤液中一定有Al3+、Fe2+、Cu2+,可能有Ag+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)3.01×1023个氯气分子的物质的量是________________ ;
(2)4g金属钙的物质的量是________________;
(3)1molH2O的质量为________________;
(4)24g O2分子所含氧原子数目(用NA表示)________________;
(5)在标准状况下,33.6L NH3的物质的量为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质,不能按如图(“→”表示反应一步完成)关系转化的是

选 项 | a | b | c |
A | Al2O3 | NaAlO2 | Al(OH)3 |
B | Al | Al(OH)3 | Al2O3 |
C | AlCl3 | Al(OH)3 | NaAlO2 |
D | MgCl2 | Mg(OH)2 | MgO |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无色的混合气体甲,可能含NO、CO2、NO2、NH3、N2中的几种,将100mL甲气体经过如图所示实验的处理,结果得到酸性溶液,而几乎无气体剩余,则甲气体的组成为( )
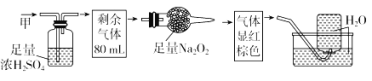
A. NH3、NO2、N2B. NH3、NO、CO2
C. NH3、NO2、CO2D. NO、CO2、N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42—可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。

下列叙述正确的是( )
A. 通电后中间隔室的SO42-离子向正极迁移,正极区溶液pH增大
B. 该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
C. 负极反应为2H2O 4e– = O2+4H+,负极区溶液pH降低
D. 当电路中通过1mol电子的电量时,会有0.5mol的O2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,在A处通入氯气,关闭B阀时,C处的红布条看不到明显现象;当打开B阀后,C 处的红布条逐渐褪色。有以下几种溶液,则D瓶中盛放的溶液可能是
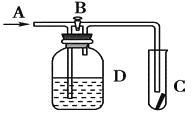
①浓硫酸 ②NaOH溶液 ③H2O ④饱和氯化钠溶液
A.①③B.①②C.②③D.②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com