
【题目】“清肺排毒汤”来源于中医经典方剂组合,对新冠肺炎病毒感染的轻型、普通型的治疗具有良好的效果。其中的一味中药黄芩的有效成分的结构简式如图所示,下列说法错误的是( )
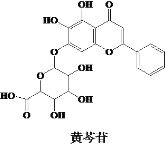
A.黄芩苷是芳香化合物,其分子式为C21H18O11
B.黄芩苷可发生取代、加成、氧化反应
C.黄芩苷分子中苯环上的一氯代物有3种
D.1 mol黄芩苷与足量钠反应,所得H2的体积在标准状况下为67.2 L
科目:高中化学 来源: 题型:
【题目】钛合金材料已经广泛应用于国防、航天、医疗等领域。已知常温下钛(Ti)与酸、碱均不反应,高温下能被空气氧化。由钛铁矿(主要成分为FeO·TiO2)提取金属钛的主要流程如图所示。有关叙述错误的是( )
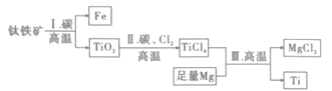
A.步骤Ⅰ、Ⅱ中的碳均作还原剂B.可用稀硫酸或稀盐酸除去金属钛中的少量镁
C.钛元素位于元素周期表中第ⅡB族 D.步骤Ⅲ需在氩气氛围中进行,防止金属被空气氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有以下物质①石墨;②钠;③酒精;④氨气;⑤硫化氢;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧纯醋酸;⑨氧化钠固体;⑩液态氯化氢。
(1)其中能导电的是_______;属于非电解质的是_________。
(2)等质量④和⑤中氢原子的数目之比为_____;若④和⑤中所含氢原子数相等,则④和⑤的质量之比为________。
(3)写出⑥和⑧在水溶液中的离子反应方程式____________________________。
(4)室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两,分别向A、B两室充入H2、O2的混合气体和1mol空气,此时活塞的位置如图所示。
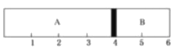
①A室混合气体所含分子总数约为______________(填数值)
②实验测得A室混合气体的质量为34g,则该混合气体的密度是同温同压下氢气密度的______倍。
③若将A室H2、O2的混合气体点燃,恢复原温度后,最终活塞停留的位置在______刻度处。
(5)在标准状况下,1L2mol/L氢氧化钠溶液中通入33.6L二氧化碳气体充分反应,所得溶液溶质的成分是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有600 mL某种混合物溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现将此溶液分成三等份,进行如下实验:
(1)向第一份中加入AgNO3溶液,有沉淀产生;
(2)向第二份中加足量NaOH溶液并加热后,收集到气体0.04 mol;
(3)向第三份中加足量BaCl2溶液后,得干燥的沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。 根据上述实验现象,以下推测正确的是
A. K+不一定存在 B. Ba2+、Mg2+不一定都存在
C. Cl-不一定存在 D. 混合溶液中CO32-的浓度为0.2 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是原子序数依次增大的5种短周期元素。A与D、C与E分别同主族,E原子的最外层电子数比次外层少2个。A、B两元素可形成BA3气体分子甲,甲能使湿润的红色石蕊试纸变蓝且每个分子内含10个电子。请回答下列问题:
(1)气体甲溶于水所得溶液呈碱性的原因(用电离方程式表示)______________。
已知:甲、乙、丙、丁4种物质之间的转化关系如下图(注:反应条件或产物已略去)。
甲![]() 乙
乙![]() 丙
丙![]() 丁
丁
请写出从甲→乙转化的化学方程式____________________________________________。
(2)用电子式表示离子化合物D2C2的形成过程____________________________________。
(3)DAEC3和DAEC4的溶液均呈现_______(填:“酸”“碱”“中”)性,在DAEB3溶液中离子浓度由大到小的顺序是________________________________;如果将两种溶液混合后发生反应的离子方程式为____________________________________。
(4)已知A2EC3和A2EC4两种酸中酸性更强的是后者,请从分子结构和性质的关系角度解释这种差异产生的原因___________________________________。
(5)B元素的三氯化物(BCl3)常温下是一种淡黄色液体,具有三角锥型的分子结构。下列关于BCl3分子的描述中不正确的是_________________。
A.BCl3分子中B显-3价、采用SP3杂化
B.BCl3分子间可形成氢键,比PCl3难挥发
C.B、C元素的电负性B< C ,第一电离能B>C
D.BCl3遇水发生水解反应产物是BH3和HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列选项中互为同系物的是__________;互为同分异构体的是__________;属于同种物质的是__________。
①H2O与D2O;②1H、2H、3H;③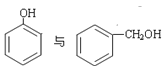 ;④
;④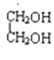 与
与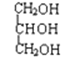 ;⑤
;⑤ ![]() ;⑥戊烯与环戊烷; ⑦
;⑥戊烯与环戊烷; ⑦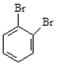 与
与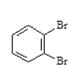
(2)羟基、羧基的性质具有明显的差异,为实现如图所示的各步转化,请在括号内填入适当试剂的化学式。
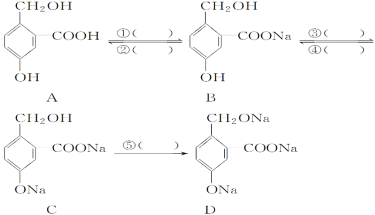
①__________;②__________;③__________;④__________;⑤__________;
(3)聚碳酸酯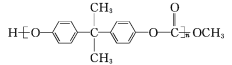 的透光率良好,可制作车、船、飞机的挡风玻璃等。①原来合成聚碳酸酯的一种原料是有毒的光气(COCl2),现在改用绿色化学原料碳酸二甲酯(
的透光率良好,可制作车、船、飞机的挡风玻璃等。①原来合成聚碳酸酯的一种原料是有毒的光气(COCl2),现在改用绿色化学原料碳酸二甲酯(![]() )与____(填序号)缩合聚合而成。
)与____(填序号)缩合聚合而成。
A.二卤代物 B.二酚类 C.二醛类 D.二烯类
②写出用绿色化学原料合成聚碳酸酯反应的化学方程式____________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.近期,四川等地频频发生地震,在地震过后,常常喷洒各类消毒液对灾民临时生活区进行消毒。某品牌的“84消毒液”的主要成分为NaClO,浓度为![]() ,密度为
,密度为![]() 。
。
请回答下列问题:
(1)该“84消毒液”的质量分数为___(保留3位有效数字)。
(2)某同学欲用NaClO固体配制240mL“84消毒液”。
①下列仪器中,不需要用到的是___。
A.烧杯 B.250 mL容量瓶 C.10mL量筒 D.胶头滴管 E.天平
②下列操作会导致所得溶液浓度偏高的是_____。
A.用长时间放置在空气中的NaClO固体配制 B.配制前,容量瓶中有少量蒸馏水
C.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒 D.定容时俯视容量瓶刻度线
Ⅱ.近年来,雾霾天气频繁发生,降低氮氧化物的排放,至关重要。
(3)三元催化剂能同时实现汽车尾气中的CO、![]() 、
、![]() 三种成分的净化,其催化剂表面物质转化的关系如图1所示。化合物X可借助傅里叶红外光谱图(如图2所示)确定。
三种成分的净化,其催化剂表面物质转化的关系如图1所示。化合物X可借助傅里叶红外光谱图(如图2所示)确定。
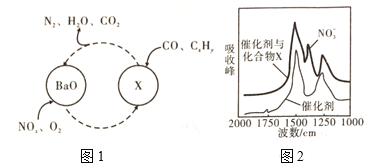
①X的化学式为____。
②在图1的转化中,既有被氧化又有被还原的元素是___(填元素符号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应NH4Cl+NaNO2═NaCl+N2↑+2H2O放热且产生气体,可用于冬天石油的开采。下列表示反应中相关微粒的化学用语正确的是( )
A.中子数为18的氯原子:![]() Cl
Cl
B.H2O的电子式:![]()
C.Na+的结构示意图:![]()
D.N2的结构式:N═N
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。已知:2KMnO4+16HCl―→2KCl+5Cl2↑+2MnCl2+8H2O

对实验现象的“解释或结论”正确的是 ( )
选项 | 实验现象 | 解释或结论 |
A | a处变蓝,b处变红棕色 | 氧化性:Cl2>Br2>I2 |
B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
C | d处立即褪色 | 氯气与水生成了漂白性物质 |
D | e处变红色 | 还原性:Fe2+>Cl- |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com