
| A、新制氯水中只有Cl2和H2O分子 |
| B、氯气跟水反应生成两种强酸 |
| C、光照氯水时有气体逸出,该气体是Cl2 |
| D、新制氯水放置数天后酸性会变强 |
| ||
| ||


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
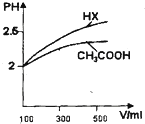 已知25℃时部分弱电解质的电离平衡常数数据如下表
已知25℃时部分弱电解质的电离平衡常数数据如下表| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | Ka1=4.3×10-7、Ka2=5.6×10-11 |
| H2SO3 | Ka1=1.0×10-2、Ka2=1.02×10-7 |
| c(H2SO3) |
| c(HSO3-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | D | E | F | G |
| 所有原子中半径最小 | 基态原子核外只有三个能级,且各能级电子数相等 | 由D形成的两种单质,其中之一是地球生物的“保护伞” | 短周期中第一电离能量小 | 单质为淡黄色晶体,不溶于水,微溶于酒精 | 最外层只有一个电子,次外层填满电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
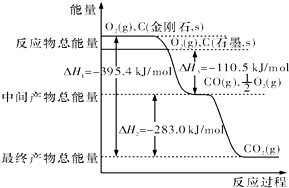
| A、Q1=Q2=57.3 |
| B、Q1>Q2>57.3 |
| C、Q1<Q2=57.3 |
| D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入的NaOH 不够 |
| B、加入的CuSO4 不够 |
| C、未用水浴加热 |
| D、加入的乙醛太少 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、H+、SO42-、HCO3- |
| B、MnO4-、Na+、S2-、K+ |
| C、Na+、K+、Cl-、NO3- |
| D、Fe3+、K+、SO42-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、可将地下输油管与外加直流电源的正极相连以保护它不受腐蚀 |
| B、当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用 |
| C、在海轮外壳连接一锌块保护外壳不受腐蚀是采用了牺牲阴极的阳极保护法 |
| D、纯银器表面在空气中因化学腐蚀渐渐变暗 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com