
已知汽车尾气无害化处理反应为2NO(g)+2CO(g)  N2(g)+2CO2(g)。下列说法不正确的是( )
N2(g)+2CO2(g)。下列说法不正确的是( )
A、升高温度可使该反应的逆反应速率降低
B、使用高效催化剂可有效提高正反应速率
C、反应达到平衡后,NO的反应速率保持恒定
D、单位时间内消耗CO和CO2的物质的量相等时,反应达到平衡
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源: 题型:
实验室用浓度为0.500mol/L的标准氢氧化钠溶液来测定未知浓度的盐酸,完善下列实验过程:
(1)滴定管使用前,先要检查滴定管的活塞 ,活塞旋转是否灵活。
(2)把标准氢氧化钠溶液注入用标准氢氧化钠溶液润洗过的蓝色手柄滴定管中,使液面位于 位置,记录读数。
(3)在锥形瓶中放入20.00mL的待测溶液,再滴加2滴酚酞,摇匀。用标准氢氧化钠溶液滴定,边滴边摇动锥形瓶,眼睛注视 的变化。直到滴入最后一滴氢氧化钠溶液,指示剂的颜色由 色变为 色,并在半分钟内溶液颜色不发生变化,停止滴定,记录读数。
(4)重复(2)和(3)操作,并记录数据。再次滴定消耗氢氧化钠溶液的数据如下表:
| 次数 | 滴定前(mL) | 滴定后(mL) |
| 1 | 0.40 | 21.10 |
| 2 | 0.10 |
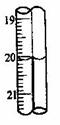 第2次滴定后滴定管的读数如右图所示,将这一读数填入上表中。根据表中的数据计算出盐酸的浓度为 mol/L。
第2次滴定后滴定管的读数如右图所示,将这一读数填入上表中。根据表中的数据计算出盐酸的浓度为 mol/L。
已知盐酸的准确浓度为0.490mol/L,则实验误差为 %。
(5)会造成实验结果偏高的操作是 (填写编号)。
a. 锥形瓶用蒸馏水洗净后,立即装入待测溶液
b. 振荡时溶液溅出锥形瓶外
c. 滴定时蓝色手柄滴定管中的液体滴在锥形瓶外
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生设计了如下方法对X盐进行鉴定:

由此分析,下列结论中正确的是
A.X中一定有Fe3+ B.Z中一定有Fe3+
C.Y为AgI沉淀 D.X一定为FeBr2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
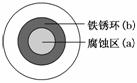 将 NaCl 溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆圈中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示。导致该现象的主要原因是液滴之下氧气含量比边缘处少。下列说法正确的是( )
将 NaCl 溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆圈中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示。导致该现象的主要原因是液滴之下氧气含量比边缘处少。下列说法正确的是( )
A.液滴中的 Cl-由 a 区向 b 区迁移
B.液滴边缘是正极区,发生的电极反应为:O2+2H2O+4e-===4OH-
C.液滴下的 Fe 因发生还原反应而被腐蚀,生成的 Fe2+由 a 区向 b 区迁移,与 b 区的OH-形成 Fe(OH)2,进一步氧化、脱水形成铁锈
D.若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加 NaCl 溶液,则负极发生的电极反应为:Cu-2e-===Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
如下图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。
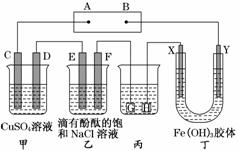
请回答:
(1)B极是电源的______________,一段时间后,甲中溶液颜色________,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明___________________,在电场作用下向Y极移动。
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为________。
(3)现用丙装置给铜件镀银,则H应是________________(填“镀层金属”或“镀件”),电镀液是________溶液。当乙中溶液的pH是13时(此时乙溶液体积为500 mL),丙中镀件上析出银的质量为________,甲中溶液的pH________(填“变大”、“变小”或“不变”)。
(4)若将C电极换为铁,其他装置都不变,则甲中发生的总反应的离子方程式为:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
为了说明影响化学反应快慢的因素,甲、乙、丙、丁四位同学分别设计了如下A-D四个实验,你认为结论不正确的是( )
A、将铜片放入稀硫酸中,无现象。若再向所得溶液中加入硝酸银溶液,一段时间后,由于形成原电池,可看到有氢气生成。
B、将相同大小、相同质量的镁条和铝条与相同浓度盐酸反应,前者速率大于后者
C、两支试管中分别加入相同质量的氯酸钾,其中一支试管中再加入少量二氧化锰,同时加热,产生氧气的快慢不同
D、相同条件下等质量的块状和粉状大理石与相同浓度盐酸反应时,粉状的反应速率快
查看答案和解析>>
科目:高中化学 来源: 题型:
将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)  2C(g)。若经2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
2C(g)。若经2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
①用物质A表示的反应的平均速率为0.3 mol·L-1·s-1
②用物质B表示的反应的平均速率为0.6 mol·L-1·s-1
③2 s时物质A的转化率为70%
④2 s时物质B的浓度为0.7 mol·L-1
其中正确的是( )
A、①③
B、①④
C、②③
D、③④
查看答案和解析>>
科目:高中化学 来源: 题型:
要将NaCl溶液中含有的少量FeCl3、AlCl3杂质除去,合理的方案是
A.加入过量氨水后过滤
B.加入过量NaOH溶液后过滤
C.先加过量NaOH溶液后过滤,取滤液再通入足量CO2再过滤
D.先加过量NaOH溶液后过滤,取滤液通入足量CO2再过滤,往滤液中加入适量盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
已知化学反应2C(s)+O2(g) 2CO(g),2CO(g)+O2(g)
2CO(g),2CO(g)+O2(g) 2CO2(g)都是放热反应,据此判断,下列说法中不正确的是(其他条件相同)( )
2CO2(g)都是放热反应,据此判断,下列说法中不正确的是(其他条件相同)( )
A.12 g碳所具有的能量一定高于28 g CO所具有的能量
B.56 g CO和32 g O2所具有的总能量大于88 g CO2所具有的总能量
C.12 g C和32 g O2所具有的总能量大于44 g CO2所具有的总能量
D.将一定质量的C燃烧,生成CO2比生成CO时放出的热量多
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com