
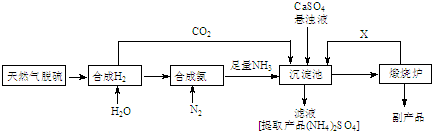

分析 (1)H2S杂质常用氨水吸收,产物为NH4HS,一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,反应过程中生成一水合氨,依据原子守恒和电子守恒配平书写化学方程式;
(2)①根据Fe为26号元素结合核外电子排布规律书写电子排布式;
②平衡状态是指外界一定各组份的浓度、物质的量、质量分数、速率不再随时间的改变而改变的动态平衡状态,据此分析;
(3)将NH3和CO2通入沉淀池中并加入CaSO4,生成(NH4)2SO4和CaCO3;
(4)由工艺流程可知,CaCO3在煅烧炉中分解生成CO2和CaO,CO2循环使用,从溶液中获取晶体应采取蒸发浓缩、冷却结晶、过滤等操作.
解答 解:(1)H2S杂质常用氨水吸收,产物为NH4HS,一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,反应过程中生成一水合氨,依据原子守恒和电子守恒配平书写化学方程式为:2NH4HS+O2$\frac{\underline{\;一定条件\;}}{\;}$2NH3•H2O+2S↓,
故答案为:2NH4HS+O2$\frac{\underline{\;一定条件\;}}{\;}$2NH3•H2O+2S↓;
(2)①因为Fe为26号元素,所以Fe3+的核外电子排布式为[Ar]3d5 ,
故答案为:[Ar]3d5 ;
②平衡状态是指外界一定各组份的浓度、物质的量、质量分数、速率不再随时间的改变而改变的动态平衡状态,
a、t1时刻正反应速率最大,不是不变,故a不选;
b、温度不变,平衡常数不变,故b不选;
c、t1时刻,各物质的量不再随时间的变化而变化,故选c;
d、t1时刻,氢气的体积分数不再随时间的改而改变,故选d;
故答案为:c、d;
(3)将NH3和CO2通入沉淀池中并加入CaSO4,生成(NH4)2SO4和CaCO3,发生CaSO4+CO2+2NH3+H2O=CaCO3↓+(NH4)2SO4,
故答案为:CaSO4+CO2+2NH3+H2O=CaCO3↓+(NH4)2SO4;
(4)由工艺流程可知,CaCO3在煅烧炉中分解生成CO2和CaO,CO2循环使用,从溶液中获取晶体应采取蒸发浓缩、冷却结晶、过滤等操作,所以必须操作步骤是BCD.
故答案为:CO2;冷却结晶.
点评 本题考查学生对物质的制备实验方案与工艺流程理解、物质分离提纯与检验以及平衡状态的判断等,题目难度中等,(3)中方程式书写是易错点,可以理解为氨气、二氧化碳、水反应生成碳酸铵,碳酸铵与硫酸钙反应生成碳酸钙、硫酸铵.


 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KNO3 K2SO4 K2CO3 K3PO4 | B. | NaOH KOH Ba(OH)2 Ca(OH)2 | ||
| C. | Na2O K2O CaO CO2 | D. | HNO3 H2SO4 H3PO4 HClO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 仪器标号 | 1 | 2 | 3 | 4 | 5 |
| 试剂标号 | E | AFG | C | G | I |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 半导体生产中常需要控制掺杂,以保证控制电阻率,三氯化磷(PCl3)中一种重要的掺杂剂.实验室要用黄磷(白磷)与干燥的Cl2模拟工业生产制取PCl3,装置如下图所示:(部分夹持装置略去)
半导体生产中常需要控制掺杂,以保证控制电阻率,三氯化磷(PCl3)中一种重要的掺杂剂.实验室要用黄磷(白磷)与干燥的Cl2模拟工业生产制取PCl3,装置如下图所示:(部分夹持装置略去)| 物质 | 熔点/℃ | 沸点/℃ |
| PCl3 | -112 | 75.5 |
| PCl5 | 2 | 105.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO2-酸性氧化物 Na2O2-碱性氧化物 Al2O3-两性氧化物 | |
| B. | 漂白粉-混合物 胆矾-纯净物 HD-单质 | |
| C. | 纯碱-碱 硫化氢-酸 小苏打-酸式盐 | |
| D. | 盐酸-强电解质 硫酸钡-强电解质 醋酸-弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com