
| A. | KNO3 K2SO4 K2CO3 K3PO4 | B. | NaOH KOH Ba(OH)2 Ca(OH)2 | ||
| C. | Na2O K2O CaO CO2 | D. | HNO3 H2SO4 H3PO4 HClO3 |
分析 A、都是钾盐的正盐;
B、都是强碱,两种一元碱,两种二元碱;
C、二氧化碳是非金属氧化物,其余为金属氧化物;
D、都是最高价含氧酸;
解答 解:A、都是钾盐的正盐,无一种物质与另外三种物质的类别不同,故A错误;
B、都是强碱,两种一元碱,两种二元碱,无一种物质与另外三种物质的类别不同,故B错误;
C、二氧化碳是非金属氧化物,其余为金属氧化物,二氧化碳这一种物质与另外三种物质的类别不同,故C正确;
D、都是最高价含氧酸,无一种物质与另外三种物质的类别不同,故D错误;
故选C.
点评 本题考查物质的分类,较简单,学生应学会利用物质的组成和性质来分析其类别,并熟悉元素的化合价,能利用化合价分析氧化还原反应,较简单.


科目:高中化学 来源: 题型:多选题

| A. | 该物质分子式为C13H14O4 | |
| B. | 能与FeCl3溶液发生显色反应 | |
| C. | 在一定条件下可发生加成、取代、消去反应 | |
| D. | 1 mol该物质最多能与2mol NaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.24L | B. | 4.48L | C. | 5.6L | D. | 11.2L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用水鉴别乙醇、苯和CCl4 | |
| B. | 用燃烧法鉴别甲烷、乙炔和四氧化碳 | |
| C. | 用碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯 | |
| D. | 用酸性高锰酸钾溶液鉴别乙炔、乙烯和丙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
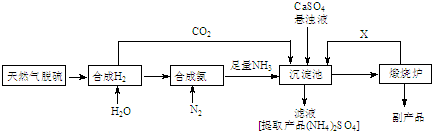

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验序号 | 待测液体积(mL) | 所消耗盐酸标准液的体积(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.50 | 20.70 |
| 2 | 20.00 | 6.00 | 26.00 |
| 3 | 20.00 | 1.40 | 21.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 对于可逆反应2A(?)+B(g)?2C(g);如图是其它条件一定时反应中C的百分含量与压强的关系曲线.回答下列问题:
对于可逆反应2A(?)+B(g)?2C(g);如图是其它条件一定时反应中C的百分含量与压强的关系曲线.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com