
下列各化学反应的离子方程式中,有错误的是( )
A.铝与氢氧化钠反应:2Al+2OH-+2H2O=2AlO2-+3 H2↑
B.氧化铝溶于氢氧化钠溶液:Al2O3+2OH-=2AlO2-+H2O
C.碘化亚铁溶液中滴入足量溴水:2Fe2++2I-+2Br2=I2+2Fe3++4Br-
D.碳酸氢镁溶液中加过量澄清石灰水
Mg2++2HCO3-+2Ca2++4OH-=2CaCO3↓+2H2O+Mg(OH)2↓
科目:高中化学 来源: 题型:
下列命名或说法正确的是( )
A.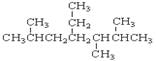 的名称是2,5,6-三甲基-4-乙基庚烷
的名称是2,5,6-三甲基-4-乙基庚烷
 B.常压下,正戊烷、异戊烷、新戊烷的沸点依次增大
B.常压下,正戊烷、异戊烷、新戊烷的沸点依次增大
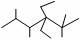
C. 的名称是2,3,5,5-四甲基-4,4-二乙基己烷
D.2,3-二甲基-1-丁烯
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学用语的表示错误的是
A、Na+的电子排布图:
B、氯离子的结构示意图: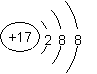
| C、甲基的电子式: |
| D、硫离子的核外电子排布式:1s22s22p63s23p6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解。
(1)卤族元素位于周期表的_________区;溴的电子排布式为______________。
(2)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在。使氢氟酸分子缔合的作用力是 。
(3)根据下表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是 。
| 氟 | 氯 | 溴 | 碘 | 铍 | |
| 第一电离能 (kJ/mol) | 1681 | 1251 | 1140 | 1008 | 900 |

(4)已知高碘酸有两种形式,化学式分别为H5IO6和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6_____HIO4(填“>”、“<”或“=”)
(5)已知ClO2-立体构型为V型。ClO2-中心氯原子的杂化轨道类型为___________,写出CN-的等电子体的化学式__________(写出1个)
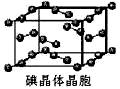 (6)下图为碘晶体晶胞结构。有关说法中正确的是_____________。
(6)下图为碘晶体晶胞结构。有关说法中正确的是_____________。
A、用均摊法可知平均每个晶胞中有4个碘原子
B、碘晶体为无限延伸的空间结构,是原子晶体
C、碘晶体中存在非极性键和范德华力
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.铁是位于第四周期第ⅧB族元素, 是一种重要的过渡元素
B.四氧化三铁是氧化铁和氧化亚铁组成的混合物
C.14克铁粉和7克硫粉混合后高温下充分反应能生成21克硫化亚铁
D.铁在溴蒸气中点燃可生成FeBr3
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸铵在强热条件下分解:4(NH4)2SO4 = 6 NH3↑+ N2↑+3SO2↑+SO3↑+7H2O若将生成的气体通入氯化钡溶液中,得到的沉淀物是( )
A.BaSO3和BaSO4 B.BaS C.BaSO3 D.BaSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
在三个密闭容器中分别充入HCl、H2S、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(P)从大到小的顺序是( )
A.P(HCl) >P(H2S)>P(O2) B.P(O2)> P(H2S) > P(HCl)
C.P(H2S)>P(HCl)>P(O2) D.P(H2S)>P(O2)>P(HCl)
查看答案和解析>>
科目:高中化学 来源: 题型:
KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表示为:
2KClO3+4HCl (浓)==2KCl+2ClO2↑+Cl2↑+2H2O。
(1)请分析该反应中电子转移的情况(用双线桥法表示)。
(2)浓盐酸在反应中显示出来的性质是________(填序号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)若产生0.1 mol Cl2,则转移的电子的物质的量为________mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com