
卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解。
(1)卤族元素位于周期表的_________区;溴的电子排布式为______________。
(2)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在。使氢氟酸分子缔合的作用力是 。
(3)根据下表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是 。
| 氟 | 氯 | 溴 | 碘 | 铍 | |
| 第一电离能 (kJ/mol) | 1681 | 1251 | 1140 | 1008 | 900 |

(4)已知高碘酸有两种形式,化学式分别为H5IO6和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6_____HIO4(填“>”、“<”或“=”)
(5)已知ClO2-立体构型为V型。ClO2-中心氯原子的杂化轨道类型为___________,写出CN-的等电子体的化学式__________(写出1个)
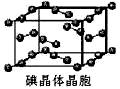 (6)下图为碘晶体晶胞结构。有关说法中正确的是_____________。
(6)下图为碘晶体晶胞结构。有关说法中正确的是_____________。
A、用均摊法可知平均每个晶胞中有4个碘原子
B、碘晶体为无限延伸的空间结构,是原子晶体
C、碘晶体中存在非极性键和范德华力
科目:高中化学 来源: 题型:
粗食盐中除含有钙离子、镁离子、硫酸根离子等可溶性杂质外,还含有泥沙等不溶性杂质。为了除去杂质在实验室中可将粗盐溶于水然后进行下列操作:(1)过滤;(2)加入过量的氢氧化钠溶液;(3)加入适量的盐酸;(4)加过量Na2CO3溶液;(5)加过量的BaCl2溶液。通过教材中“粗盐的提纯”及你做过的该实验回答下列问题。
(1)以上操作的正确顺序是( )
A.(5)(4)(2)(1)(3) B.(1)(2)(3)(4)(5)
C.(5)(4)(3)(2)(1) D.(1)(5)(4)(2)(3)
(2)实验室进行NaCl溶液蒸发时,一般有以下操作过程:①放置酒精灯;②固定铁圈位置;③放上蒸发皿(蒸发皿中盛有NaCl溶液);④加热搅拌;⑤停止加热。其正确的操作顺序为___________。(3)如何运用最简的方法检验溶液中有无SO42―离子?______________________________。如果有,应该如何除去SO42―离子?___________________________________________。(4)在粗盐经过溶解等步骤后,在过滤前的溶液中滴加饱和Na2CO3溶液,直至不再产生沉淀为止。这步操作的目的是______________________________________________。(5)将经过操作(4)后的溶液过滤。请问这一操作能除掉哪些杂质?(6)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的。溶解时:__________________________________________________________________。过滤时:__________________________________________________________________。蒸发时:__________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
水是一种重要的自然资源,是人类赖以生存不可缺少的物质。水质优劣直接影响人体健康。请回答下列问题:
(l)天然水中溶解的气体主要有____、____ ______(填化学式)。
(2)检验蒸馏水的纯度时,最简单易行的方法是测定水的____。
(3)水的净化与软化的区别是:水的净化是用混凝剂(如明矾等)使____,而水的软化是(4)。
(4)通过施加一定压力使水分子透过半透膜而将大分子或离子截留,从而使水得以净化的方法称为____;电渗析法净化水时,使离子通过半透膜的推动力是____。
(5)某天然水中。c(Ca2+)=1.2×10-3mol/L, c(Mg2+)=6×10-4mol/L, c(HCO3-)=8×10-4mol/L
要软化10  这种天然水,需先加入Ca(OH)2_______g,再加入Na2CO3_______g。
这种天然水,需先加入Ca(OH)2_______g,再加入Na2CO3_______g。
查看答案和解析>>
科目:高中化学 来源: 题型:
CO2的资源利用是解决温室效应的重要途径。以下是在一定条件下用NH3捕获CO2生成重要化工产品三聚氰酸的反应(未配平):
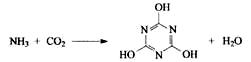
下列有关三聚氰酸的说法正确的是
A、分子式为C3H6N3O3 B、分子中既含极性键,又含非极性键
C、属于共价化合物 D、生成该物质的上述反应为中和反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各化学反应的离子方程式中,有错误的是( )
A.铝与氢氧化钠反应:2Al+2OH-+2H2O=2AlO2-+3 H2↑
B.氧化铝溶于氢氧化钠溶液:Al2O3+2OH-=2AlO2-+H2O
C.碘化亚铁溶液中滴入足量溴水:2Fe2++2I-+2Br2=I2+2Fe3++4Br-
D.碳酸氢镁溶液中加过量澄清石灰水
Mg2++2HCO3-+2Ca2++4OH-=2CaCO3↓+2H2O+Mg(OH)2↓
查看答案和解析>>
科目:高中化学 来源: 题型:
下列制取、检验、提纯或保存物质的方法可行的是( )
①向某溶液中加入KSCN溶液,检验该溶液是否含有Fe3+
②用植物油、NaOH溶液制取肥皂 ③向FeCl3饱和溶液中滴加NaOH溶液制取Fe(OH)3胶体 ④用焰色反应检验K+时需透过蓝色钴玻璃观察 ⑤少量液溴用水液封后密封保存在棕色试剂瓶中 ⑥向混有乙酸的乙酸乙酯中加入NaOH溶液后再分液,提纯乙酸乙酯
A.①③⑤⑥ B.②④⑤⑥ C.①②④⑤ D.①③④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
使等体积的AlCl3.CaCl2.NaCl溶液中的Cl-完全转化为AgCl沉淀,所用0.1 mol/L AgNO3溶液的体积相同,则这三种溶液的物质的量浓度之比为( )
A.1:2:3 B.1:1:1 C.2:3:6 D.6:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室制Cl2反应为4HCl(浓)+MnO2 MnCl2+Cl2↑+2H2O下列说法不正确的是( )。
MnCl2+Cl2↑+2H2O下列说法不正确的是( )。
A.还原剂是HCl,氧化剂是MnO2
B.每生成1 mol Cl2,转移电子的物质的量为2 mol
C.每消耗1 mol MnO2,起还原剂作用的HCl消耗4 mol
D.转移电子的物质的量为1 mol时,生成标准状况下Cl2的体积为11.2 L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com