
【题目】向1 L的密闭容器中加入1 mol X、0.3 mol Z和一定量的Y三种气体。一定条件下发生反应,各物质的浓度随时间变化如图一所示。图二为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。下列说法不正确的是
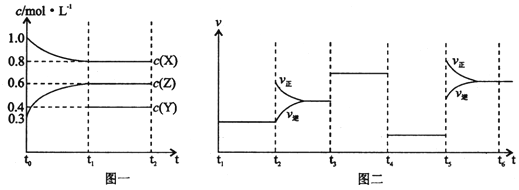
A.Y的起始物质的量为0.5 mol
B.该反应的化学方程式为:2X(g)+Y(g) ![]() 3Z(g) H<0
3Z(g) H<0
C.若t0=0,t1=10 s,则t0~t1阶段的平均反应速率为v(Z)=0.03 mol/(L·s)
D.反应物X的转化率t6点比t3点高
【答案】B
【解析】
试题分析:t3~t4阶段与t4~t5阶段正逆反应速率都相等,而t3~t4阶段为使用催化剂,如t4~t5阶段改变的条件为降低反应温度,平衡移动发生移动,则正逆反应速率不相等,则t4~t5阶段应为减小压强;反应中X的浓度变化为1mol/L-0.8mol/L=0.2mol/L,Z的浓度变化为0.6mol/L-0.3mol/L=0.3mol/L,则X、Z的化学计量数之比为2:3,该反应为气体体积不变的反应,则Y为反应物,该反应为2X(g)+Y(g)![]() 3Z(g),t5时为升高温度,平衡正向移动,说明正反应H>0。A.X减少0.2mol/L,则Y减少0.1mol/L,则起始Y的浓度为0.1mol/L+0.4mol/L=0.5mol/L,起始物质的量为0.5mol/L×2L=1mol,故A正确;B.由上述分析可知,此温度下该反应的化学方程式为2X(g)+Y(g)
3Z(g),t5时为升高温度,平衡正向移动,说明正反应H>0。A.X减少0.2mol/L,则Y减少0.1mol/L,则起始Y的浓度为0.1mol/L+0.4mol/L=0.5mol/L,起始物质的量为0.5mol/L×2L=1mol,故A正确;B.由上述分析可知,此温度下该反应的化学方程式为2X(g)+Y(g)![]() 3Z(g)H>0,故B错误;C.若t0=0,t1=10 s,则t0~t1阶段的平均反应速率为v(Z)=
3Z(g)H>0,故B错误;C.若t0=0,t1=10 s,则t0~t1阶段的平均反应速率为v(Z)=![]() =0.03 mol/(L·s),故C正确;D.t3为使用催化剂,平衡不移动,t5时为升高温度,平衡正向移动,反应物X的转化率t6点比t3点高,故D正确;故选B。
=0.03 mol/(L·s),故C正确;D.t3为使用催化剂,平衡不移动,t5时为升高温度,平衡正向移动,反应物X的转化率t6点比t3点高,故D正确;故选B。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】结合下表回答下列问题(均为常温下的数据):
酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) |
CH3COOH | 1.8×10-5 | H2CO3 | K1=4.4×10-7 | H2C2O4 | K1=5.4×10-2 | H2S | K1=1.3×10-7 |
HClO | 3×10-8 | K2=4.7×10-11 | K2=5.4×10-5 | K2=7.1×10-15 |
请回答下列问题:
(1) 同浓度的CH3COO-、HCO3-、CO32-、HC2O4-、ClO-、S2-中结合H+的能力最弱的是_________。
(2) 0.1mo1/L的H2C2O4溶液与0.1mo1/L的KOH的溶液等体积混合后所得溶液呈酸性,该溶液中各离子浓度由大到小的顺序为________________。
(3)pH相同的NaC1O和CH3COOK溶液中,[c(Na+)-c(C1O-)]______[c(K+)-c(CH3COO-)](填“>”、“<”或“=”) 。
(4) 向0.1mo1/LCH3COOH 溶液中滴加NaOH 溶液至c(CH3COOH): c(CH3COO-)=5:9,此时溶液pH=_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、氧、氯、镁、镍、铜是几种重要的元素,请回答下列问题:
(1)镍元素的核电荷数为28,则基态原子的电子排布式为____________________,结构中有__________种不同形状的电子云。
(2)MgO的熔点高于CuO的理由是________________________________________。
(3)镁原子第一电离能反常地高于铝的原因是_____________________________。
(4)Ni与CO能形成配合物![]() ,该分子中
,该分子中![]() 键与
键与![]() 键个数比为__________。
键个数比为__________。
(5) ![]() 分子中的中心原子杂化轨道类型是__________,该分子的空间构型为__________。
分子中的中心原子杂化轨道类型是__________,该分子的空间构型为__________。
(6)铜与氧可形成如图所示的晶胞结构,其中铜原子均匀地分散在晶胞内部,a、b原子的坐标参数依次为(0,0,0)、![]() ,则d原子的坐标参数为____________________,已知:该晶体的密度为
,则d原子的坐标参数为____________________,已知:该晶体的密度为![]() ,
, ![]() 是阿伏加德罗常数的值,则晶胞参数为__________cm(列出计算式即可)。
是阿伏加德罗常数的值,则晶胞参数为__________cm(列出计算式即可)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正丁醚常用作有机反应的溶剂。实验室制备正丁醚的反应和主要实验装置如下:2CH3CH2CH2CH2OH![]() (CH3CH2CH2CH2)2O+H2O,反应物和产物的相关数据如下表:
(CH3CH2CH2CH2)2O+H2O,反应物和产物的相关数据如下表:
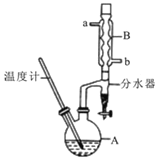

①将6 mL浓硫酸和37 g正丁醇,按一定顺序添加到A中,并加几粒沸石。
②加热A中反应液,迅速升温至135℃,维持反应一段时间。
③分离提纯:待A中液体冷却后将其缓慢倒入盛有70 mL水的温度分液漏斗中,振摇后静置,分液得粗产物。
④粗产物依次用40 mL水、20 mL NaOH溶液和40 mL水洗涤,分液后加入约3g无水氯化钙颗粒,静置一段时间后弃去氯化钙。
⑤将上述处理过的粗产物进行蒸馏,收集馏分,得纯净正丁醚11g。请回答:
(1)步骤①中浓硫酸和正丁醇的添加顺序为:应先加 。
(2)加热A前,需先从 (填“a”或“b”)口向B中通入水。
(3)步骤③的目的是初步洗去 ,振摇后静置,粗产物应 (填“上”或“下”)口倒出。
(4)步骤⑤中,加热蒸馏时应收集 (填选项字母)左右的馏分。
A.100℃ B.117℃ C.135℃ D.142℃
(5)反应过程中会观察到分水器中收集到液体物质,且分为上下两层,随着反应的进行,分水器中液体逐渐增多至充满时,上层液体会从左侧支管自动流回A。分水器中上层液体的主要成分为 ,下层液体的主要成分为 。
(6)本实验中,正丁醚的产率为 (精确到1%)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然食用香料X是芳香族化合物,可以从某些植物中提取。由x合成H的路线如下:
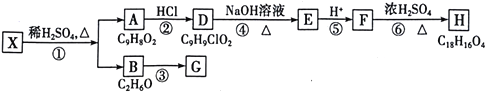
已知:①A的核磁共振氢谱有6个峰;②H为酯类物质,结构中除苯环外还含有一个六元环;③G的产量是衡量一个国家石油化工发展水平的标志。
请回答下列问题:
(1)A的结构简式为_____________________________。
(2)⑥的反应类型为___________________,反应③的化学方程式为___________________________。
(3)F中所含官能团的名称为_________________,其同分异构体中,遇FeCl3溶液发生显色反应,且能与碳酸氢钠溶液反应,其苯环上一氯代物只有一种,符合条件的同分异构体数目为______种,写出其中一种结构简式__________________________________。
(4)设计一条以G为起始原料合成乙二酸的路线________________(无机物任选,注明反应条件),示例如下:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中可以获得淡水、食盐并可提取镁和溴等物质.
(1)海水淡化的方法主要有_____________、电渗析法、________________ 。
(2)必须经过化学变化才能从海水中获得的物质是(填序号)_____________.
A.氯、溴、碘 B.钠、镁、铝 C.烧碱、氢气 D.食盐、淡水
(3)从海水中提取镁的流程如图所示:
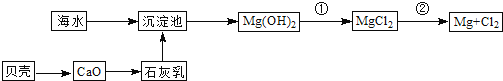
反应②的化学方程式为_________________________________________________。
(4)从海水中提取溴的主要步骤是向浓缩的海水中通入氯气,将溴离子氧化生成溴。向溴单质的水溶液中通入空气和水蒸气将溴单质吹入盛有SO2溶液的吸收塔,其目的是_________,该反应的化学方程式为________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体X和气体Y各0.16mol充入10 L恒容密闭容器中,发生反应:X(g)+Y(g)![]() 2Z(g) △H<0。反应过程中测定的数据如下表:
2Z(g) △H<0。反应过程中测定的数据如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
请计算:
(1)反应前2 min的平均速率ν(Z) = __________________________,
(2)到达平衡时,X的转化率为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关化学与生产、生活相关的叙述正确的是( )
A.碘酒能消毒是利用碘的还原性
B.葡萄糖注射液不能产生丁达尔效应,不属于胶体
C.14C可用于文物的年代鉴定,14C与12C互为同素异形体
D.某溶液中加盐酸,生成的气体能使澄清石灰水变浑浊,则原溶液中一定含有CO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为短周期元素,A~E原子序数依次增大,质子数之和为40,B、C同周期,A、D同主族,A、C能形成两种液态化合物A2C和A2C2,E是地壳中含量最多的金属元素。试回答:
(1)B元素在周期表中的位置为__________;
(2)将D的单质投入A2C中,反应后得到一种无色溶液。E的单质在该无色溶液中反应的离子方程式为__________;
(3)A、C两元素可组成10电子粒子X-,Y与X-具有相同的原子种类及数目,且不带电,Y的电子式为__________;
(4)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2C2和稀硫酸浸泡既达到了上述目的,又保护了环境,该反应的化学方程式为__________;
(5)我国首创的海洋电池以E的单质为负极,铂网为正极,空气做氧化剂,海水做电解质溶液。电池的正极反应式为__________,电池总反应的化学方程式为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com