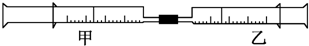
分析:(1)①配制480mL 0.1mol?L
-1 NaOH溶液,应选择500ml容量瓶,依据m=CVM计算需要氢氧化钠的质量;
②依据配制一定物质的量浓度步骤选择合适的仪器;
③依据容量瓶查漏的正确方法解答;
④依据C=
进行误差分析,凡是能够使n增大,或者使V减小的操作,都会使C偏大;凡是能够使n减小,V增大的操作都会使C偏小;
⑤试剂瓶标签应标明溶液名称和物质的量浓度;
(2)依据托盘天平的正确使用方法和注意事项以及配制一定物质的量浓度溶液的正确操作步骤解答.
解答:
解:(1)①配制500ml 0.1mol?L
-1 NaOH溶液,需要氢氧化钠的质量m=0.5L×0.1mol?L
-1×40g/mol=2.0 g,故答案为:2.0;
②配制一定物质的量浓度溶液的一般步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶贴标签等,需要的仪器有:托盘天平、药匙、烧杯、玻璃棒、量筒、500mL容量瓶、胶头滴管;
故答案为:500mL容量瓶;胶头滴管;
③容量瓶使用前应先检查是否漏水,方法是:在容量瓶内装入半瓶水,塞紧瓶塞,用右手食指顶住瓶塞,另一只手五指托住容量瓶底,将其倒立(瓶口朝下),观察容量瓶是否漏水.若不漏水,将瓶正立且将瓶塞旋转180°后,再次倒立,检查是否漏水,若两次操作,容量瓶瓶塞周围皆无水漏出,即表明容量瓶不漏水.经检查不漏水的容量瓶才能使用;
故答案为:在容量瓶内装入半瓶水,塞紧瓶塞,用右手食指顶住瓶塞,另一只手五指托住容量瓶底,将其倒立(瓶口朝下),观察容量瓶是否漏水.若不漏水,将瓶正立且将瓶塞旋转180°后,再次倒立,检查是否漏水,若两次操作,容量瓶瓶塞周围皆无水漏出,即表明容量瓶不漏水.经检查不漏水的容量瓶才能使用;
④i 定容时俯视刻度线,导致溶液的体积偏小,溶液的浓度偏高,故选A;
ii 放在滤纸上称量NaOH固体,导致称取的氢氧化钠的质量偏小,溶质的物质的量偏小,溶液的浓度偏低,故选B;
iii 搅拌或转移时,有液体溅出,导致溶质的物质的量偏小,溶液的浓度偏低,故选B;
iv 未冷至室温就转移定容,冷却后溶液的体积偏小,溶液的浓度偏高,故选A;
v 转移前,容量瓶内有蒸馏水,对溶质的物质的量和溶液的体积不会产生影响,故选C;
vi 定容时水多用胶头滴管吸出,吸出的液体中含有溶质,溶质的物质的量偏小,溶液的浓度偏低,故选B;
⑤试剂瓶(盛放上述配制好的溶液)上标签:
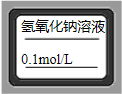
,故答案为:NaOH溶液;0.1mol?L
-1;
(2)使用托盘天平时,应先调节平衡,称量一般固体用滤纸即可,称量氢氧化钠固体等腐蚀性物质时应放在干燥的烧杯中,称量完毕游码应拨回原处,托盘天平的精确度为0.1g,读数时应保留小数点后1为;
配制一定物质的量浓度溶液,计算出需要的氢氧化钠的质量,放在烧杯中加适量蒸馏水溶解,冷却到室温后进行移液,移液时应用玻璃棒引流,然后用蒸馏水洗涤烧杯内壁和玻璃棒2-3次,洗涤液亦应转入容量瓶,然后加蒸馏水到离刻度线1-2cm,改用胶头滴管逐滴滴加到凹液面最低处与刻度线相切,然后摇动容量瓶,使溶液混合均匀,将配合的溶液装入带胶塞的试剂瓶内;
故答案为:(1)NaOH应放在干燥的烧杯中称量(2)用过的游码未拨回原处(3)托盘天平只能称出0.1~0.2g,称不出1.00g(4)烧杯和玻璃棒未洗涤,洗涤液亦应转入容量瓶(5)溶解NaOH应冷却后再转移至容量瓶中(6)容量瓶中的溶液未摇匀(7)配好的溶液应及时转移到有胶塞的试剂瓶内.


 ,故答案为:NaOH溶液;0.1mol?L-1;
,故答案为:NaOH溶液;0.1mol?L-1;

 .请写出A与稀、冷的KMnO4溶液在碱性
.请写出A与稀、冷的KMnO4溶液在碱性