
【题目】如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极.
接通电源,经过一段时间后,测得丙中K2SO4的质量分数为10.47%,乙中c电极质量增加.回答问题: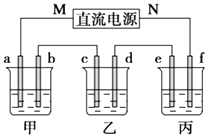
(1)电源的N端为极;
(2)电极b上发生的电极反应式为;
(3)丙装置损失的质量为(该处保留两位有效数字);电极b上生成的气体在标准状况下的体积为;
(4)电极c的质量变化是g;
(5)①若该直流电源为甲烷燃料电池,电解质溶液为KOH溶液.通入甲烷的铂电极上发生的电极反应式为 .
②已知上述燃料电池中,每转移1mol电子,就有 112KJ的化学能转化为电能.写出常温下甲烷燃烧的热化学方程式 .
【答案】
(1)正
(2)4OH﹣﹣4e﹣=2H2O+O2↑
(3)4.49g;2.8L
(4)16g
(5)CH4﹣8e﹣+10OH﹣=CO32﹣+7H2O;CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣896kJ/mol
【解析】解:(1)该装置是电解池,接通电源,经过一段时间后,乙中c电极质量增加,说明c电极是电解池阴极,则d电极是阳极,连接电解池阳极的N端电极是正极,所以答案是:正;(2)电解氢氧化钠溶液时,阳极上氢氧根离子放电生成氧气,电极反应式为:4OH﹣﹣4e﹣=2H2O+O2↑,所以答案是:4OH﹣﹣4e﹣=2H2O+O2↑;(3)l00g 10.00%的K2SO4溶液电解一段时间后K2SO4浓度变为 ![]() ,电解硫酸钾溶液实际上是电解的水,所以电解水的质量为100﹣
,电解硫酸钾溶液实际上是电解的水,所以电解水的质量为100﹣ ![]() =4.49g,减少4.49g水即为0.25mol.由方程式2H2+O2═2H2O可知,生成2molH2O,转移4mol电子,所以整个反应中转化0.5mol电子,则电极b上生成的气体在标准状况下的体积为
=4.49g,减少4.49g水即为0.25mol.由方程式2H2+O2═2H2O可知,生成2molH2O,转移4mol电子,所以整个反应中转化0.5mol电子,则电极b上生成的气体在标准状况下的体积为 ![]() ×22.4L/mol=2.8L;所以答案是:4.49g;2.8L;(4)因为连接电解池阳极的N端电极是正极,则M为负极,所以c电极为析出铜,由(3)得整个反应中转化0.5mol电子,则电极c增加的质量=
×22.4L/mol=2.8L;所以答案是:4.49g;2.8L;(4)因为连接电解池阳极的N端电极是正极,则M为负极,所以c电极为析出铜,由(3)得整个反应中转化0.5mol电子,则电极c增加的质量= ![]() ×64g/mol=16g.所以答案是:16g;(5)①甲烷燃料电池中,负极上甲烷失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为:CH4﹣8e﹣+10OH﹣=CO32﹣+7H2O,
×64g/mol=16g.所以答案是:16g;(5)①甲烷燃料电池中,负极上甲烷失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为:CH4﹣8e﹣+10OH﹣=CO32﹣+7H2O,
所以答案是:CH4﹣8e﹣+10OH﹣=CO32﹣+7H2O;
②每转移1mol电子,就有112KJ的化学能转化为电能,所以1mol甲烷燃烧生成二氧化碳和液态水放热112kJ×8=896kJ,
甲烷燃烧的热化学方程式为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣896kJ/mol;
所以答案是:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣896kJ/mol.


科目:高中化学 来源: 题型:
【题目】过氧化氢H2O2,(氧的化合价为﹣1价),俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。对于下列A~D涉及H2O2的反应,填写空白:
A.Na2O2+2HCl===2NaCl+H2O2B.Ag2O+H2O2===2Ag+O2+H2O
C.2H2O2===2H2O+O2D.3H2O2+Cr2(SO4)3+10KOH===2K2CrO4+3K2SO4+8H2O
(1)H2O2仅体现氧化性的反应是__(填代号)。
(2)H2O2既体现氧化性又体现还原性的反应是__(填代号)。
(3)在稀硫酸中,KMnO4和H2O2能发生氧化还原反应。
氧化反应:H2O2﹣2e﹣===2H++O2↑
还原反应:MnO4﹣+5e﹣+8H+===Mn2++4H2O
写出该氧化还原反应的离子方程式:___________________。
(4)在K2Cr2O7+14HCl===2KCl+3Cl2↑+7H2O+2CrCl3的反应中,有0.3 mol电子转移时生成Cl2的体积为:_______标准状况),被氧化的HCl的物质的量为__。
(5)除去镁粉中混入的铝粉杂质用溶解、_______方法,化学反应方程式为_________。
(6)下列物质中:①NaNO3固体、②熔融KCl、③液氨、④石墨、⑤氯化氢、⑥盐酸、⑦蔗糖。其中:
属于电解质的是:__(填序号,下同);
既不是电解质也不是非电解质的是:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中的B~K分别代表有关反应的一种反应物或生成物,其中A、C、F、K是固体;E是常见的气体单质.固态物质A加热后生成的气体混合物若通过碱石灰只剩余气体B,若通过浓硫酸则只剩余气体D.各物质间的转化关系如图所示: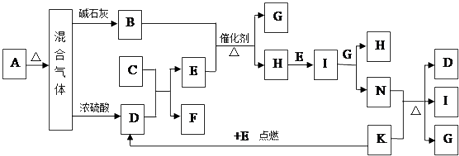
请回答下列问题:
(1)写出实验室检验A物质中含有的阳离子的方法
(2)B与E反应得到1molH,则此时转移电子的物质的量为mol.
(3)写出实验室制取B的化学方程式 .
(4)写出N的稀溶液与过量的铁粉反应的离子方程式 .
(5)若混合气体通过碱石灰得到的气体B与通过浓硫酸得到的气体D的物质的量之比是8:5,则用物质的量的关系表示此固体A的组成为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列仪器可以加热的是( )
①蒸馏烧瓶;②容量瓶;③蒸发皿;④试管;⑤表面皿;⑥分液漏斗;⑦量筒;⑧锥形瓶
A. ①③④⑧B. ②④⑥⑧C. ③④⑤D. ②③④⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列仪器:①烧杯;②锥形瓶;③圆底烧瓶;④试管;⑤坩埚;其中可以用酒精灯直接加热的仪器是( )
A. ①②③④ B. ④⑤ C. ①③ D. ④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食盐溶液中存在Ca2+、Mg2+、SO42-等杂质,除杂时加入NaOH、Na2CO3、BaCl2和盐酸,下列添加试剂顺序正确的有
①NaOH BaCl2Na2CO3HCl ②BaCl2HCl NaOH Na2CO3
③Na2CO3BaCl2NaOH HCl ④BaCl2 NaOH Na2CO3HCl
A. ①③B. ①④C. ③④D. ①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按如图所示装置进行实验,并回答下列问题: 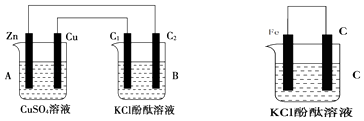
(1)判断装置的名称:A池为 , B池为 .
(2)锌极为极,电极反应式为;石墨棒C1为极,电极反应式为;石墨棒C2附近发生的实验现象为 .
(3)写出C 装置中溶液颜色变红的电极反应式: .
(4)当C2极析出224mL气体(标准状况下)时,CuSO4溶液的质量变化了g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是电解CuCl2溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是( ) 
A.a为负极,b为正极
B.d为阳极,c为阴极
C.电解过程中,d电极质量增加
D.电解过程中,氯离子浓度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Pd(相对原子质量207)中加入王水(浓硝酸与浓盐酸的混合物)的反应可以表示:Pd+HCl+HNO3→A+B↑+H2O(未配平).其中B为无色有毒气体,该气体在空气中不能稳定存在;A中含有三种元素,其中Pd元素的质量分数为42.4%,H元素的质量分数为0.8%.通过计算判断物质A的化学式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com