
【题目】如图中的B~K分别代表有关反应的一种反应物或生成物,其中A、C、F、K是固体;E是常见的气体单质.固态物质A加热后生成的气体混合物若通过碱石灰只剩余气体B,若通过浓硫酸则只剩余气体D.各物质间的转化关系如图所示: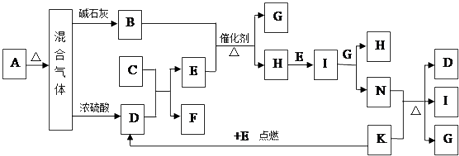
请回答下列问题:
(1)写出实验室检验A物质中含有的阳离子的方法
(2)B与E反应得到1molH,则此时转移电子的物质的量为mol.
(3)写出实验室制取B的化学方程式 .
(4)写出N的稀溶液与过量的铁粉反应的离子方程式 .
(5)若混合气体通过碱石灰得到的气体B与通过浓硫酸得到的气体D的物质的量之比是8:5,则用物质的量的关系表示此固体A的组成为
【答案】
(1)取适量A物质放入试管中,加入适量NaOH等强碱溶液并加热,若能产生使湿润的红色石蕊试纸变蓝的气体,则证明含有铵根离子
(2)5
(3)Ca(OH)2+2NH4Cl ![]() CaCl2+2H2O+2NH3↑或浓氨水加CaO或NaOH固体
CaCl2+2H2O+2NH3↑或浓氨水加CaO或NaOH固体
(4)3Fe+8H++2NO3﹣=2NO↑+3Fe2++4H2O
(5)NH4HCO3和(NH4)2CO3按物质的量之比为2:3混合而成
【解析】解:A、C、F、K是固体;E是常见的气体单质,I是红棕色的气态氧化物.固态物质A(混合物)加热后生成的气体混合物若通过碱石灰只剩余气体B,若通过浓硫酸则只剩余气体D,E是常见的气体单质,可以初步推断为O2 , I是红棕色的气态氧化物判断为NO2 , 依据转化关系可知H为NO,G为H2O,N为HNO3 , B为NH3 , .固态物质A(混合物)加热后生成的气体混合物若通过碱石灰只剩余气体B进一步确定B为NH3 , 若通过浓硫酸则只剩余气体D,说明D为酸性气体且无还原性,推测D为CO2 , 根据反应:N(HNO3)+K(C)=D(CO2)+I(NO2)+G(H2O),C为Na2O2 , F为(Na2CO3),所以A受热分解生成碱性气体NH3和酸性气体CO2 , 证明A为碳酸铵盐,(1)实验室检验A物质中含有的阳离子是NH4+的方法:取适量A物质放入试管中,加入适量NaOH等强碱溶液并加热,若能产生使湿润的红色石蕊试纸变蓝的气体,则证明含有铵根离子,所以答案是:取适量A物质放入试管中,加入适量NaOH等强碱溶液并加热,若能产生使湿润的红色石蕊试纸变蓝的气体,则证明含有铵根离子;(2)B与E反应是氨气的催化氧化反应,反应的化学方程式为:4NH3+5O2 ![]() 4NO+6H2O,得到H为NO,反应中生成4molNO电子转移20mol,则得到1molNO,此时转移电子的物质的量为5mol;所以答案是:5;(3)实验室制取B(NH3)的化学方程式为:Ca(OH)2+2NH4Cl
4NO+6H2O,得到H为NO,反应中生成4molNO电子转移20mol,则得到1molNO,此时转移电子的物质的量为5mol;所以答案是:5;(3)实验室制取B(NH3)的化学方程式为:Ca(OH)2+2NH4Cl ![]() CaCl2+2H2O+2NH3↑,或浓氨水加CaO或NaOH固体;所以答案是:Ca(OH)2+2NH4Cl
CaCl2+2H2O+2NH3↑,或浓氨水加CaO或NaOH固体;所以答案是:Ca(OH)2+2NH4Cl ![]() CaCl2+2H2O+2NH3↑或浓氨水加CaO或NaOH固体;(4)N的稀溶液HNO3与过量的铁粉反应生成亚铁盐,反应的离子方程式为:3Fe+8H++2NO3﹣═2NO↑+3Fe2++4H2O;所以答案是:3Fe+8H++2NO3﹣═2NO↑+3Fe2++4H2O;(5)混合气体通过碱石灰得到的气体B为NH3与通过浓硫酸得到的气体D(CO2)的物质的量之比是8:5,依据化学反应的原子守恒得到,若是碳酸氢铵,铵根离子和碳酸氢根离子物质的量之比为1:1,若为碳酸铵.铵根离子和碳酸根离子物质的量为2:1,混合气体中氨气和二氧化碳物质的量之比为8:5,介于1:1和2:1间,所以判断A为碳酸铵和碳酸氢铵的混合物,物质的量之比通过平均值法计算为3:2:则用物质的量的关系表示此固体A的组成为NH4HCO3和(NH4)2CO3按物质的量之比为2:3混合而成;所以答案是:NH4HCO3和(NH4)2CO3按物质的量之比为2:3混合而成.
CaCl2+2H2O+2NH3↑或浓氨水加CaO或NaOH固体;(4)N的稀溶液HNO3与过量的铁粉反应生成亚铁盐,反应的离子方程式为:3Fe+8H++2NO3﹣═2NO↑+3Fe2++4H2O;所以答案是:3Fe+8H++2NO3﹣═2NO↑+3Fe2++4H2O;(5)混合气体通过碱石灰得到的气体B为NH3与通过浓硫酸得到的气体D(CO2)的物质的量之比是8:5,依据化学反应的原子守恒得到,若是碳酸氢铵,铵根离子和碳酸氢根离子物质的量之比为1:1,若为碳酸铵.铵根离子和碳酸根离子物质的量为2:1,混合气体中氨气和二氧化碳物质的量之比为8:5,介于1:1和2:1间,所以判断A为碳酸铵和碳酸氢铵的混合物,物质的量之比通过平均值法计算为3:2:则用物质的量的关系表示此固体A的组成为NH4HCO3和(NH4)2CO3按物质的量之比为2:3混合而成;所以答案是:NH4HCO3和(NH4)2CO3按物质的量之比为2:3混合而成.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
【题目】3.6g碳在一定量的氧气中燃烧,反应后生成的混合气体相对氢气的密度是16,则生成的一氧化碳的质量是(相对密度指在相同的温度和压强下物质的密度之比)
A. 3.3 g B. 6.3 g C. 8.4 g D. 13.2 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子,在溶液中能大量共存,加入H2SO4溶液后既有气体放出又有沉淀生成的一组是( )
A.Ba2+、NO ![]() 、NH
、NH ![]() 、Cl﹣
、Cl﹣
B.Ba2+、HCO ![]() 、NH
、NH ![]() 、NO
、NO ![]()
C.K+、Cu2+、Cl﹣、OH﹣
D.Na+、CO ![]() 、SO
、SO ![]() 、K+
、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是(NA为阿伏加德罗常数的值) ( )
A. 硫酸的摩尔质量是98 g
B. 1molO2的质量是32g/mol
C. 2g氢气所含原子数目为2NA
D. 标准状况下,11.2LCH4的物质的量为0.5mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是四种常见的短周期元素其原子半径随原子序数的变化如下图。
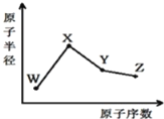
已知W一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期中最强。下列说法正确的是 ( )
A. 对应的气态氢化物的稳定性:Y>Z
B. X的非金属性是同周期中最强的
C. 对应简单离子的半径:X>W
D. Y的氧化物能与X的最高价氧化物对应的水化物反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E均为短周期主族元素,其原子序数依次增大。其中A元素原子核内只有一个质子;A与C、B与D分别同主族;B、D两元素原子序数之和是A、C两元素原子序数之和的2倍。
请回答下列问题:
(1)由上述元素组成的下列物质中属于非电解质的是________(填字母)。
A.C2B2 B.DB2 C.E2 D.C2DB3
(2)D元素在元素周期表中的位置为_______________________________;化合物C2B中两种离子的半径大小关系为________>________(填离子符号)。
(3)实验室中欲选用下列装置制取并收集纯净干燥的E2气体。实验中应选用的装置为________________(按由左到右的连接顺序填写);
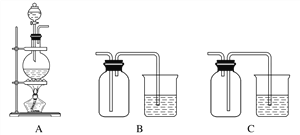
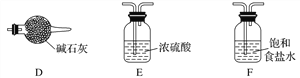
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极.
接通电源,经过一段时间后,测得丙中K2SO4的质量分数为10.47%,乙中c电极质量增加.回答问题: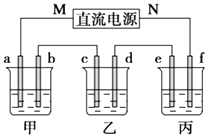
(1)电源的N端为极;
(2)电极b上发生的电极反应式为;
(3)丙装置损失的质量为(该处保留两位有效数字);电极b上生成的气体在标准状况下的体积为;
(4)电极c的质量变化是g;
(5)①若该直流电源为甲烷燃料电池,电解质溶液为KOH溶液.通入甲烷的铂电极上发生的电极反应式为 .
②已知上述燃料电池中,每转移1mol电子,就有 112KJ的化学能转化为电能.写出常温下甲烷燃烧的热化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】小明体检的血液化验单中,葡萄糖为5.9 mmol/L。表示该体检指标的物理量是( )。
A. 溶解度 B. 物质的量浓度
C. 质量分数 D. 摩尔质量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com