
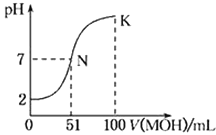
【题目】常温下,向100 mL 0.01 mol·L-1HA溶液中逐滴加入0.02 mol·L-1的MOH溶液,如中所示曲线表示混合溶液的pH变化情况。下列说法中正确的是( )
A.HA为一元弱酸,MOH为一元强碱
B.滴入MOH溶液的体积为50 mL时,c(M+)>c(A-)
C.N点水的电离程度大于K点水的电离程度
D.K点时,c(MOH)+ c(M+)=0.02 mol·L-1
【答案】C
【解析】
A.0.01molL-1 HA溶液中pH=2,则HA是强酸,与50mL碱溶液恰好反应后,溶液呈酸性,而与51mL碱恰好反应溶液呈中性,说明碱为弱碱,A错误;
B.MOH是弱碱,滴入MOH溶液的体积为50 mL时,溶液呈酸性,由电荷守恒可知溶液中c(A-)>c(M+),B错误;
C.由图像可知,N点溶液呈中性,水电离的氢离子为10-7mol/L,K点溶液呈碱性,MOH电离的氢氧根离子抑制了水电离,水电离的氢离子小于10-7mol/L,所以N点水的电离程度大于K点水的电离程度,C正确;
D.在K点时混合溶液体积是酸溶液的2倍,物质的量也是HA的2倍,所以c(MOH)+ c(M+)=![]() =0.01 mol·L-1,D错误;
=0.01 mol·L-1,D错误;
故答案选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】元素铬(Cr)在自然界主要以+3价和+6价存在。
(1)+6价的Cr能引起细胞的突变而对人体不利,可用亚硫酸钠将其还原。离子反应方程式为:3SO32-+Cr2O72-+8H+===2Cr3++3SO42-+4H2O,该反应氧化剂和还原剂的物质的量之比为___________。
(2)工业上利用铬铁矿( FeO. Cr2O3)冶炼铬的工艺流程如图所示:
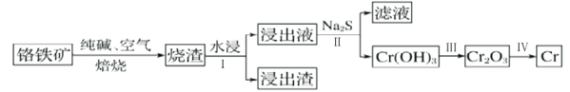
①为加快焙烧速率和提高原料的利用率,可采取的措施之一是___________。
②水浸Ⅰ要获得浸出液的操作是___________。
③浸出液的主要成分为Na2CrO4,加入Na2S反应后有Na2SO4生成,则操作Ⅱ发生反应的离子方程式为___________。
(3)常温下Cr(OH)3的溶度积Ksp=1×10-32,若要使Cr3+完全沉淀pH为___________[c(Cr3+)降至10-5mol·L-1可认为完全沉淀]。
(4)以铬酸钠(Na2CrO4)为原料,用电化学法可制备重铬酸钠(Na2Cr2O7),实验装置如图所示(已知:2CrO42-+2H+=Cr2O72-+H2O)。
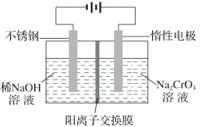
①阳极的电极反应式为___________。
②电解一段时间后,测得阳极区溶液中Na+物质的量由amol变为bmol,则生成重铬酸钠的物质的量为___________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.实验室利用铜和稀硝酸制备一氧化氮:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,该反应的离子方程式为___。每生成11.2LNO(标准状况),转移的电子数为___NA。
Ⅱ.(1)在发射“神舟”十一号的火箭推进器中装有肼(N2H4)和过氧化氢,当两者混合时即产生气体,并放出大量的热。已知:
N2H4(l)+2H2O2(l)==N2(g)+4H2O(g) ΔH1;
H2O(l)==H2O(g) ΔH2
请写出液态肼与足量过氧化氢反应生成氮气和液态水的热化学方程式:_____。
(2)在25℃,101kPa下,1molCO完全燃烧放出283.0kJ的热量。请写出表示CO燃烧热的热化学方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X为Fe2O3和CuO的混合物且氧化性强弱顺序:Fe3+>Cu2+>H+>Fe2+。X样品可发生如图所示的转化关系:
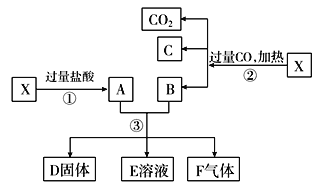
(1)写出步骤③可能发生反应的离子方程式:________________________(共有3个,任写一个即可)。
(2)若溶液E中只有一种金属离子,则一定是__________;若溶液E中含有两种金属离子,则一定是________。
(3)若D固体是纯净物,该固体是________(填化学式)。
(4)印刷电路板是由高分子材料和铜箔复合而成的,可用FeCl3溶液作“腐蚀剂”刻制印刷电路板,该过程发生反应的离子方程式为____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用I2O5可消除CO污染,反应为I2O5(s)+5CO(g)![]() 5CO2(g)+I2(s)。不同温度下,向装有足量的I2O5固体的2L恒容密闭容器中通入2mol CO,测得CO2 的体积分数ψ(CO2)随时间t变化曲线如右图,下列说法正确的是
5CO2(g)+I2(s)。不同温度下,向装有足量的I2O5固体的2L恒容密闭容器中通入2mol CO,测得CO2 的体积分数ψ(CO2)随时间t变化曲线如右图,下列说法正确的是

A. b点时,CO的转化率为20%
B. 容器内的压强保持恒定,表明反应达到平衡状态
C. b点和d点的化学平衡常数:Kb>Kd
D. 0到0.5min反应速率v(CO)=0.3mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有a、b、c、d四个金属电极,有关的反应装置及部分反应现象如下:
实验装置 | 部分实验现象 |
| a极质量减小,b极质量增加 |
| b极有气体产生,c极无变化 |
| d极溶解,c极有气体产生 |
| 电流计指示在导线中电流从a极流向d极 |
由此可判断这四种金属的活动性顺序是( )
A.a>b>c>dB.b>c>d>aC.d>a>b>cD.a>b>d>c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以重晶石(BaSO4)为原料,可按如下工艺生产立德粉(ZnS·BaSO4):
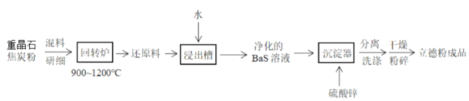
下列说法不正确的是
A.在回转炉中重晶石被过量焦炭还原为可溶性硫化钡,该过程的化学方程式为BaSO4+4C![]() BaS+4CO↑
BaS+4CO↑
B.回转炉尾气中含有有毒气体,生产上可通过水蒸气变换将其转化为CO2和一种清洁能源气体,该反应的化学方程式为CO+H2O![]() CO2+H2
CO2+H2
C.在潮湿空气中长期放置的“还原料”。会逸出臭鸡蛋气味的气体,且水溶性变差。其原因是“还原料”表面生成了难溶于水的BaSO4
D.沉淀器中发生的离子反应方程式为:S2-+Ba2++Zn2++SO42-=ZnS·BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一种锂电池,用金属锂和石墨作电极材料,电解质溶液是由四氯铝锂(LiAlCl4)溶解在亚硫酰氯(![]() )中而形成的,电池总反应方程式为:8Li+3SOCl2===6LiCl+Li2SO3+2S,下列叙述中正确的是( )
)中而形成的,电池总反应方程式为:8Li+3SOCl2===6LiCl+Li2SO3+2S,下列叙述中正确的是( )
A. 电解质溶液中混入水,对电池反应无影响
B. 金属锂作电池的正极,石墨作电池的负极
C. 电池工作过程中,亚硫酰氯(SOCl2)被还原为Li2SO3
D. 电池工作过程中,金属锂提供的电子与正极区析出的硫的物质的量之比为4∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式中的反应热,表示燃烧热的是( )
A. NH3(g)+![]() O2(g)
O2(g)![]()
![]() N2(g)+
N2(g)+![]() H2O(g) ΔH=-a kJ·mol-1
H2O(g) ΔH=-a kJ·mol-1
B. C6H12O6(s)+6O2(g)![]() 6CO2(g)+6H2O(l) ΔH=-b kJ·mol-1
6CO2(g)+6H2O(l) ΔH=-b kJ·mol-1
C. C(s) +H2O(g) == CO(g)+H2(g) H=-c kJ·mol-1
D. CH3CH2OH(l)+![]() O2(g)
O2(g)![]() CH3CHO(l)+H2O(l) ΔH=-d kJ·mol-1
CH3CHO(l)+H2O(l) ΔH=-d kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com