
����Ŀ��������������Ҫ������������ԭ��������ˮ��Һ�ֳ�Ϊ˫��ˮ��������������ɱ����Ư�ȡ�ij��ѧ��ȤС��ȡһ�����Ĺ���������Һ��ȷ�ⶨ�˹�������ĺ���������д���пհף�
��ȡ10.00 mL�ܶ�Ϊ�� g/mL�Ĺ�������ԭ��Һϡ�ͳ�250 mL����ȡϡ����������Һ25.00 mL����ƿ�У�����ϡ�����ữ��������ˮϡ�ͣ�������������
��1���ø�����ط�(һ��������ԭ�ζ���)�ɲⶨ����Һ�е�H2O2�ĺ�������������Ũ��Ϊ0.10 mol��L1��KMnO4����Һ500 mL��Ӧȷ��ȡ_________g KMnO4[��֪M(KMnO4)=158.0 g��mol1]��
a.���Ƹñ���Һʱ�����������в���Ҫ�õ�����_________��(�ñ�ű�ʾ)��
��������ƽ ���ձ� ����Ͳ �������� ������ƿ ����ͷ�ι� ����Һ��
b.����ʱ���Ӷ������������ս��__________(�ƫ��ƫС�����䡱)��
��2����ɲ���ƽ���ӷ���ʽ��
![]()
![]() ��
��![]() H2O2��
H2O2��![]()
![]()
![]() Mn2+��
Mn2+��![]() O2����
O2����![]()
��3���ζ�ʱ����������ر���Һע��____________(���ʽ����ʽ��)�ζ����С��ζ������յ��������____________________________________________��
��4���ظ��ζ����Σ�ƽ������KMnO4����ҺV mL����ԭ����������Һ�й����������������Ϊ_____________��
��5�����ζ�ǰ�ζ��ܼ����������ݣ��ζ���������ʧ����ⶨ���______________ (�ƫ�ߡ���ƫ�͡����䡱)��
���𰸡���1��7.9 ���� ƫС
��2��2 5 6 H+ 2 5 8H2O
��3����ʽ�������һ�θ��������Һ����Һ����ɫ��Ϊdz��ɫ(����ɫ)����30���ڲ���ɫ
��4��![]()
��5��ƫ��
�����������⿼����һ�����ʵ���Ũ����Һ�����Ƽ����������ζ���������ԭ��Ӧ����ƽ����1���ø�����ط�(һ��������ԭ�ζ���)�ɲⶨ����Һ�е�H2O2�ĺ�������������Ũ��Ϊ0.10 mol��L1��KMnO4����Һ500 mL��Ӧȷ��ȡ������ص�����Ϊ��0.1 mol/L��0.5 L��158.0 g/mol=7.9 g���ù���������Һ��Ҫ��������ƽ�������������������ձ����ܽ⣬Ȼ��ת�Ƶ�����ƿ�У�����Ҫ��ȡҺ�����Ͳ����Һ�ܣ�����ʱ���Ӷ�������ʹ������Һ���������Ũ�ȼ�С��
��2�����������Mn�Ļ��ϼ۴ӣ�7�۽��ͣ�2�ۣ�˫��ˮ�е���Ԫ�ش�1�����ߵ�0�ۣ��������������������Ը��ݵ��ӵ�ʧ�غ��֪���������ͻ�ԭ�������ʵ���֮����2��5���ٸ��������غ�͵���غ�ɵû�ѧ����ʽ��2![]() ��5H2O2��6H+
��5H2O2��6H+![]() 2Mn2+��5O2����8H2O��
2Mn2+��5O2����8H2O��
��3�����������Һ���������ԣ��ܸ�ʴ������Ӧ������ʽ�ζ��ܡ��������Ը��������Һ�����Ϻ�ɫ�ģ������յ�������ǵ���һ�θ��������Һ����Һ��dz��ɫ����30���ڲ���ɫ��
��4�����ݻ�ѧ����ʽ���Եõ���ϵʽ��2![]() ~5H2O2������0.1 mol/L KMnO4����ҺV mL��������0.1V��103 mol�ĸ������ʱ������˫��ˮ�����ʵ�����0.25V��103 mol����ԭ�������������Ϊ��0.00025V mol��34 g/mol=0.0085V g������������Һ�й����������������Ϊ��
~5H2O2������0.1 mol/L KMnO4����ҺV mL��������0.1V��103 mol�ĸ������ʱ������˫��ˮ�����ʵ�����0.25V��103 mol����ԭ�������������Ϊ��0.00025V mol��34 g/mol=0.0085V g������������Һ�й����������������Ϊ��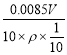 =
=![]() ��
��
��5�����ζ�ǰ�ζ��ܼ����������ݣ��ζ���������ʧ�������������Ը��������Һ���ƫ�����Բⶨ���ƫ�ߡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ��ұ�����ĵ�һ����Ӧԭ��Ϊ2SnO2 + 3C![]() 2Sn + aM��+ CO2��,������˵���д������(����)
2Sn + aM��+ CO2��,������˵���д������(����)
A. ��Ӧ��SnO2����ԭ B. a��ֵΪ3
C. ��Ӧ���������������� D. ÿ����1 mol CO2ת�Ƶ���8 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ת��Ϊ±������;���϶࣬�����ܵõ��ϴ�������ķ�����
A.��������������ȡ����ӦB.��ϩ�����������ӳɷ�Ӧ
C.��ϩ���Ȼ��ⷢ���ӳɷ�ӦD.��Ȳ���Ȼ��ⷢ���ӳɷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����17�֣��±���Ԫ�����ڱ���һ����, ��Ա��е��١�����Ԫ��,��д���пհ�(��д��Ų��÷�):
���� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0�� |
2 | �� | �� | �� | |||||
3 | �� | �� | �� | �� | �� | |||
4 | �� | �� |
��1������ЩԪ����,��ѧ��������õ���:_____������Ԫ�ط�����
��2��������������ˮ�����У�������ǿ�Ļ��������ѧʽ��/span>______��������ǿ�Ļ��������ѧʽ��:__________��
��3���ȽϢ���ݵ�����������Ӧ��ˮ���_________������ǿ������ѧʽ������ͨ��________________________________˵����д��Ӧ����ѧ����ʽ����
��4��ʵ������ȡ�ڵ��⻯�����ѧ����ʽ_______________________________ ���ڵ��⻯����ڵ�����������ˮ���ﷴӦ���õIJ�����ѧʽΪ______
��5���������γɶ������������һ���Ǻ���ɫ���壬���÷���ʽ˵�������岻�˲�����ˮ���ռ���ԭ��________________������ѧ����ʽ��ʾ��
��6���ȽϢ�����⻯�_________ ���ȶ�������ѧʽ��
��7��д���ܵĵ�����ˮ��Ӧ�����ӷ���ʽ_______________________��
��8��д����Ԫ�ص������ṹʾ��ͼ______,�����Ӱ뾶_________ S2-�������������д����Ԫ�������ڱ���λ��_______________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ԫ�صĻ�ѧ���ʹ�ϵ�����е���
A. ������ B. ������ C. ���������� D. ������Ӳ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���⻯����ҽҩ��������״���������μ�����̵�����������Ҳ����ʳƷ���Ӽ����й���ȡ� ��ҵ����NaOH��Һ��ˮ������ȡ�⻯�ƹ��壬���Ʊ�����ͼ���£�

��֪��N2H4��H2O��100�����Ϸֽ⡣
��1����֪���ںϳɹ��̵ķ�Ӧ�����к���NaIO3�����ںϳɹ�����������3 mol I2 �������� NaIO3�����ʵ���Ϊ mol��
��2��д����ԭ�����е����ӷ���ʽ ���ڻ�ԭ�����У�Ϊ�˼ӿ췴Ӧ���ɲ�ȡ����߷�Ӧ�¶ȣ����¶Ȳ��ó��� ������ѡ�������Լ�������õ⻯�ƹ������Ƿ���NaIO3���� (ѡ����ĸ)��
A.FeCl2��Һ B.������ C.KI��Һ D.������Һ
��3���ⶨ��Ʒ��NaI������ʵ�鲽�����£�
a.��ȡ4.000 g ��Ʒ���ܽ⣬��250 mL ����ƿ�ж��ݣ�
b.��ȡ25.00 mL ����Һ����ƿ�У�Ȼ�����������FeCl3��Һ����ַ�Ӧ���ټ���A��Һ��ָʾ����
c.�� 0.1000 mol��L 1 ��Na2S2O3��Һ���еζ����յ�(������Ӧ�ķ���ʽΪ��
2Na2S2O3 +I2![]() Na2S4O6 +2NaI)���ظ��ⶨ2�Σ����õ�����������±���
Na2S4O6 +2NaI)���ظ��ⶨ2�Σ����õ�����������±���
�ⶨ��� | ����Һ���/ mL | ��Һ�ζ���������/ mL | ��Һ�ζ����յ����/ mL |
1 | 25.00 | 0.06 | 24.04 |
2 | 25.00 | 0.02 | 24.02 |
3 | 25.00 | 0.12 | 24.14 |
������b�У�����������FeCl3��Һʱ�����������ӷ���ʽΪ ��
������A����Ϊ (������)���ζ��յ�۲쵽������Ϊ ��
���������Ʒ��NaI�ĺ���Ϊ ��(ֻд���о�����ֵ�ı���ʽ����)
��4���⻯�ƹ���ı��淽���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����÷�ѧ�ؼ��������˿ɿڵķ����������ķ����м⽷�����⡢���Ѽ������������ͳ���˺Ͱ���������˵����ȷ����(����)
A. ���⸻������ B. ������������
C. ����������ά�� D. ���Ѹ���ά����C
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����в����ڵ��Ĺ̶�����( )
A����ҵ�ϳɰ�
B�������죬�����еĵ���ת��Ϊ�ܱ�ֲ�����յ�������
C���ð����������Ƴɡ���李�����
D����������ĸ������������еĵ�ת��Ϊ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯��ͨ��һ����ѧ��Ӧʵ�ֵ���
A. Na2O2��Na B. Al2O3��Al(OH)3
C. SiO2��H2SiO3 D. Na2CO3��NaOH
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com