
【题目】屈昔多巴( )可治疗直立性低血压所致头昏、头晕和乏力,帕金森病患者的步态僵直等。以下是屈昔多巴的一种合成路线(通常
)可治疗直立性低血压所致头昏、头晕和乏力,帕金森病患者的步态僵直等。以下是屈昔多巴的一种合成路线(通常![]() 简写为BnCl,
简写为BnCl,![]() 简写为CbzCl ):
简写为CbzCl ):

回答下列问题:
(1)反应①的反应类型为_____________,其作用为_________________。
(2)屈昔多巴中所含的非含氧官能团名称为_______________,屈昔多巴分子中有___________个手性碳原子。
(3)反应②为加成反应,有机物X的名称为______________________。
(4)![]() 显________________性(填“酸”、“中”或“碱”),写出其与盐酸反应的化学方程式:_______________________。
显________________性(填“酸”、“中”或“碱”),写出其与盐酸反应的化学方程式:_______________________。
(5)![]() 的同分异构体中,能与NaHCO3溶液反应生成CO2的二取代芳香化合物有_______种,其中核磁共振氢谱为四组峰的结构简式为______________(任写一种)。
的同分异构体中,能与NaHCO3溶液反应生成CO2的二取代芳香化合物有_______种,其中核磁共振氢谱为四组峰的结构简式为______________(任写一种)。
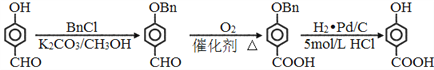
(6)参照上述合成路线,以对羟基苯甲醛为原料(无机试剂任选),设计制备对羟基苯甲酸的合成路线:______________________。
【答案】 取代反应 保护羟基 氨基 2 氨基乙酸(或“甘氨酸”) 碱 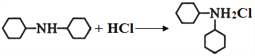 6
6 ![]()
【解析】(1)反应①为酚羟基上的氢原子被Bn取代。由于酚羟基易被氧化,所以其作用为保护酚羟基。(2)根据屈昔多巴的结构简式可判断其中所含的非含氧官能团名称为氨基,屈昔多巴分子中有2个手性碳原子,即与醇羟基和氨基相连的碳原子。(3)反应②为加成反应,根据原子守恒和生成物结构简式可判断有机物X的名称为氨基乙酸;(4)![]() 中含有氨基,显碱性,与盐酸反应的化学方程式为
中含有氨基,显碱性,与盐酸反应的化学方程式为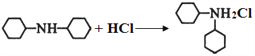 。(5)
。(5)![]() 的同分异构体中,能与NaHCO3溶液反应生成CO2,说明含有羧基,其苯环上的两个取代基可以是-COOH和CH2Cl或-CH2COOH和-Cl,均有邻间对三种,即二取代芳香化合物有6种,其中核磁共振氢谱为四组峰的结构简式为
的同分异构体中,能与NaHCO3溶液反应生成CO2,说明含有羧基,其苯环上的两个取代基可以是-COOH和CH2Cl或-CH2COOH和-Cl,均有邻间对三种,即二取代芳香化合物有6种,其中核磁共振氢谱为四组峰的结构简式为![]() 。(6)参照上述合成路线可知以对羟基苯甲醛为原料制备对羟基苯甲酸时首先要保护酚羟基,则其合成路线为
。(6)参照上述合成路线可知以对羟基苯甲醛为原料制备对羟基苯甲酸时首先要保护酚羟基,则其合成路线为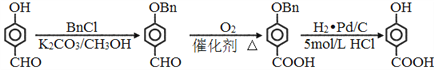 。
。


 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案科目:高中化学 来源: 题型:
【题目】传统的制备合成氨原料气H2的方法是水煤气法。已知:
①C(s)+H2O(g)=CO(g)+H2(g) △H1=﹢131.3kJ·mol-1
②C(s)+2H2O(g)=CO2(g)+2H2(g) △H2=﹢90.2kJ·mol-1
③CO(g)+H2O(g)=CO2(g)+H2(g) △H3
(1)反应①△H1>0,在一定条件下,能自发进行的原因是_______________;△H3=__________kJ·mol-1。
(2)已知800℃时:CO(g)+H2O(g)![]() CO2(g)+H2(g) K=1.0。在此温度下向一2L的恒温恒容密闭容器中充入2molH2O(g)和2molCO,2min后达到平衡,则平衡时CO2的物质的量浓度为_______________;从反应开始至达到平衡时H2O的平均反应速率为_______________。
CO2(g)+H2(g) K=1.0。在此温度下向一2L的恒温恒容密闭容器中充入2molH2O(g)和2molCO,2min后达到平衡,则平衡时CO2的物质的量浓度为_______________;从反应开始至达到平衡时H2O的平均反应速率为_______________。
(3)900℃时,反应:CO(g)+H2O(g) ![]() CO2(g)+H2(g)的平衡常数K__________1.0(填“>”“<”或“=”)。
CO2(g)+H2(g)的平衡常数K__________1.0(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,密闭容器中进行反应:2SO2(g)+O2(g)![]() 2SO3(g) △H<0。测得v正(SO2)随反应时间(t)的变化如图所示。下列有关说法正确的是( )
2SO3(g) △H<0。测得v正(SO2)随反应时间(t)的变化如图所示。下列有关说法正确的是( )

A. t2时改变的条件是:只加入一定量的SO2
B. 在t1时平衡常数K1大于t3时平衡常数K2
C. t1时平衡混合气的![]() 大于t3时平衡混合气的
大于t3时平衡混合气的![]()
D. t1时平衡混合气中SO3的体积分数等于t3时平衡混合气中SO3的体积分数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y均为元素周期表中前20号元素,其简单离子的电子层结构相同,下列说法正确的是( )
A. 由![]() 与
与![]() 得,m+b=n+a
得,m+b=n+a
B. ![]() 的还原性一定大于
的还原性一定大于![]()
C. X、Y一定是同周期元素
D. 若X的原子半径大于Y,则X的氢化物稳定性一定大于Y的氢化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是重要的化学工业基础原料和液体燃料。工业上可利用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
化学反应 | 平衡常数 | 温度(℃) | |
500 | 800 | ||
①2H2(g)+CO(g) | K1 | 2.5 | 0.15 |
②H2(g)+CO2(g) | K2 | 1.0 | 2.50 |
③3H2(g)+ CO2(g) | K3 | ||
(1)反应②是 (填“吸热”或“放热”)反应。

(2)某温度下反应①中H2的平衡转化率(a)与体系总压强(P)的关系如图所示。则平衡状态由A变到B时,平衡常数K(A) K(B)(填“>”、“<”或“=”)。
(3)500℃ K3= ;反应③△H 0(填“>”“=”或“<”)
在500℃、2L的密闭容器中,进行反应③,测得某时刻H2、CO2、CH3OH、H2O的物质的量分别为6mol、2 mol、10 mol、10 mol,此时v(正) v(逆)(填“>”“=”或“<”)

(4)一定温度下,在3 L容积可变的密闭容器中发生反应②,已知c(CO)与反应时间t变化曲线Ⅰ如图所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ。当曲线Ⅰ变为曲线Ⅱ时,改变的条件是 。当曲线Ⅰ变为曲线Ⅲspan>时,改变的条件是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增大,分别可以形成简单离子W2-、X+、Y3+、Z2-,下列判断错误的是
A. W 和 Z 在同一主族
B. Y3+、 Z2-两种离子都能促进水的电离
C. X 元素的单质能跟水剧烈反应
D. W 元素能形成两种氢化物,分子中含有类型完全相同的化学键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将过氧化钠加入到氯化亚铁溶液中,最终可以观察到的现象是( )
A. 过氧化钠将溶液漂白 B. 生成红褐色沉淀
C. 除溶解外无特殊现象产生 D. 生成白色沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com