
����Ŀ����ͳ���Ʊ��ϳɰ�ԭ����H2�ķ�����ˮú��������֪��
��C(s)+H2O(g)=CO(g)+H2(g) ��H1=��131.3kJ��mol��1
��C(s)+2H2O(g)=CO2(g)+2H2(g) ��H2=��90.2kJ��mol��1
��CO(g)+H2O(g)=CO2(g)+H2��g�� ��H3
��1����Ӧ�١�H1��0����һ�������£����Է����е�ԭ����_______________����H3=__________kJ��mol��1��
��2����֪800��ʱ��CO(g)+H2O(g)![]() CO2(g)+H2��g�� K=1.0���ڴ��¶�����һ2L�ĺ��º����ܱ������г���2molH2O(g)��2molCO,2min��ﵽƽ�⣬��ƽ��ʱCO2�����ʵ���Ũ��Ϊ_______________���ӷ�Ӧ��ʼ���ﵽƽ��ʱH2O��ƽ����Ӧ����Ϊ_______________��
CO2(g)+H2��g�� K=1.0���ڴ��¶�����һ2L�ĺ��º����ܱ������г���2molH2O(g)��2molCO,2min��ﵽƽ�⣬��ƽ��ʱCO2�����ʵ���Ũ��Ϊ_______________���ӷ�Ӧ��ʼ���ﵽƽ��ʱH2O��ƽ����Ӧ����Ϊ_______________��
��3��900��ʱ����Ӧ��CO(g)+H2O(g) ![]() CO2(g)+H2(g)��ƽ�ⳣ��K__________1.0���������������������
CO2(g)+H2(g)��ƽ�ⳣ��K__________1.0���������������������
���𰸡� ��S��0 �������� ����ϵ���Ҷ����� -41.1 0.5 mol��L��1 0.25 mol��L��1��min��1 ����λд�������֣� ��
��������(1)�Է����е���������H-T��S��0����Ӧ��C(s)+H20(g)=CO(g)+H2(g)��H=+131.3kJ/mol�����ȷ�Ӧ����H��0����S��0�����Է�Ӧ�Է������Ǹ����½��еķ�Ӧ�����ݸ�˹���ɣ���-���õ�������H3=(��90.2kJ��mol��1)-(��131.3kJ��mol��1)=-41.1KJ/mol��
(2)���ݻ�ѧƽ������ʽ��ʽ���跴Ӧ�ﵽƽ������ˮ�����ʵ���Ϊx
CO(g)+H2O(g)C02(g)+H2(g)
��ʼ��(mol) 22 0 0
�仯��(mol) x x xx
ƽ����(mol) 2-x2-x x x
K=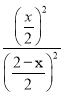 =1������õ�x=1��ƽ��ʱCO2�����ʵ���Ũ��Ϊ
=1������õ�x=1��ƽ��ʱCO2�����ʵ���Ũ��Ϊ![]() =0.5mol/L���ӷ�Ӧ��ʼ���ﵽƽ��ʱH2O��ƽ����Ӧ����Ϊ
=0.5mol/L���ӷ�Ӧ��ʼ���ﵽƽ��ʱH2O��ƽ����Ӧ����Ϊ![]() =0.25 mol��L��1��min��1 ��
=0.25 mol��L��1��min��1 ��
(3)900��ʱ��������ɷ�Ӧ��֪��Ӧ�Ƿ��ȷ�Ӧ������ƽ��������У���ӦCO(g)+H2O(g)C02(g)+H2(g)��ƽ�ⳣ����С��K��1.0��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ѧ������Ф���2005��ŵ������ѧ������������ϩ�����̼��̼˫���ᱻ��ɢ�����飬�γ��·��ӣ����ֹ��̱�����Ϊϩ�����ֽⷴӦ ��ϩ�����ֽⷴӦ�����������Ϊ������顣(��ͼ��ʾ)
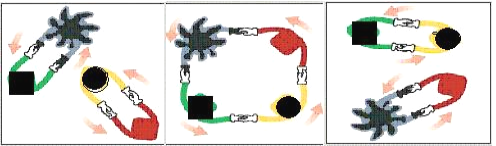
ϩ�����ֽⷴӦ�еĴ����ǽ�������(��CH2==M)������������ϩ����������������������ʱ������������������������赸��������ǡ�������顱����ϳ������·��ӣ�����һ�����µ�ϩ�����ӣ���һ���ǽ���ԭ�Ӻ���������顣�������Ѱ����һ��ϩ�����ӣ��ٴΡ�������顱����C6H5CH2CH==CH2��CH2==M��һ�������»�Ϸ�Ӧ�����в��ﲻ���ܴ��ڵ���
A. C6H5CH2 CH2 C6H5 B. CH2= CH2
C. C6H5CH2CH==M D. C6H5CH2CH==CH CH2 C6H5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2NO2![]() N2O4�Ŀ��淴Ӧ�У�����״̬һ������ƽ��״̬���ǣ� ��
N2O4�Ŀ��淴Ӧ�У�����״̬һ������ƽ��״̬���ǣ� ��
A. N2O4��NO2�ķ�������Ϊ1��2
B. N2O4��NO2��Ũ�����
C. ��ϵ����ɫ���ٸı�
D. ��λʱ������1molN2O4ת��ΪNO2��ͬʱ����2molNO2ת��ΪN2O4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)��![]() �й���______��Ԫ�أ�_______�ֺ��أ���Ϊͬλ�ص���_______,������������_______��
�й���______��Ԫ�أ�_______�ֺ��أ���Ϊͬλ�ص���_______,������������_______��
(2)Ԫ�����ڱ�����_____�����ڡ�
(3)����õĽ���Ԫ��λ�����ڱ��еĵ�______�壬����õķǽ���Ԫ��λ�����ڱ��еĵ�_____�塣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ�ˮ��Һ�ܵ��磬�����ڷǵ���ʵ��ǣ�������
A. HCl B. Cl2 C. NaHCO3 D. CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯���̣���Fe(OH)3����������� �ڵ����ʼ������� ��ú���� ��ú���ͷ��� ��������Ӧ����NaCl ��N2O4��NO2���Ȼ��������ȴ�����в�����ѧ�仯����
A. �٢ۢ�B. �ڢܢ�C. �٢�D. �٢ܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ǻ��������һ����Ҫ�����Ϻ��л��ϳɵ��м��壬�ڹ�ũҵ������ҽҩ�ȷ����ж�����;����ṹ��ʽ��ͼ��ʾ������˵���������

A�����ǻ������ķ���ʽΪC9H8O3
B�����ǻ�������ܷ���������ȡ������ȥ���ۺϵȷ�Ӧ
C��1mol���ǻ������������Na��Ӧ���ų�1mol H2
D������ǻ�����������ͬ�����ŵ�ͬ���칹�廹��15�֣��������ǻ���̼̼˫��ֱ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ� ��
�����ӻ�����һ����ǿ����ʣ����ۻ�����һ�����������
�ڵ����һ�������ӻ�����ǵ����һ���ǹ��ۻ�����
�۷ǽ���������һ���ǹ��ۻ�����⻯��һ���ǹ��ۻ�����
�����ӻ�����������״̬��һ�����磬���ۻ�����������״̬��һ��������
A. �٢�B. �ڢ�C. �ۢ�D. ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������( )������ֱ���Ե�Ѫѹ����ͷ�衢ͷ�κͷ���������ɭ�����ߵIJ�̬��ֱ�ȡ�������������͵�һ�ֺϳ�·��(ͨ��
)������ֱ���Ե�Ѫѹ����ͷ�衢ͷ�κͷ���������ɭ�����ߵIJ�̬��ֱ�ȡ�������������͵�һ�ֺϳ�·��(ͨ��![]() ��дΪBnCl��
��дΪBnCl��![]() ��дΪCbzCl )��
��дΪCbzCl )��

�ش��������⣺
(1)��Ӧ�ٵķ�Ӧ����Ϊ_____________��������Ϊ_________________��
(2)��������������ķǺ�������������Ϊ_______________��������ͷ�������___________������̼ԭ�ӡ�
(3)��Ӧ��Ϊ�ӳɷ�Ӧ���л���X������Ϊ______________________��
(4)![]() ��________________�ԣ���ᡱ�����С������д���������ᷴӦ�Ļ�ѧ����ʽ��_______________________��
��________________�ԣ���ᡱ�����С������д���������ᷴӦ�Ļ�ѧ����ʽ��_______________________��
(5)![]() ��ͬ���칹���У�����NaHCO3��Һ��Ӧ����CO2�Ķ�ȡ�����㻯������_______�֣����к˴Ź�������Ϊ�����Ľṹ��ʽΪ______________(��дһ��)��
��ͬ���칹���У�����NaHCO3��Һ��Ӧ����CO2�Ķ�ȡ�����㻯������_______�֣����к˴Ź�������Ϊ�����Ľṹ��ʽΪ______________(��дһ��)��
(6)���������ϳ�·�ߣ��Զ��ǻ�����ȩΪԭ��(���Լ���ѡ)������Ʊ����ǻ�������ĺϳ�·�ߣ�______________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com