
【题目】(1)用双线桥法表示出下列反应的电子转移方向和数目。
①3S+6KOH![]() K2SO3+2K2S+3H2O__________________________
K2SO3+2K2S+3H2O__________________________
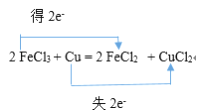
②2FeCl3+Cu=2FeCl2+CuCl2________________________________
(2)现用如图所示的装置制取饱和氯水,请回答有关问题:

①写出装置甲中发生反应的化学方程式:_________________________。
②装置乙的作用是:______________________。
③若丁装置中为NaOH与酚酞的混合溶液,将氯气通入丁装置中,溶液红色褪去,则推测可能的原因是:
a.________________________________________;
b.________________________________________。
【答案】 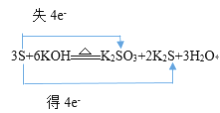
 4HCl(浓) + MnO2
4HCl(浓) + MnO2 ![]() MnCl2 + Cl2↑+ 2H2O 除去氯气中混有的氯化氢气体杂质 氯气与NaOH反应,将NaOH反应了,溶液褪色 HClO的漂白性,使溶液褪色
MnCl2 + Cl2↑+ 2H2O 除去氯气中混有的氯化氢气体杂质 氯气与NaOH反应,将NaOH反应了,溶液褪色 HClO的漂白性,使溶液褪色
【解析】试题分析:(1) ①3S+6KOH![]() K2SO3+2K2S+3H2O的反应中,硫原子化合价由0变为+4,硫原子化合价由0变为-2,化合价升降的最小公倍数是4,所以转移电子数是4;②2FeCl3+Cu=2FeCl2+CuCl2的反应中,铜元素失去2个电子,铁元素得到2个电子;
K2SO3+2K2S+3H2O的反应中,硫原子化合价由0变为+4,硫原子化合价由0变为-2,化合价升降的最小公倍数是4,所以转移电子数是4;②2FeCl3+Cu=2FeCl2+CuCl2的反应中,铜元素失去2个电子,铁元素得到2个电子;
(2)①甲中二氧化锰与浓盐酸反应生成氯气、氯化锰、水;
②甲中生成的氯气含有杂质氯化氢。
③NaOH与酚酞的混合溶液呈红色,将氯气通入丁装置中,氯气消耗氢氧化钠,氯气与水反应的产物次氯酸具有漂白作用。
解析:(1) ①3S+6KOH![]() K2SO3+2K2S+3H2O的反应中,硫原子化合价由0变为+4,硫原子化合价由0变为-2,化合价升降的最小公倍数是4,所以转移电子数是4,用双线桥表示出反应的电子转移方向和数目是
K2SO3+2K2S+3H2O的反应中,硫原子化合价由0变为+4,硫原子化合价由0变为-2,化合价升降的最小公倍数是4,所以转移电子数是4,用双线桥表示出反应的电子转移方向和数目是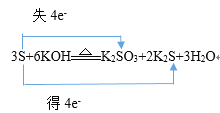 ;②2FeCl3+Cu=2FeCl2+CuCl2的反应中,铜元素失去2个电子,铁元素得到2个电子,用双线桥表示出反应的电子转移方向和数目是
;②2FeCl3+Cu=2FeCl2+CuCl2的反应中,铜元素失去2个电子,铁元素得到2个电子,用双线桥表示出反应的电子转移方向和数目是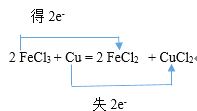 ;
;
(2)①甲中二氧化锰与浓盐酸反应生成氯气、氯化锰、水,反应方程式是4HCl(浓) + MnO2 ![]() MnCl2 + Cl2↑+ 2H2O;
MnCl2 + Cl2↑+ 2H2O;
②甲中生成的氯气含有杂质氯化氢,饱和食盐水的作用是除去氯气中的氯化氢。
③NaOH与酚酞的混合溶液呈红色,将氯气通入丁装置中,氯气消耗氢氧化钠,氯气与水反应的产物次氯酸具有漂白作用。所以溶液红色褪去的可能原因是a.氯气与NaOH反应,将NaOH反应了,溶液褪色;b. HClO的漂白性,使溶液褪色。


 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:
【题目】煤炭可以转化为清洁能源和化工原料.
(1)用煤可以制得水煤气.工业上可用煤和水通过水煤气法制氢气,已知下列热化学方程式:
C(s)+![]() O2(g)═CO(g)△H1=-110.5kJmol-1
O2(g)═CO(g)△H1=-110.5kJmol-1
2H2(g)+O2(g)═2H2O(g)△H2=-483.6kJmol-1
试求水煤气法制氢气的反应的反应热△H3.
C(s)+H2O(g)═CO(g)+H2(g)△H3= ______ kJmol-1
(2)若H-H、O=O和O-H键的键能分别是436kJmol-1、496kJmol-1和mkJmol-1,结合上述热化学方程式的相关数据计算,m= ______ .
(3)已知一氧化碳与水蒸气反应过程的能量变化如图所示:

则此反应为 ______ (填“吸热”或“放热”)反应,反应的热化学方程式为 ______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔性碳棒)持续通入甲烷,在标准状况下,消耗甲烷体积VL。则下列说法正确的是( )

A.OH-由A端移向B端
B.0<V≤22.4L时,电池总反应的化学方程式为:CH4 + 2O2 + KOH = KHCO3 + 2H2O
C.22.4L<V≤44.8L时,负极电极反应为:CH4 - 8e- + 9CO32- + 3H2O = 10HCO3-
D.V=33.6L时,溶液中阴离子浓度大小关系为:c(CO32- )>c(HCO3- )>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用KMnO4氧化密度为1.19g/mL、质量分数为36.5%的盐酸。反应的化学方程式如下:2KMnO4+16HCl==2KCl+2MnCl2+5Cl2↑+8H2O,请回答下列问题:
(1)求该盐酸的物质的量浓度。
(2)耗15.8 g KMnO4时,有多少摩尔HCl被氧化?
(3)耗15.8 g KMnO4时,产生的Cl2在标准状况下的体积为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2H2(g)+O2(g)![]() 2H2O(l) ΔH=571.6 kJ·mol1,CO(g)+
2H2O(l) ΔH=571.6 kJ·mol1,CO(g)+![]() O2(g)
O2(g)![]() CO2(g) ΔH=282.8 kJ·mol1,现有CO、H2和CO2组成的混合气体112.0 L(标准状况),经完全燃烧后放出的总热量为851.4 kJ,并生成18 g液态水。则燃烧前混合气体中CO的体积分数为
CO2(g) ΔH=282.8 kJ·mol1,现有CO、H2和CO2组成的混合气体112.0 L(标准状况),经完全燃烧后放出的总热量为851.4 kJ,并生成18 g液态水。则燃烧前混合气体中CO的体积分数为
A.80% B.40% C.60% D.20%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学反应速率的说法中正确的是( )
A.决定化学反应速率的主要因素是温度
B.反应速率用于衡量化学反应进行快慢
C.可逆反应达到平衡状态时正逆反应的速率都为0
D.增大反应物的量或提高反应温度一定能增大反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用铁片与稀硫酸反应制取氢气,下列措施能使氢气生成速率明显加快的是( )
A. 加入适量的蒸馏水 B. 改用质量分数为98%的浓硫酸
C. 将稀硫酸改用稀硝酸 D. 适当增加稀硫酸的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaClO2广泛用于造纸工业、污水处理等,其漂白能力是漂白粉的4~5倍,工业上用C1O2气体制NaClO2的工艺流程如下:

己知:NaClO2饱和溶液在低于38℃时析出NaC1O2·3H2O,高于38℃时析出NaClO2
下列说法不正确的是
A. 吸收器中生成NaClO2的离子方程式:2ClO2+2OH-+H2O2=2ClO2-+O2+2H2O
B. 流程中的结晶、过滤操作应该是蒸发结晶、趁热过滤
C. 提高吸收器中的反应温度可以提高反应速率,也提高反应物的利用率
D. 发生器中反应结束后,向其中通入一定量空气的目的是驱赶出ClO2,使其被充分吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼及其化合物在工业上有许多用途。以铁硼矿(主要成分为Mg2B2O5·H2O和Fe3O4,还有少量Fe2O3、FeO、CaO、Al2O3和SiO2等)为原料制备硼酸(H3BO3)的工艺流程如图所示:

回答下列问题:
(1)写出Mg2B2O5·H2O与硫酸反应的化学方程式__________________。
(2)利用____(写化学式,下同)的磁性,可将其从“浸渣”中分离。“浸渣”中还剩余的物质是__________________。
(3)“净化除杂”需先加H2O2溶液,作用是__________________。
(4)单质硼可用于生成具有优良抗冲击性能硼钢。以硼酸和金属镁为原料可制备单质硼,用化学方程式表示制备过程__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com