
【题目】下列操作不能用于检验NH3的是
A.气体使湿润的酚酞试纸变红 B.气体能使湿润的红色石蕊试纸变蓝
C.气体与蘸有浓H2SO4的玻璃棒靠近 D.气体与蘸有浓盐酸的玻璃棒靠近
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述不相符的是( )
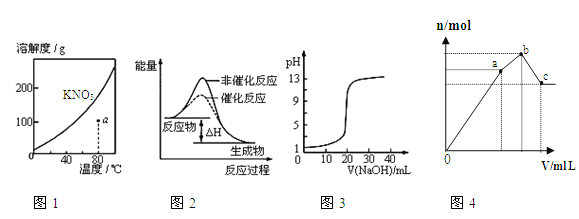
A.图1表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液
B.图2表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化
C.图3表示0.1000molL-1NaOH溶液滴定20.00mL0.1000molL-1醋酸溶液得到滴定曲线
D.图4 表示向NH4Al(SO4)2溶液中逐滴滴入Ba(OH)2溶液,随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应原理在科研和生产中有广泛应用。
(1)已知:3Fe2O3(s)+CO(g)=2Fe3O4(s)+4CO2(g) △H1=-47kJ/mol;
Fe3O4(s)+4CO(g)=3Fe(s)+4CO2(g) △H2=-14kJ/mol。
则Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H=________。
(2)煤化工行业中常常通过研究不同温度下反应的平衡常数来解决各种实际问题。将等体积的CO和H2O(g)通入一恒容密闭容器中,发生反应:CO(g)+H2O(g)![]() H2(g)+CO2(g),该反应的平衡常数随温度的变化如下表所示。
H2(g)+CO2(g),该反应的平衡常数随温度的变化如下表所示。
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | 1 |
① 该反应的平衡常数表达式K=_______,该反应的正反应是_______(填“吸热”或“放热”)反应。
② 若反应在800℃时进行, CO和H2O(g)的起始浓度均为0.020 mol·L-1,则该条件下,CO的平衡转化率为_________。
③ 下列措施中能够提高CO转化率的是______(填字母)
a.降低温度 b.加入催化剂 c.增加CO的浓度 d.加入H2O(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】120℃时,2体积某烃和8体积O2混合,完全燃烧后恢复到原来的温度和压强,体积不变,该分子式中所含的碳原子数不可能是( )
A. 1 B. 2 C. 3 D. 5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欧盟征收航空碳排税以应对冰川融化和全球变暖,使得对如何降低大气中CO2的含量及有效地开发利用碳资源的研究显得更加紧迫。请运用化学反应原理的相关知识研究碳及其化合物的性质。
(1)近年来,我国储氢碳纳米管研究取得重大进展,用电弧法合成的碳纳米管中常伴有大量碳纳米颗粒(杂质),这种碳纳米颗粒可用氧化气化法提纯,请完成并配平下述化学方程式:
口C+口K2Cr2O7+口______=口CO2↑+口K2SO4+口Cr2(SO4)3+口H2O
(2)甲醇是一种新型燃料,甲醇燃料电池即将从实验室走向工业化生产。工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2(g)=CH3OH(g) △H1=-116kJ/mol
①下列措施中有利于增大该反应的反应速率的是_______(填字母代号)。
A.随时将CH30H与反应混合物分离 B.降低反应温度
C.增大体系压强 D.使用高效催化剂
②已知:CO(g)+1/2O2(g)=CO2(g) △H2=-283kJ/mol
H2(g)+1/2O2(g)=H2O(g) △H3=-242kJ/mol
则表示lmol气态甲醇完全燃烧生成CO2和水蒸气时的热化学方程式为______________。
③在容积为1L的恒容容器中,分别研究在230℃、250℃和270℃ 三种温度下合成甲醇的规律。右图是上述三种温度下不同的H2和CO的起始组成比(起始时CO的物质的量均为lmol)与CO平衡转化率的关系。

请回答:
i)在上述三种温度中,曲线Z对应的温度是_________;
ii)利用图中a点对应的数据,计算出曲线Z在对应温度下,反应CO(g)+2H2(g)=CH3OH(g)的平衡常数K=__________。
(3)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9。 CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为5.6×10-5mol/L,则生成沉淀所需CaCl2溶液的最小浓度为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,直线交点处的圆圈为NaCl晶体中Na+离子或Cl-离子所处的位置。
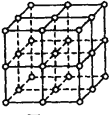
这两种离子在空间三个互相垂直的方向上都是等距离排列的。
(1)请将其中代表Na+离子的圆圈涂黑(不必考虑体积大小),以完成NaCl晶体的结构示意图。_______
(2)晶体中,在每个Na+离子的周围与它最接近的且距离相等的Na+离子共有_____个。
(3)晶体中每一个重复的结构单元叫晶胞。在NaCl晶胞中正六面体的顶点上、面上、棱上的Na+或Cl-离子为该晶胞与其相邻的晶胞所共有。一个晶胞中,Cl-离子的个数等于______,即______(填计算式),Na+离子的个数等于_______,即__________(填计算式)。
(4)设NaCl的摩尔质量为M g/mol,食盐晶体的密度为![]() g/cm3,阿伏加德罗常数为NA。食盐晶体中两个距离最近的钠离子中心间的距离为______cm。
g/cm3,阿伏加德罗常数为NA。食盐晶体中两个距离最近的钠离子中心间的距离为______cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用0.1 mol·L-1NaOH溶液分别滴定10mL相同浓度的盐酸和醋酸(溶质用HA表示),利用电导率传感器绘制电导率曲线如图所示。下列说法不正确的是( )

A. b点pH值大于1 B. 盐酸浓度为 0.lmol·L-1
C. c点:c(Na+)>c(A-)>c(H+)>c(OH-) D. 曲线Ⅰ为盐酸,曲线Ⅱ为醋酸溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将W1g光亮铜丝在空气中加热一段时间后,迅速插入下列物质中,取出干燥,如此反复几次,最后取出铜丝,洗涤、干燥后称其质量为W2g。下列所插入的物质与铜丝质量关系不正确的是( )
A. 石灰水Wl<W2 B. COW1=W2 C. 稀H2SO4溶液W1>W2 D. 乙醇W1<W2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com