
����Ŀ����ͼ��ֱ�߽��㴦��ԲȦΪNaCl������Na+���ӻ�Cl-����������λ�á�
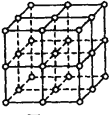
�����������ڿռ��������ഹֱ�ķ����϶��ǵȾ������еġ�
��1���뽫���д���Na+���ӵ�ԲȦͿ�ڣ����ؿ��������С���������NaCl����Ľṹʾ��ͼ��_______
��2�������У���ÿ��Na+���ӵ���Χ������ӽ����Ҿ�����ȵ�Na+���ӹ���_____����
��3��������ÿһ���ظ��Ľṹ��Ԫ�о�������NaCl��������������Ķ����ϡ����ϡ����ϵ�Na+��Cl-����Ϊ�þ����������ڵľ��������С�һ�������У�Cl-���ӵĸ�������______����______�������ʽ����Na+���ӵĸ�������_______����__________�������ʽ����
��4����NaCl��Ħ������ΪM g/mol��ʳ�ξ�����ܶ�Ϊ![]() g/cm3�������ӵ�����ΪNA��ʳ�ξ���������������������������ļ�ľ���Ϊ______cm��
g/cm3�������ӵ�����ΪNA��ʳ�ξ���������������������������ļ�ľ���Ϊ______cm��
���𰸡� 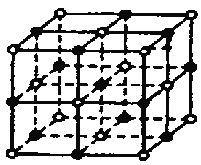 12 4 Cl-����=8��
12 4 Cl-����=8��![]() +6��
+6��![]() =4 4 Na+����=12��
=4 4 Na+����=12��![]() +1=4 d=
+1=4 d=![]()
��������(1)�Ȼ��ƾ����У������ӻ������ӵ���λ������6���Ȼ��ƾ���Ľṹʾ��ͼΪ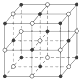 ��
��
(2)��NaCl�����У�Na+��Cl-������λ���Ƕ������ĺ���ߵ��е㣬�����ӡ������ӵ���λ������6��������Na+��ӽ����Ҿ�����ȵ�Na+����12����
(3)���ݾ�̯�����ٴ��ڶ�������ӣ�ͬʱΪ8���������У�ÿ��������1/8���ھ������ڴ������ϵ����ӣ�ͬʱΪ4���������У�ÿ��������1/4���ھ������۴������ϵ����ӣ�ͬʱΪ2���������У�ÿ��������1/2���ھ������ܴ��ھ����ڲ�(����)�����ӣ�����ȫ���ڸþ������ɴ˿�֪����NaCl�����У���Cl-��12��![]() +1=4������Na+��8��
+1=4������Na+��8��![]() +6��
+6��![]() =4����
=4����
(4)�辧���߳�Ϊa����NaCl�����У���Cl-4������Na4���������ܶȹ�ʽ�ѣ�![]() ���ɵ�a=
���ɵ�a=![]() �����Ծ�����Խ��߳�Ϊ
�����Ծ�����Խ��߳�Ϊ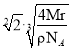 ��������������������������ļ�ľ�����ھ�����Խ��ߵ�һ�룬��������������������������ļ�ľ���Ϊ
��������������������������ļ�ľ�����ھ�����Խ��ߵ�һ�룬��������������������������ļ�ľ���Ϊ =
=![]() cm��
cm��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪ��Ȫˮƿ�ϵIJ���˵�����֣��г���������Ȼˮ����ָ�꣬����ĸơ��ء�����ָ
A��ԭ�� B������ C������ D��Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������[CO(NH2)2]��һ���ܺĺܵ͵����ⷽ�����乤��ԭ����ͼ��ʾ���ܷ�ӦΪCO(NH2)2+2OH-![]() N2��+3H2��+CO32-������˵���������
N2��+3H2��+CO32-������˵���������

A. �����IJ��Ͽ�ѡ�������Ʒ
B. ���ع���ʱ������������Һ��pH��С
C. �����ĵ缫��ӦʽΪCO(NH2)2+8OH--6e-==N2��+ CO32-+6H2O��
D. ����·��ͨ��3 mol ���ӣ�����������������Ϊ33. 6L(��״��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����в����������ڼ���NH3����
A������ʹʪ��ķ�̪��ֽ��� B��������ʹʪ��ĺ�ɫʯ����ֽ����
C��������պ��ŨH2SO4�IJ��������� D��������պ��Ũ����IJ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ç������һ�ֺϳ�ҩ���Ƶ�ԭ�ϣ����������ƻ������ʯ���ֲ���С����й����������л��������˵����ȷ����
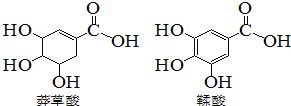
A. ç�������ʽΪC7H10O5
B. �����ᶼ������ˮ�����ӳɷ�Ӧ
C. ���������ç������ӻ�Ϊͬϵ��
D. �����ʵ������������������������Ʒ�Ӧ�������������Ƶ����ʵ�����ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����
A���ϸ�ִ�л�����β���ŷű������ڷ�ֹ������Ⱦ
B��ʹ�ö�����������ʳƷ�����彡��������
C��ʹ������������ˮ����ʱ���ɵ��л��Ȼ�����ܶ������к�
D��ʳƷ�������ĺ��ḻ������Ӫ���صķ�ˮ�ɳ�������ˮ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E����Ԫ�ص�ԭ��������������Aԭ�������ӣ�B�ĵ����ڿ����к�����࣬C��DԪ��ͬ������ԭ������DΪC�Ķ�����EԪ�صļ۵����Ų�ʽΪ(n-l)dn+6ns1���ش��������⣺
��1��Ԫ��B�����ڱ��е�λ���� ��EԪ�ص�Ԫ�ط���Ϊ �������γ�E+��ԭ��Ϊ ��
��2��DԪ�ػ�̬ԭ�ӵĺ�����ӹ���Ų�ͼΪ![]() ��
��
��3��AԪ����CԪ���γ����ֳ����Ļ������ԭ�Ӹ����ȷֱ�Ϊ2��1��1��1�����ֻ������������Ȼ��ܣ�ԭ���� ������һ�ֻ�����������������½�KMnO4��ԭΪMn2+����ط�Ӧ�����ӷ���ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ʋ����Ĺ�ҵ��ˮ���е��ؽ������ӣ�Cu2+��Ni2+�ȣ���CN�γ����Գ�ȥ�������õ�ⷨ�Ʊ��������ƣ�Na2FeO4)������ˮ��Ŀǰ�Ƚ��Ƚ��ķ�������֪�軯���ж��ӷ������װ����ͼ��ʾ������ѡ����ȷ���ǣ� ��
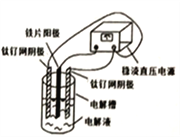
A. ��Ƭ���ӵ�Դ�ĸ���
B. ���ʱ��ÿ����lmolFeO42-��ת�Ƶ���3mol
C. CN��������CO2��N2��Cu2+��Ni2+�γ����ܼ����ȥ
D. ��֪HFeO4-�������Ա�FeO42-��ǿ����pH<7ʱ������ˮЧ�ʸ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ����һ���������ォ��ˮ�е�����(H2NCONH2����Ԫ����-3��)�Ļ�ѧ��ֱ��ת��Ϊ���ܣ������ɶԻ��������ʵ�װ�ã�ͬʱ���ô�װ�õĵ��������϶�ͭ������˵���в���ȷ����( )
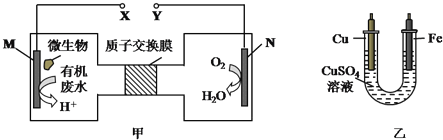
A��H+�����ӽ���Ĥ���������ƶ�
B��ͭ�缫Ӧ��Y������
C��M�缫��Ӧʽ��H2NCONH2+H2O-6e-�TCO2��+N2��+6H+
D����N�缫����0.25mol����ʱ�������缫����16g
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com