
把下列四种X溶液分别加入四个盛有10 mL 2 mol·L-1盐酸的烧杯中,均加水稀释到50 mL,此时,X和盐酸发生反应,其中反应速率最快的是( )
A.10℃ 20 mL 3 mol·L-1的X溶液
B.20℃ 30 mL 2 mol·L-1的X溶液
C.20℃ 10 mL4 mol·L-1的X溶液
D.10℃ 10 mL 2 mol·L-1的X溶液
 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
含镁3%-5%的镁铝合金,现已成为轮船制造、化工生产、机械制造等行业的重要原材料。现有一块已知质量为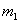 g的镁铝合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案:
g的镁铝合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案:
实验设计1:镁铝合金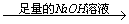 充分反应后测定剩余固体质量
充分反应后测定剩余固体质量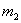 g
g
实验设计2:镁铝合金 生成的气体在标准状况下的体积为VL。
生成的气体在标准状况下的体积为VL。
请回答以下问题:
(1)实验设计1:
①在溶解、过滤中使用的玻璃仪器除烧杯外还有 。
②镁的质量分数: 。如果过滤得到沉淀没有用蒸馏水洗涤数次后烘干,再测定剩余固体质量。则镁的质量分数会 (填“偏大”、“偏小”或“无影响”)。
(2)实验设计2:测定生成的气体装置如右图,进行的操作有:
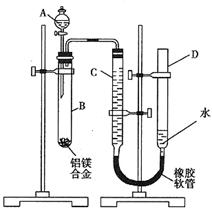 a.记录C的液面位置;
a.记录C的液面位置;
b.由A向B中滴加足量试剂。
c.待B中不再有气体产生并恢复至室温后,记录
C的液面位置;
d.检查气密性;
e. 将药品和水装入各仪器中,连接好;
①上述操作的顺序是:________________(填序号)。
②记录C的液面位置时,除视线平视外,还应注意:
_____________ 。

 (3)请你利用实验设计1和实验设计2的模式再设计一个实验方案测定其中镁的质量分数:
(3)请你利用实验设计1和实验设计2的模式再设计一个实验方案测定其中镁的质量分数:

 铝镁合金 溶液 过滤,测定质量。
铝镁合金 溶液 过滤,测定质量。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:① S(单斜,s)+O2(g) === SO2(g) △H1=-297.16 kJ·mol-1
② S(正交,s)+O2(g) === SO2(g) △H2=-296.83 kJ·mol-1
③ S(单斜,s) === S(正交,s) △H3
下列说法正确的是( )
A.△H3=+0.33 kJ·mol-1
B.单斜硫转化为正交硫的反应是吸热反应
C.S(单斜,s)=== S(正交,s) △H3<0,正交硫比单斜硫稳定
D.S(单斜,s)=== S(正交,s) △H3>0,单斜硫比正交硫稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
下列相应要求的热化学方程式书写正确的是(ΔH的绝对值均正确)( )
A.C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) ΔH=-1 367.0 kJ·mol-1(燃烧热)
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=+57.3 kJ·mol-1(中和热)
C.S(s)+O2(g)===SO2(g) ΔH=-296.8 kJ·mol-1(反应热)
D.2NO2===O2+2NO ΔH=+116.2 kJ·mol-1(反应热)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中,不能用勒夏特列原理解释的是( )
A.红棕色的NO2,加压后颜色先变深后变浅
B.高压比常压有利于SO2合成SO3的反应
C.由H2、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深
D.黄绿色的氯水光照后颜色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
若溶液中由水电离产生的c(OH-)=1×10-14 mol∙L-1,满足此条件的溶液中一定可以大量共存的离子组是( )
A.Al3+、Na+、NO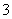 、Cl- B.K+、Na+、Cl-、NO
、Cl- B.K+、Na+、Cl-、NO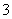
C.K+、Na+、Cl-、AlO D.K+、NH
D.K+、NH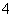 、SO
、SO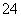 、NO
、NO
查看答案和解析>>
科目:高中化学 来源: 题型:
[化学——选修2:化学与技术](15分)
将海水淡化与浓海水资源化结合起来是综合利用海水的重要途径之一。一般是先将海水淡化获得淡水,再从剩余的浓海水中通过一系列工艺流程提取其他产品。
回答下列问题:
(1)下列改进和优化海水综合利用工艺的设想和做法可行的是________(填序号)。
①用混凝法获取淡水
②提高部分产品的质量
③优化提取产品的品种
④改进钾、溴、镁等的提取工艺
(2)采用“空气吹出法”从浓海水吹出Br2,并用纯碱吸收。碱吸收溴的主要反应是Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3,吸收1 mol Br2时,转移的电子数为________mol。
(3)海水提镁的一段工艺流程如下图:

浓海水的主要成分如下:
| 离子 | Na+ | Mg2+ | Cl- | SO |
| 浓度/(g·L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
该工艺过程中,脱硫阶段主要反应的离子方程式为______________________________,产品2的化学式为__________,1 L浓海水最多可得到产品2的质量为________g。
(4)采用石墨阳极、不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为________________________;电解时,若有少量水存在会造成产品镁的消耗,写出有关反应的化学方程式:____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于煤、石油、天然气等资源的说法正确的是
A.石 油裂解得到的汽油是纯净物
油裂解得到的汽油是纯净物
B.石油产品都可用于聚合反应
C.天然气是一种清洁的化石燃料
D.水煤气是通过煤的液化得到的气体燃料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com