
【题目】下列有关硅的叙述正确的是
A.硅在常温下能跟氧气发生化合反应
B.硅是组成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第一位
C.硅的化学性质不活泼,在常温下不与任何物质反应
D.硅在电子工业中是重要的半导体材料
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案科目:高中化学 来源: 题型:
【题目】等质量且足量的两份锌a、b,分别加入等量的稀H2SO4,同时向a中加入少量的CuSO4溶液,下列各图表示产生H2的体积(V)与时间(t)的关系,其中正确的是 ( )
A. 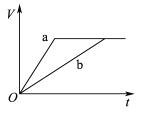 B.
B. 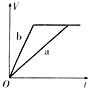
C. 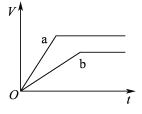 D.
D. 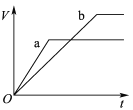
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为落实“五水共治”,某工厂拟综合处理含NH4+废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:
下列说法不正确的是
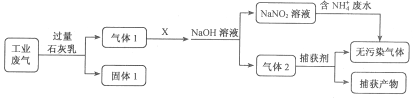
A. 固体1中主要含有Ca(OH)2、CaCO3、CaSO3
B. X可以是空气,且需过量
C. 捕获剂所捕获的气体主要是CO
D. 处理含NH4+废水时,发生反应的离子方程式为:NH4++NO2-==N2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝元素对人体健康有害。因此,世界卫生组织正式把铝确定为食品污染源之一而加以控制。铝在下列场合使用时应加以控制的是( )
①制铝合金②制电线③制炊具④制银色漆颜料⑤用明矾净水⑥明矾和小苏打制食品膨松剂⑦制易拉罐⑧用氢氧化铝凝胶制胃药⑨包装糖果和小食品
A.③⑤⑧⑨B.⑥⑧⑨C.③⑤⑨D.③⑤⑥⑦⑧⑨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年,科学家研究了乙醇催化合成乙酸乙酯的新方法:2C2H5OH(g) ![]() CH3COOC2H5(g)+2H2(g),在常压下反应,冷凝收集,测得常温下液体收集物中主要产物的质量分数如图所示。关于该方法,下列推测不合理的是
CH3COOC2H5(g)+2H2(g),在常压下反应,冷凝收集,测得常温下液体收集物中主要产物的质量分数如图所示。关于该方法,下列推测不合理的是
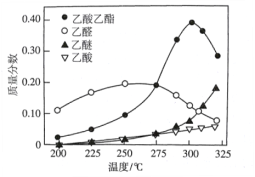
A. 反应温度不宜超过300℃
B. 该反应属于消去反应
C. 在催化剂作用下,乙醛是反应历程中的中间产物
D. 提高催化剂的活性和选择性,减少乙醚、乙烯等副产物是工艺的关键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子![]() 使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用
使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用![]() 表示
表示![]() 请认真观察如图,然后回答问题.
请认真观察如图,然后回答问题.

![]() 图中所示反应是______
图中所示反应是______![]() 填“吸热”或“放热”
填“吸热”或“放热”![]() 反应.
反应.
![]() 已知拆开1mol
已知拆开1mol![]() 键、1mol
键、1mol![]() 、1mol
、1mol![]() 键分别需要吸收的能量为436kJ、151kJ、
键分别需要吸收的能量为436kJ、151kJ、![]() 则由1mol氢气和1mol碘反应生成HI会______
则由1mol氢气和1mol碘反应生成HI会______![]() 填“放出”或“吸收”
填“放出”或“吸收”![]() ______kJ的热量
______kJ的热量![]() 在化学反应过程中,是将______转化为______.
在化学反应过程中,是将______转化为______.
![]() 下列反应中,属于放热反应的是______,属于吸热反应的是______.
下列反应中,属于放热反应的是______,属于吸热反应的是______.
![]() 物质燃烧
物质燃烧
![]() 炸药爆炸
炸药爆炸
![]() 酸碱中和反应
酸碱中和反应
![]() 二氧化碳通过炽热的碳
二氧化碳通过炽热的碳
![]() 食物因氧化而腐败
食物因氧化而腐败
![]() 与
与![]() 反应
反应
![]() 铁粉与稀盐酸反应.
铁粉与稀盐酸反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A+、B2+、C-、D2-4种离子具有相同的电子层结构。现有以下排列顺序:
①B2+>A+>C->D2-②C->D2->A+>B2+③B2+>A+>D2->C-④D2->C->A+>B2+4种离子的半径由大到小以及4种元素原子序数由大到小的顺序分别是( )
A.①④B.④①C.②③D.③②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO3,还含有少量MgO、SiO2等杂质)来制备,工艺流程如下:

回答下列问题:
(1)“酸浸”实验中,铁的浸出率结果如上图所示。由图可知,当铁的浸出率为70%时,所采用的实验条件为_____________。
(2)“酸浸”后,钛主要以![]() 形式存在,写出相应反应的离子方程式________。
形式存在,写出相应反应的离子方程式________。
(3)TiO2·xH2O沉淀与双氧水、氨水反应40 min所得实验结果如下表所示:

分析40 ℃时TiO2·xH2O转化率最高的原因________。
(4)Li2Ti5O15中Ti的化合价为+4,其中过氧键的数目为_______。
(5)若“滤液②”中![]() ,加入双氧水和磷酸(设溶液体积增加1倍),使
,加入双氧水和磷酸(设溶液体积增加1倍),使![]() 恰好沉淀完全即溶液中
恰好沉淀完全即溶液中![]() ,此时是否有
,此时是否有![]() 沉淀生成? ________(列式计算)。
沉淀生成? ________(列式计算)。![]() 的Ksp分别为
的Ksp分别为![]()
(6)写出“高温煅烧②”中由![]() 制备
制备![]() 的化学方程式___________。
的化学方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】干燥剂的干燥性能可用干燥干燥效率(1立方米空气中实际余留水蒸气的质量![]() 来衡量
来衡量![]() 某些干燥剂的干燥效率如下:
某些干燥剂的干燥效率如下:
物质 | MgO | CaO | ZnCl2 | ZnBr2 |
干燥效率 | 0.008 | 0.2 | 0.8 | 1.1 |
根据以上数据,有关叙述错误的是
A. MgO的干燥性能比CaO差 B. 干燥效率可能与干燥剂的阴阳离子半径大小有关
C. MgCl2可能是比CaCl2更好的干燥剂 D. 上述干燥剂中阳离子对干燥性能的影响比阴离子大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com