
某同学对Cl2与KI溶液的反应进行了实验探究。反应装置如下:
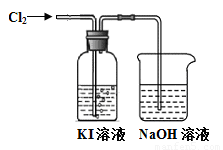
通入氯气一段时间,KI溶液变为黄色。继续通入氯气一段时间后,溶液黄色褪去,变为无色。继续通入氯气,最后溶液变为浅黄绿色。
(1)已知I2+I- I3- , I2、I3-在水中均呈黄色。为确定黄色溶液的成分,进行了以下实验。
I3- , I2、I3-在水中均呈黄色。为确定黄色溶液的成分,进行了以下实验。
| 操作 | 实验现象 |
a | 取2~3 mL黄色溶液,加入足量CCl4, 振荡静置。 | CCl4层呈紫红色, 水层显浅黄色。 |
b | 取2~3 mL饱和碘水,加入足量CCl4, 振荡静置。 | CCl4层呈紫红色,水层几近无色。 |
① 实验b的目的是?? ?????????????????????????????????? ???? 。
② 根据实验a中,水层中含有的粒子有????????????????????????? 。
③ 实验a中水溶液颜色变浅的原因是????????????????????????????????? 。
④ 为保证实验的严谨性,在实验a、b的基础上,需补充一个实验,该实验为??????? 。
(2)通入氯气,溶液由黄色变为无色,是因为氯气将I2氧化。已知1 mol Cl2可氧化0.2 mol I2,该反应的化学方程式是????????????????????????????????? 。
(3) 根据上述实验,请预测向淀粉-KI溶液中持续通入氯气,可能观察到的现象为??????????????? 。
(1)① 对比实验,证明实验a中水层显浅黄色是因为存在I2+I- I3-平衡,不是单一的I2浓度降低所导致的。(2分)
I3-平衡,不是单一的I2浓度降低所导致的。(2分)
② I2、I-、I3-、Cl-、K+(可不写H2O、H+、OH-)(2分)
③ 由于萃取使水溶液中I2浓度降低,同时I2+I- I3-平衡逆向向移动,I3-浓度也降低,导致水溶液颜色变浅。(2分)
I3-平衡逆向向移动,I3-浓度也降低,导致水溶液颜色变浅。(2分)
④ 取2~3 mL KI溶液,滴加少量的氯水(或通入少量氯气,或加入少量碘单质),再加入足量CCl4, 振荡静置,观察到水层是否为黄色。(2分)
【或取少量实验a的水层溶液滴加AgNO3溶液,观察是否有黄色沉淀生成。或取少量实验a的水层溶液淀粉溶液,观察是否变蓝。】
(2)I2+5Cl2+6H2O  10H Cl +2 H IO3(2分)
10H Cl +2 H IO3(2分)
(3)溶液先变蓝后褪色(1分)
【解析】
试题分析:(1)①? 实验b的目的是对比实验,证明实验a中水层显浅黄色是因为存在I2+I- I3-平衡,不是单一的I2浓度降低所导致的。
I3-平衡,不是单一的I2浓度降低所导致的。
② 根据实验a中,取2~3 mL黄色溶液,加入足量CCl4, 振荡静置。因为KI+Cl2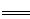 2KCl+I2,水层中,含有含有Cl-、K+,水层显浅黄色,说明存在I2+I-
2KCl+I2,水层中,含有含有Cl-、K+,水层显浅黄色,说明存在I2+I- I3-,对可逆反应I2、I-、I3-均存在;
I3-,对可逆反应I2、I-、I3-均存在;
③ 实验a中水溶液颜色变浅的原因是由于萃取使水溶液中I2浓度降低,同时I2+I- I3-平衡逆向向移动,I3-浓度也降低,导致水溶液颜色变浅。
I3-平衡逆向向移动,I3-浓度也降低,导致水溶液颜色变浅。
④ 为保证实验的严谨性,在实验a、b的基础上,需补充检验I-或I2的实验,所以答案是取2~3 mL KI溶液,滴加少量的氯水(或通入少量氯气,或加入少量碘单质),再加入足量CCl4, 振荡静置,观察到水层是否为黄色。(或取少量实验a的水层溶液滴加AgNO3溶液,观察是否有黄色沉淀生成。或取少量实验a的水层溶液淀粉溶液,观察是否变蓝。)
(2)已知1 mol Cl2可氧化.2 mol I2,知Cl2和I2的系数比是5:1,根据氧化还原反应特点,化合价升降总数相等,判断出I2变为+5价,配平得I2+5Cl2+6H2O  10HCl +2H IO3;
10HCl +2H IO3;
(3)向淀粉-KI溶液中持续通入氯气,可能观察到的现象为溶液先变蓝,I2+5Cl2+6H2O  10HCl +2HIO3所以后褪色;
10HCl +2HIO3所以后褪色;
考点:考查探究实验和实验方案的设计。


科目:高中化学 来源: 题型:阅读理解
| 编号 | 操作 | 现象 |
| I | 先向2mL 0.1mol/L FeCl2溶液中滴加KSCN溶液,再滴加新制氯水 | |
| II | 先向2mL 0.1mol/L FeCl3溶液中滴加KSCN溶液,再滴加0.1mol/L KI溶液 | 滴加KSCN溶液后,溶液变成红色;滴加KI溶液后,红色无明显变化 |
| 编号 | 操作 | 现象 |
| III | 向2mL 0.1mol/L KI溶液中滴加1mL 0.1mol/L FeCl3溶液,再滴加KSCN溶液 | 滴加FeCl3溶液后,溶液变成黄色;滴加KSCN溶液后,溶液变成红色 |
| 编号 | 操作 | 预期现象及结论 |
| IV | 向2mL 0.1mol/L KI溶液中滴加1mL0.1mol/L FeCl3溶液, | 预期现象:溶液变蓝(或溶液分层,下层溶液为紫色;或生成蓝色沉淀),结论:Fe3+能与I-发生氧化还原反应,生成I2(或Fe2+) 预期现象:溶液变蓝(或溶液分层,下层溶液为紫色;或生成蓝色沉淀),结论:Fe3+能与I-发生氧化还原反应,生成I2(或Fe2+) |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 实验编号 | 1 | 2 | 3 |
| 消耗Na2S2O3体积/mL | 26.90 | 27.00 | 26.96 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验操作 | 预期现象和结论 |
| 步骤1: | |
| 步骤2: | |
| … |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

①设计甲装置的目的是_________________。甲装置__________(填“能”或“不能”)用乙装置来代替。
②装置乙中盛有的液体是__________,该装置可看作是一个___________(填某仪器名称)。
(2)在氮的化合物中,有一类盐叫亚硝酸盐,如亚硝酸钠(NaNO2)等。NaNO2是一种潜在的致癌物质,过量或长期使用会对人产生危害。由于亚硝酸钠有咸味,外观与NaCl相似,曾多次发生过被误当食盐使用的事件。已知:HNO2是一种弱酸,不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把I-氧化成I2;AgNO2是一种难溶于水易溶于酸的化合物。试回答下列问题:
①人体正常的血红蛋白中应含Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是_____________。
A.亚硝酸盐是还原剂 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐被还原
②下列说法中,能用来区别NaNO2和NaCl的是______________。
A.测定这两种溶液的pH
B.用AgNO3和HNO3两种试剂来区别
C.在酸性条件下加入KI淀粉试液来区别
③把新制氯气通入到NaNO2溶液中,氯水褪色,生成NaNO3和HCl,请写出此反应的离子方程式______________。
④为了测定某样品中NaNO2的含量,可以使用标准?KMnO4?溶液进行滴定,试回答:KMnO4溶液在滴定过程中作____________(填“氧化剂”或“还原剂”),该滴定过程_____________(填“要”或“不要”)另加指示剂。
⑤已知HNO2的酸性比醋酸略强,某同学在家中进行鉴别NaNO2与NaCl的实验,但他家中只有浓醋酸,请问该实验能否成功?____________(填“能”或“不能”),请说明理由_______
_____________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com