
| A. | 醋酸 | B. | 碳酸钠溶液 | C. | CuSO4溶液 | D. | KCl溶液 |
分析 n[Ba(OH)2]=$\frac{17.1g}{171g/mol}$=0.1mol,溶液中溶质的物质的量=1mol/L×0.1L=0.1mol,溶液导电性强弱与离子浓度成正比,离子浓度变化最小,则溶液导电性变化最小,据此分析解答.
解答 解:n[Ba(OH)2]=$\frac{17.1g}{171g/mol}$=0.1mol,溶液中溶质的物质的量=1mol/L×0.1L=0.1mol,溶液导电性强弱与离子浓度成正比,离子浓度变化最小,则溶液导电性变化最小,
A.醋酸是弱电解质,醋酸溶液中离子浓度较小,则醋酸溶液导电性较弱,加入氢氧化钡后生成强电解质醋酸钡,导致离子浓度变化较大,溶液导电性变化较大,故A不选;
B.碳酸钠是强电解质,离子浓度较大,导电性较强,加入氢氧化钡后生成碳酸钡和氢氧化钠,NaOH仍然是强电解质,离子浓度变化不大,溶液导电性变化不大,故B选;
C.硫酸铜是强电解质,离子浓度较大,导电性较强,加入氢氧化钡后生成硫酸钡沉淀和水,离子浓度变化较大,溶液导电性变化较大,故C不选;
D.KCl是强电解质,离子浓度较大,导电性较强,加入氢氧化钡后二者不反应,离子浓度变化较大,溶液导电性变化较大,故D不选;
故选B.
点评 本题考查溶液导电性强弱判断,为高频考点,侧重考查学生分析判断能力,明确溶液导电性强弱影响因素及物质之间的反应是解本题关键,溶液导电性强弱与离子浓度成正比,与电解质强弱无关.


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案科目:高中化学 来源: 题型:选择题
| A. | 含大量SO2的溶液中:NH4+、F-、HCO3-、ClO- | |
| B. | 能使淀粉碘化钾试纸变蓝的溶液:Cl-、Na+、S2-、NH4+ | |
| C. | $\frac{{k}_{w}}{c({H}^{+})}$=10-13mol/L的溶液中:Al3+、Fe3+、NO3-、ClO4- | |
| D. | 滴入KSCN溶液显红色的溶液中:NO3+、Na+、AlO2-、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 编号 | 热化学方程式 | 化学平衡常数 |
| ① | CO(g)+2H2(g)?CH3OH(g)△H1 | K1 |
| ② | 2CH3OH(g)?CH3OCH3(g)+H2O(g)△H2=-24kJ/mol | K2 |
| ③ | CO(g)+H2O(g)?CO2(g)+H2(g)△H3=-41kJ/mol | K3 |
| 化学键 | H-H | C≡O | C-O | H-O | C-H |
| E/(kJ/mol) | 436 | 1076 | 343 | 465 | 413 |
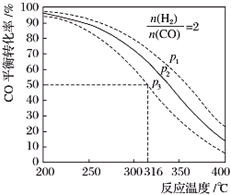
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4:9:24:14:28 | B. | 1:2:5:3:6 | C. | 8:9:12:10:20 | D. | l:l:l:l:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9种、7种、6种 | B. | 9种、5种、6种 | C. | 7种、5种、4种 | D. | 8种、5种、5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铅蓄电池属于二次电池,在充电过程中,阳极质量减小,阴极质量增加 | |
| B. | 常温下,能自发进行的反应,△H一定小于“0” | |
| C. | 一定条件下,使用催化剂能加快反应速率并提高反应物的活化能 | |
| D. | 相同条件下,溶液中Fe3+、Cu2+、Zn2+的氧化性依次减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由元素X与Z形成的化合物中只含共价键 | |
| B. | XY2、ZY2、M2Y2的晶体分别属于3种不同类型的晶体 | |
| C. | 单质M的晶体是体心立方堆积,M的配位数是8 | |
| D. | X的氢化物X2H2分子中含有2个σ键和3个π键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com