
【题目】下列实验能成功的是( )
A. 将铁屑、溴水、苯混合制溴苯
B. 苯和硝基苯采用分液的方法分离
C. 聚乙烯使酸性KMnO4溶液褪色
D. 用水鉴别:苯、乙醇、四氯化碳
 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:
【题目】铝(熔点660℃)是一种应用广泛的金属,工业上用A12O3(熔点2045℃)和冰晶石(Na2AlF6,六氟合铝酸钠)混合熔融后电解制得。回答下列问题:
(l)铝属于活泼金属却能在空气中稳定存在,原因是(用化学用语及相关文字说明)_______.
(2)将0.1 mol/L AlCl3溶液和10%NH4F溶液混合制取Na2AlF6。该实验所用试管及盛装NaF 溶液的试剂瓶均为塑料材质,原因是____________。
(3)下列关于氧化铝的叙述正确的是_______
A.氧化铝可以治疗胃酸过多。
B.氧化铝因为熔点高,可以作耐火材料.
C.氧化铝是铝热剂的成分之一。
D.氧化铝是两性氧化物,所以既能溶于盐酸又能溶于氨水。
(4)某工厂排放出有毒物质NOCl , 它遇水就会生成NO3-。NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为_________。水源中的NO3-对人类健康会产生危害。为了降低水源中NO3-的浓度,有研究人员建议在碱性条件下用铝粉将NO3-还原为N2,该反应的离子方程式为_________,此方法的缺点是处理后的水中生成了A1O3-,仍然可能对人类健康产生危害,还需要对该饮用水进行一系列后续处理。
已知25℃时,Ksp[Al(OH)3] = l.3×l0-33 Al(OH)3![]() AlO2-+H++H2O K=1.0×10-13
AlO2-+H++H2O K=1.0×10-13
25℃时,若欲使上述处理后的水中A1O2-浓度降到1.0×10-6mol/L,则应调节至pH=_______。
此时水中c(A13+)=__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【加试题】节能减排已经成为全社会的共识,浙江省在原先推行乙醇汽油的基础上,开始试点甲醇汽油(即在汽油中添加一定量的甲醇),根据检测的数据分析认为,若绍兴全市的100余万辆机动车全部使用甲醇汽油,一年内能减少有害气体(一氧化碳)排放将近100万吨。甲醇常利用煤气化过程中生成的CO和H2来制备:CO+2H2CH3OH 。
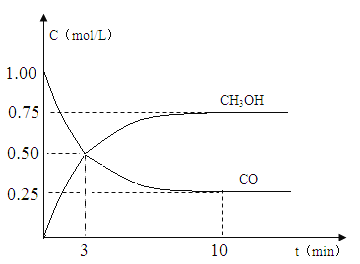
请根据图示回答下列:
(1)关于该自发反应的下列说法中,正确的是 (填字母):
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
(2)现进行如下实验,在体积为1L的密闭容器中,充入1molCO和3molH2,测得CO和CH3OH(g)的浓度随时间变化如图所示。从反应开始到平衡,CO的平均反应速率v(CO)= mol/(Lmin),该反应的平衡常数K= 。
(3)恒容条件下,达到平衡后,下列措施中能使n(CH3OH)/n(CO)增大的有 。
A.升高温度 B.充入He气 C.再冲入1molCO和3molH2 D.使用催化剂
(4)若在一体积可变的密闭容器中充入1molCO、2molH2和1molCH3OH,达到平衡时测的混合气体的密度是同温同压下起始的1.6倍(此过程三种物质均处于气态),则平衡时混合气体的平均摩尔质量= g/mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水的状态除了气、液和固态外,还有玻璃态。它是由液态水急速冷却到165 K时形成的,玻璃态的水无固定形状,不存在晶体结构,且密度与普通液态水的密度相同,有关玻璃态水的叙述正确的是
A. 水由液态变为玻璃态,体积缩小
B. 水由液态变为玻璃态,体积膨胀
C. 玻璃态是水的一种特殊状态
D. 玻璃态水是分子晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:pOH=-lgc(OH-),在常温下溶液中的pH+pOH=14,又已知正常人(人的体温高于室温)的血液pH=7.3,则正常人血液的pOH是( )
A. 大于6.7 B. 小于6.7
C. 等于6.7 D. 无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能够鉴定氯乙烷中氯元素的存在的最佳操作是( )
A. 在氯乙烷中直接加入AgNO3溶液
B. 加蒸馏水,充分搅拌后,加入AgNO3溶液
C. 加入NaOH溶液,加热后加入稀硝酸酸化,然后加入AgNO3溶液
D. 加入NaOH的乙醇溶液,加热后加入AgNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某含镍(NiO)废料中有FeO、Al2O3、MgO、SiO2等杂质,用此废料提取NiSO4的工艺流程如图:

已知:①有关金属离子生成氢氧化物沉淀所需的pH如图。

②25℃时,NH3·H2O的电离常数Kb=1.8×10-5。
HF的电离常数Ka=7.2×10-4,Ksp (MgF2)=7.4×10-11。
(1)加Na2CO3调节溶液的pH至5,得到废渣2的主要成分是__________(填化学式)。
(2)Mg能与饱和NH4Cl溶液反应产生NH3,请用化学平衡移动原理解释(用必要的文
字和离子方程式回答)_______________________________________。
(3)25 ℃时,1 mol·L-1的NaF溶液中c(OH-)=________ mol·L-1(列出计算式即可)。
NH4F溶液呈 _____(填“酸性”、“碱性”或“中性”)。
(4)已知沉淀前溶液中c(Mg2+)=1.85×10-3mol·L-1,当除镁率达到99%时,溶液中c(F-)=_______ mol·L-1。
(5)在NaOH溶液中用NaClO与NiSO4反应可得NiO(OH),化学方程式为________________________________;NiO(OH)与贮氢的镧镍合金可组成镍氢碱性电池(KOH溶液),工作原理为:LaNi5H6+6NiO(OH) ![]() LaNi5+6NiO+6H2O,负极的电极反应式:__________________________________。
LaNi5+6NiO+6H2O,负极的电极反应式:__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、生产科技密切相关。下列说法错误的是
A. 单质硅可用于制取通信芯片
B. 《天工开物》中描述:“世间丝、麻、袭、褐皆具素质……文中的丝、麻主要成分是蛋白质
C. 航母上拦阻索中的钢丝属于金属材料
D. 工业生产玻璃、水泥、漂白粉,均需要用石灰石为原料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com