
| A、铁跟稀硫酸反应:Fe+2H+═Fe2++H2↑ |
| B、Ca(HCO3)2溶液和盐酸反应:Ca(HCO3)2+2H+═Ca2++2H2O+2CO2↑ |
| C、醋酸跟氢氧化钾溶液反应:CH3COOH+OH-═CH3COO-+H2O |
| D、MgCO3跟稀硫酸反应:MgCO3+2H++SO42-═MgSO4↓+H2O+CO2↑ |


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
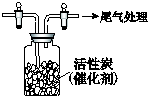 某学习小组依据SO2具有还原性,推测SO2能被Cl2氧化生成SO2Cl2.
某学习小组依据SO2具有还原性,推测SO2能被Cl2氧化生成SO2Cl2.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若金属没有剩余,反应中转移的电子数目为2y NA | ||
| B、若金属全部溶解,则溶液中一定含有Fe3+ | ||
C、当溶液中金属离子只有Fe3+、Cu2+时,则a与b的关系为:b≥80y(1-
| ||
| D、若金属全部溶解,且产生336mL气体(标准状况),则b=0.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一氧化碳是不稳定的氧化物,它能继续和氧气反应生成稳定的二氧化碳,故反应一定是吸热反应 |
| B、在101kPa时,1mol碳燃烧所放出的热量为碳的燃烧热 |
| C、物质燃烧都需要氧气 |
| D、物质燃烧放出热量的多少与外界条件有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是我国“长征二号F”运载火箭发射现场.图中可以看到从火箭的下部喷射出大量的红棕色的气体,关于这种红棕色气体的认识正确的是( )
如图是我国“长征二号F”运载火箭发射现场.图中可以看到从火箭的下部喷射出大量的红棕色的气体,关于这种红棕色气体的认识正确的是( )| A、是溴蒸气,火箭发射时作氧化剂 |
| B、是二氧化氮气体,火箭发射时作还原剂 |
| C、是溴蒸气,火箭发射时作还原剂 |
| D、是二氧化氮气体,火箭发射时作氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、仅①④ | B、仅①②④ |
| C、除⑤外 | D、全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、物质的量就是物质的数量 |
| B、1mol任何物质都含有6.02×1023个原子 |
| C、1mol水中含有1mol氢分子和1mol氧原子 |
| D、1mol H2分子中含有2mol H |
查看答案和解析>>
科目:高中化学 来源: 题型:
 X、Y、Z、R、W、M五种元素分别位于周期表中四个紧邻的周期,原子序数依次增大,其它相关信息如下列两表所示:
X、Y、Z、R、W、M五种元素分别位于周期表中四个紧邻的周期,原子序数依次增大,其它相关信息如下列两表所示:| 元素 | 相关信息 |
| X | X原子的价电子构型为nsn |
| Y | Y与R位于同主族 |
| Z | Z是除稀有气体外第一电离能最大的元素 |
| W | W的单质是人们将太阳能转换为电能的常用材料 |
| M | M是人们生活中最常用的金属 |
| I1 | I2 | I3 | I4 | I5 | |
| R的电离能/kJ?mol-1 | 584 | 1823 | 2751 | 11584 | 14837 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com