
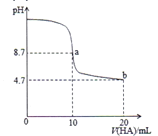
【题目】室温下,将0.1mol/L的一元酸HA溶液逐滴滴加到10mL0.1mol/LNaOH溶液中,pH的变化曲线如图所示。下列说法错误的是
A. a点所示溶液中c(Na+)>c(A-)>c(OH-)>c(HA)
B. a、b两点所示溶液中水的电离程度a点大于b点
C. pH=7时,c(Na+)=c(A-)+c(HA)
D. 一元酸HA为弱酸
【答案】C
【解析】A. a点时加入10mL的一元酸HA,酸碱恰好中和得到NaA溶液,溶液的pH=8.7,说明NaA为强碱弱酸盐,A-发生水解反应A-+H2O![]() HA+ OH-且水解是微弱的,则c(Na+)>c(A-)>c(OH-),因水也电离产生OH-,则c(OH-)>c(HA),所以微粒浓度大小顺序为:c(Na+)>c(A-)>c(OH-)>c(HA),故A正确;B. a点时溶液中只有NaA,A-发生水解促进水的电离,b点溶液中酸过量,酸抑制水的电离,所以a、b两点所示溶液中水的电离程度a点大于b点,故B正确;C. pH=7时,c(H+)=c(OH-),由电荷守恒可知,c(Na+)+ c(H+)=c(A-)+c(OH-),则c(Na+)=c(A-),故C错误;D. 根据A项分析可知,HA为一元弱酸,故D正确;答案选C。
HA+ OH-且水解是微弱的,则c(Na+)>c(A-)>c(OH-),因水也电离产生OH-,则c(OH-)>c(HA),所以微粒浓度大小顺序为:c(Na+)>c(A-)>c(OH-)>c(HA),故A正确;B. a点时溶液中只有NaA,A-发生水解促进水的电离,b点溶液中酸过量,酸抑制水的电离,所以a、b两点所示溶液中水的电离程度a点大于b点,故B正确;C. pH=7时,c(H+)=c(OH-),由电荷守恒可知,c(Na+)+ c(H+)=c(A-)+c(OH-),则c(Na+)=c(A-),故C错误;D. 根据A项分析可知,HA为一元弱酸,故D正确;答案选C。


科目:高中化学 来源: 题型:
【题目】化学是一门以实验为基础的自然科学。
(1)近年频繁发生的有关化学品泄漏或爆炸事件一次次给我们敲响了安全警钟,操作不当就会存在安全隐患。下列做法正确的是_______________。
①将水沿着烧杯内壁缓缓加入浓硫酸中,并用玻璃棒不断搅拌;
②酒精、钠等着火,可以用水扑灭;
③如果发生氯气泄露,可用沾Na2CO3溶液的湿毛巾捂住口鼻,向上风口或地势高的地方撤离;
④夜间厨房发生煤气泄漏时,应立即开灯检查煤气泄漏原因,并打开所有门窗通风;
⑤不慎将浓硫酸沾到皮肤上,要立即用干布拭去,再用大量水冲洗,然后涂上NaOH溶液;
⑥加热液体的试管口不能对着自己或别人;
⑦实验中当有少量的过氧化钠或金属钠剩余时,用纸包裹好后将其放入垃圾桶中
(2)某同学需要配制0.1mol·L-1 的NaHCO3溶液500mL,请根据溶液配制过程中的情况回答下列问题:
①应称取固体NaHCO3的质量为____________________。
②实验中除了托盘天平(带砝码和镊子)、烧杯、药匙、玻璃棒外还需要的其它仪器有_________________________
③定容观察液面时俯视刻度线,所配溶液浓度_______(填“偏高”、“偏低”或“无影响”)
④所配的NaHCO3溶液在保存时,常因温度过高而分解,含有少量Na2CO3,若要除去杂质Na2CO3,最简便的方法是_______,其反应的离子方程式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NOx是大气污染物之一,主要来源于工业烟气及汽车尾气等。除去NOx的方法统称为脱硝,一般有干法脱硝[选择性催化剂法(SCR)]、湿法脱硝等。
请完成下列问题:
(1)汽车发动机工作时会引发反应N2(g)+O2(g)![]() 2NO(g)。2000 K 时,向固定容积的密闭容器中充入等物质的量的N2、O2 发生上述反应,各组分体积分数(φ)的变化如图1所示。N2 的平衡转化率为_____________。
2NO(g)。2000 K 时,向固定容积的密闭容器中充入等物质的量的N2、O2 发生上述反应,各组分体积分数(φ)的变化如图1所示。N2 的平衡转化率为_____________。

(2)在密闭、固定容积的容器中,一定量NO发生分解的过程中,NO 的转化率随时间变化关系如图2 所示。
①反应2NO(g)![]() N2(g)+O2(g) △H_______0 (填“>”或“<” )。
N2(g)+O2(g) △H_______0 (填“>”或“<” )。
②一定温度下,能够说明反应2NO(g)![]() N2(g)+O2(g)已达到化学平衡的________(填序号)。a.容器内的压强不发生变化 b.混合气体的密度不发生变化
N2(g)+O2(g)已达到化学平衡的________(填序号)。a.容器内的压强不发生变化 b.混合气体的密度不发生变化
C.NO、N2、O2 的浓度保持不变 d.2v(NO)正=v(N2 )逆
(3)干法脱硝:SCR(选择性催化剂法)技术可有效降低柴油发动机在空气过量条件下的NO 排放。其工作原理如下:

①尿素[CO(NH2)2]水溶液热分解为NH3和CO2,该反应的化学方程式为____________。
②反应器中NH3 还原NO 的化学方程式为____________________。
(4)湿法脱硝:采用NaClO2 溶液作为吸收剂可对烟气进行脱硝。323 K 下,向足量碱性NaClO2 溶液中通入含NO 的烟气,充分反应后,溶液中离子浓度的分析结果如下表:
离子 | NO3- | NO2- | Cl- |
c/(mol L-1) | 2.0×10-4 | 1.0×10-4 | 1.75×10-4 |
①NaClO2 溶液显碱性,用离子方程式解释原因_______________________。
②依据表中数据,写出NaClO2溶液脱硝过程中发生总反应的离子方程式_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2H4通常用作火箭的高能燃料,N2O4作氧化剂.请回答下列问题:
(1)已知:N2(g)+2O2(g)═2NO2(g)△H=+a kJ/mol
N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=﹣b kJ/mol
2NO2(g)N2O4(g)△H=﹣c kJ/mol
写出气态肼在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式 .
(2)N2、H2合成氨气为放热反应.800K时向下列起始体积相同的密闭容器中充入2molN2、3molH2 , 甲容器在反应过程中保持压强不变,乙容器保持体积不变,丙是绝热容器,三容器各自建立化学平衡.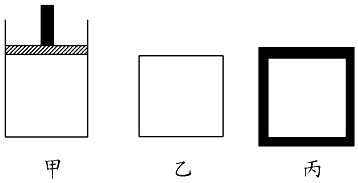
①达到平衡时,平衡常数K甲K乙K丙(填“>”、“<”或“=”).
②达到平衡时N2的浓度c(N2)甲c(N2)乙,c(N2)乙c(N2)丙(填“>”、“<”或“=”).
③对甲、乙、丙三容器的描述,以下说法正确的是 .
A.乙容器气体密度不再变化时,说明此反应已达到平衡状态
B.在甲中充入稀有气体He,化学反应速率加快
C.向甲容器中充入氨气,正向速率减小,逆向速率增大
D.丙容器温度不再变化时说明已达平衡状态.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关细胞内化合物的叙述,正确的是( )
A.水分子可缓和细胞的温度变化
B.无机盐在细胞内多以化合物存在
C.二糖和单糖均可进一步水解
D.磷脂是细胞内重要的贮能物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的数值,下列说法正确的是(N﹣14 O﹣16 C﹣12 H﹣1)( )
A.常温常压下,46 g的NO2和N2O4混合气体含有的原子数为3NA
B.标准状况下,22.4 L CH2Cl2中含有的氯原子数目为2NA
C.16g CH4与18 g NH4+ 所含质子数相等
D.1molCu在足量硫蒸气中反应时转移2NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把一块生物组织或结构捣碎后进行化学分析,得知其中含有水、蛋白质、DNA和糖原等成分,由此可判断该组织或结构是 ( )
A.SARS病毒 B.家兔的肝脏 C.甜菜的块根 D.细菌
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年中国首次海域可燃冰(CH4·nH2O,密度ρ1 g·cm-3)试开采成功。若以辛烷代表汽油(密度ρ2 g·cm-3)的组成,下列说法不正确的是
① CH4(g) + 2O2(g) =CO2(g) + 2H2O(l) ΔH1 = —a kJ·mol-1
② 2C8H18(l) + 25O2(g) =16CO2 (g) + 18H2O(l) ΔH 2 = —b kJ·mol-1
A. 可燃冰适宜保存在低温,高压的环境中
B. 1 m3可燃冰可释放出标准状况下![]() m3的CH4
m3的CH4
C. 汽油的燃烧热约为0.5b kJ·mol-1
D. 1m3可燃冰释放出的甲烷燃烧放出的热量约为等体积汽油的![]() 倍
倍
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com