
【题目】测定室温下NH3H2O的浓度及电离平衡常数Kb
(1)从三颈瓶中用(填仪器名称)量取25.00mL氨水至锥形瓶中,用0.0500molL﹣1HCl滴定.用pH计采集数据、电脑绘制滴定曲线如下图. 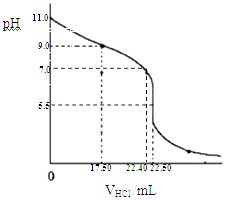
(2)据图,计算氨水的浓度为molL﹣1;写出NH3H2O电离平衡常数Kb的表达式,Kb= , 当pH=11.0时计算Kb的近似值,Kb≈ . (Kb保留两位有效数字)
(3)关于该滴定实验的说法中,正确的是 .
A.锥形瓶中有少量蒸馏水不影响测定结果
B.未滴加酸碱指示剂,实验结果不科学
C.酸式滴定管未用盐酸润洗会导致测得氨水的浓度偏高
D.滴定终点时俯视读数会导致测得氨水的浓度偏高.
【答案】
(1)碱式滴定管(或移液管)
(2)0.0450;  ;2.2×10﹣5
;2.2×10﹣5
(3)AC
【解析】解:(1)氨水中含有一水合氨,一水合氨电离出氢氧根离子而使溶液呈碱性,所以用移液管或碱式滴定管量取氨水,
所以答案是:碱式滴定管(或移液管);(2)氨水的物质的量浓度= ![]() mol/L=
mol/L= ![]() mol/L=0.0450mol/L;pH=11的氨水中c(OH﹣)=0.001mol/L,c(OH﹣)≈c(NH4+)=0.001mol/L,c(NH3H2O)≈0.0450mol/L,根据Kb=
mol/L=0.0450mol/L;pH=11的氨水中c(OH﹣)=0.001mol/L,c(OH﹣)≈c(NH4+)=0.001mol/L,c(NH3H2O)≈0.0450mol/L,根据Kb= ![]() =
= ![]() =2.2×10﹣5;
=2.2×10﹣5;
所以答案是:0.0450; ![]() ;2.2×10﹣5;(3)A.锥形瓶中有少量蒸馏水不影响氨水的物质的量,所以不影响测定结果,故A正确;
;2.2×10﹣5;(3)A.锥形瓶中有少量蒸馏水不影响氨水的物质的量,所以不影响测定结果,故A正确;
B.利用pH计判断滴定终点更准确,不需要酸碱指示剂即可,故B错误;
C.酸式滴定管未用盐酸润洗会导致盐酸浓度偏低,则使用盐酸的体积偏大,所以导致测定结果偏高,故C正确;
D.滴定终点时俯视读数会导致盐酸体积偏小,则盐酸物质的量偏小,测定结果偏低,故D错误.
所以答案是:AC.
【考点精析】利用弱电解质在水溶液中的电离平衡对题目进行判断即可得到答案,需要熟知当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理.


 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:
【题目】合成氨工业中,每生产2molNH3 , 放出92.4kJ热量.
(1)写出合成氨反应的热化学方程式为 .
(2)已知: 
1mol N﹣H键断裂吸收的能量等于kJ.
(3)已知关于铁的氧化物存在下列三个热化学方程式: Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=﹣24.8kJ/mol ①
Fe2O3(s)+ ![]() CO(g)═
CO(g)═ ![]() Fe3O4(s)+
Fe3O4(s)+ ![]() CO2(g)△H=﹣15.73kJ/mol ②
CO2(g)△H=﹣15.73kJ/mol ②
Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=+640.4kJ/mol ③
则CO还原FeO的热化学方程式为CO(g)+FeO(s)═Fe(s)+CO2(g)△H=kJ/mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用100 mL 1 mol·L-1硫酸与锌粉反应制备氢气,下列措施一定能加快反应速率的是
A.改用300 mL 1 mol·L-1硫酸B.降低温度
C.用锌粒代替锌粉D.滴加少量CuSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学想通过实验探究硫和碳得电子能力的强弱,通过比较它们最高价氧化物对应水化物的酸性强弱来验证,设计了如图实验。

(1)仪器a的名称是________,应盛放下列药品中的________(填字母)。
A.稀硫酸 B.亚硫酸C.氢硫酸 D.盐酸
(2)仪器b的名称是________,应盛放下列药品中的________(填字母)。
A.碳酸钙 B.硫酸钠 C.氯化钠 D.碳酸钠
(3)仪器c中应盛放的试剂是________,如果看到的现象是____________________,证明b中反应产生了________,即可证明________比________酸性强,得电子能力________比________强,b中发生反应的离子方程式为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 油脂属于酯类化合物,酯类在碱性条件下的水解叫皂化反应
B. 用电子式表示氯化氢分子的形成过程:![]()
C. 浓硝酸溅在皮肤上,使皮肤呈黄色是由于浓硝酸和蛋白质发生了颜色反应
D. 工业上常用电解熔融AlCl3的方法来制备单质铝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中提取溴的工业流程如图:
(1)以上步骤I中已获得游离态的溴,步骤II又将之转变成化合态的溴,其目的是 。
(2)步骤Ⅱ通入热空气或水蒸气吹出Br2,利用了溴的 。
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(3)以上流程Ⅱ中涉及的离子反应如下,请在下面方框内填入适当的化学计量数及相应物质:
口Br2 + 口CO32-![]() 口BrO3-+ 口Br-+ 口
口BrO3-+ 口Br-+ 口
(4)上述流程中吹出的溴蒸气, 也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏,写出溴与二氧化硫水溶液反应的化学方程式: 。
(5)实验室分离溴还可以用溶剂萃取法,下列可以用作溴的萃取剂的是 。
A.乙醇 B.四氯化碳 C.烧碱溶液 D.苯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com