
将下列5种物质:N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上______+______→______+______+______+______ 组成一个未配平的化学方程式,正确的顺序是
A.FeSO4、Fe(NO3)3; Fe2(SO4)3、HNO3 、N2O、H2O
B.HNO3、FeSO4; Fe2(SO4)3、Fe(NO3)3、N2O 、H2O
C.HNO3、Fe2(SO4)3; FeSO4、Fe(NO3)3、N2O、H2O
D.Fe2(SO4)3、N2O; FeSO4、HNO3 、Fe(NO3)3、H2O
科目:高中化学 来源:2015-2016学年湖南师大附属中学高二上二次阶段测化学卷(解析版) 题型:选择题
在蒸发皿中加热蒸干下列物质的溶液,再高温灼烧可以得到原溶质固体的是
A.AlCl3 B.NaHCO3 C.MgSO4 D.KMnO4
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西省高一上12月月考化学试卷(解析版) 题型:选择题
在一些高档茶叶、点心等食品的包装盒中有一个小袋,将小袋打开,可看到灰黑色粉末,其中有些已变成棕褐色,将灰黑色粉末溶于盐酸,取上层清液,滴入几滴氯水,再滴入KSCN溶液,马上出现血红色,以下结论不正确的是
A.该灰黑色粉末作抗氧化剂
B.该灰黑色粉末不可食用
C.小袋中原来装有铁粉
D.小袋中原来装有Fe2O3
查看答案和解析>>
科目:高中化学 来源:2016届天津市高三上12月学业调研化学试卷(解析版) 题型:填空题
运用化学反应原理研究物质的性质具有重要意义。请回答下列问题:
(1)氨气可以构成燃料电池,其电池反应原理为4NH3+3O2═2N2+6H2O。电解质为KOH溶液,则负极反应式为______________________________。
(2)向BaCl2溶液中通CO2不会出现沉淀,因此某同学根据相同的理由认为向BaCl2溶液中通入SO2也不会出现沉淀,但在实验验证中发现了异常情况,将SO2通入BaCl2溶液中开始并无沉淀,放置一段时间出现了白色沉淀,则产生该沉淀的离子反应方程式为_ 。
(3)有人认为Mg、Si的单质用导线连接后插入NaOH溶液中可以形成原电池,你认为是否可以,若可以,试写出负极的电极方程式(若认为不行可不写):___________________。
查看答案和解析>>
科目:高中化学 来源:2016届贵州省高三上学期1月月考理综化学试卷(解析版) 题型:选择题
有机物M 的结构简式如下: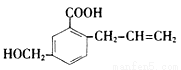 下列有关M 的叙述不正确的是
下列有关M 的叙述不正确的是
A.M的分子式为C11H12O3
B.能使溴的四氯化碳溶液褪色
C.一定条件下,M能生成高分子化合物
D.能发生加成反应不能发生取代反应
查看答案和解析>>
科目:高中化学 来源:2015-2016年海南省高一上第三次月考化学试卷(解析版) 题型:填空题
(1)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有____性(填氧化性或还原性)。铁粉也可以将Fe3+转变为易吸收的Fe2+,离子方程式为:_________________。
(2)印刷电路板是高分子材料和铜箔复合而成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”溶解铜箔,生成CuCl2和FeCl2相关的化学方程式:________________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016年湖南湘潭、岳阳两校高二上第三次联考化学卷(解析版) 题型:选择题
含有一个双键的烯烃,和H2加成后的产物结构简式如下图,则此烃可能有的结构有
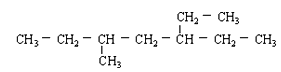
A.5种 B.6种 C.7种 D.8种
查看答案和解析>>
科目:高中化学 来源:2015-2016年山东省高一上12月月考化学试卷(解析版) 题型:选择题
纯碱和小苏打是厨房中两种常见的用品,它们都是白色固体。下列区分这种两种物质的方法正确的是
A.分别用炒锅加热两种样品,全部分解挥发,没有物质残留的是小苏打
B.先将两样品配成溶液,分别加入CaCl2,无白色沉淀生成的是小苏打
C.两只小玻璃杯,分别加入少量两种样品,再加入等浓度等体积的食醋,产生气泡快的是小苏打
D.先将两样品配成溶液,分别加入澄清石灰水,无白色沉淀生成的是小苏打
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省宝安第一外国语学校高二上期中考试化学试卷(解析版) 题型:填空题
在一个温度和体积不变的容器中,硫可以发生如下转化,其反应过程和能量关系如图1所示。(SO2(g)+1/2O2(g) SO3(g) ΔH=-98.45kJ·mol-1)
SO3(g) ΔH=-98.45kJ·mol-1)
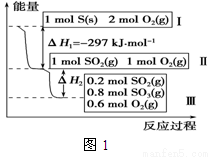
(1)硫燃烧的热化学方程式为:__________________。
(2)恒容条件下,下列措施中能使n(SO2)/ n(SO3)比图1所示情况减小的有____________。
A.降低温度 B.充入He C.再充入1 mol SO2(g)和1 mol O2(g) D.使用催化剂
(3)恒温恒容时,图1中II到III反应放出的热量比1 mol SO2和2 mol O2充分反应放出的热量__________
(填 “多”、“少”或“相等”)。
(4)某SO2(g)和O2(g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2(g)的量,则图中t2时引起平衡移动的条件可能是_____________;图中表示平衡混合物中SO3的含量最高的一段时间是_____________。(如t1~t2、t3~t4、t5~t6 、t6~t7等)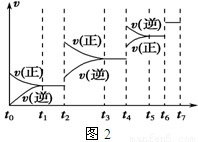
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com