
| A、无色溶液中:K+、Na+、MnO4-、SO42- |
| B、c(Fe3+)=0.1 mol/L的溶液中:K+、ClO-、SO42-、SCN- |
| C、由水电离出的c(OH-)=10-13mol?L-1的溶液中:Na+、Ba2+、Cl-、Br- |
| D、能使甲基橙变黄色的溶液中:Na+、NO3-、S2-、AlO2- |


 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:高中化学 来源: 题型:
 ,这种脂肪醇为( )
,这种脂肪醇为( )| A、CH3CH2CH2OH |
| B、CH2=CH-CH2-OH |
C、 |
D、 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:1:1 |
| B、6:2:3 |
| C、4:3:18 |
| D、2:1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径:丁>丙>乙>甲 |
| B、单质的氧化性:乙>丙>丁 |
| C、气态氢化物稳定性:乙>丙>丁 |
| D、甲与乙、丙、丁形成的化合物均为共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有④ | B、有④⑤ |
| C、有②④⑤ | D、全部都对 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Al3+、NH4+、Br-、Cl- |
| B、Na+、Mg2+、ClO-、NO3- |
| C、K+、MnO4-、CH3CHO、SO42- |
| D、Na+、K+、SiO32-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等物质的量的N2和CO所含分子数均为NA |
| B、1 mol Na2O2 固体中含离子总数为4 NA |
| C、1.7 g H2O2中含有的电子数为0.9 NA |
| D、标准状况下,2.24 L甲烷所含共价键数为0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2 mol重水含有NA个D2O分子 |
| B、1 g氢气含有NA个H2分子 |
| C、2 mol钠与过量稀盐酸反应生成NA个H2分子 |
| D、22.4 L水含有NA个H2O分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:

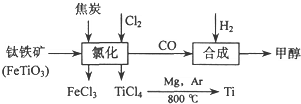
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com