

分析 (1)根据实验发生装置→除杂装置→收集装置→尾气处理装置排序;
(2)发生装置是制备氯气的装置,需要圆底烧瓶、分液漏斗和酒精灯等;
(3)实验制备氯气气的反应为二氧化锰和浓盐酸加热反应生成氯化锰、氯气和水;
(4)浓盐酸与MnO2发生化学反应,随着反应的进行,盐酸的浓度降低,还原性减弱,稀盐酸与MnO2不反应,以此解答该题;
(5)根据氯气、氯化氢的溶解性大小分析;
(6)氯气有毒,多余的氯气需要用氢氧化钠吸收;
(7)氯气为黄绿色气体,密度大于空气密度,依据集气瓶是否充满黄绿色气体判断;
解答 解:(1)实验装置的连接顺序为:发生装置→除杂装置→收集装置→尾气处理装置;除杂装置中长导管进气、短导管出气;因为饱和食盐水中有水,浓硫酸有吸水性,所以先连接盛有饱和食盐水的装置后连接盛浓硫酸的装置;收集装置中,氯气的密度大于空气的,应该采用长进短出的方式,故导管连接顺序为:E-C-D-A-B-H-G-F,
故答案为:E-C;D-A;B-H;G-F;
(2)在制备氯气的发生装置中,用到的玻璃仪器除酒精灯外,还有反应容器圆底烧瓶、添加浓盐酸的分液漏斗、加热需要的酒精灯等,所以用到的玻璃仪器除酒精灯外,还有圆底烧瓶、分液漏斗,
故答案为:圆底烧瓶、分液漏斗;
(3)气体发生装置中进行的反应是氯气的实验室制备,反应的离子方程式为:MnO2+2Cl-+4H+$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,
故答案为:MnO2+2Cl-+4H+$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
(4)反应的化学方程式为:4HCl(浓)+MnO2 $\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,
A.n(HCl)=$\frac{146g}{36.5g/mol}$=4mol,n(MnO2)=$\frac{174g}{87g/mol}$=2mol,浓盐酸与MnO2发生化学反应,随着反应的进行,盐酸的浓度降低,还原性减弱,稀盐酸与MnO2不反应,所以生成的n(Cl2)<1mol;
B.n(MnO2)=$\frac{87g}{8g/mol}$=1mol,由于浓盐酸足量,生成的n(Cl2)=1mol,所以所得C12 的物质的量的关系,A<B,
故答案为:<;
(5)氯化氢极易溶于水,氯气能溶于水,且与水反应,Cl2+H2O=H++Cl-+HClO,食盐水溶液中的氯离子抑制氯气的溶解,降低氯气的溶解度,
故答案为:除去挥发出的HCl气体,抑制C12在水中的溶解;
(6)氯气是有毒的气体,氢氧化钠溶液和氯气反应,所以可用氢氧化钠溶液吸收多余的氯气,防止污染空气,反应的化学方程式为:Cl2+2NaOH=NaCl+NaClO+H2O,
故答案为:Cl2+2NaOH=NaCl+NaClO+H2O;
(7)氯气为黄绿色气体,密度大于空气密度,所以当收集满氯气时,集气瓶充满黄绿色气体,观察集气瓶是否充满黄绿色气体验证,
答:集气瓶充满黄绿色气体;
点评 本题考查了氯气的实验室制法及其化学性质,题目难度中等,注意明确实验装置仪器的连接顺序为:实验发生装置→除杂装置→收集装置→尾气处理装置;还要掌握实验室制备气体的装置选择、实验除杂的方法选择及试剂作用、化学方程式的书写方法、反应现象判断等知识.


科目:高中化学 来源: 题型:推断题
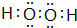 ,并指明A2C2分子中化学键的类型共价键(或极性共价键和非极性共价键).
,并指明A2C2分子中化学键的类型共价键(或极性共价键和非极性共价键).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
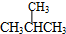 和
和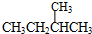 ;
;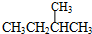 和
和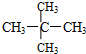 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.500 mol | B. | 1.00 mol | C. | 0.125mol | D. | 0.25 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
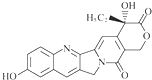
| A. | 可以与溴水反应 | |
| B. | 可以与FeCl3溶液发生显色反应 | |
| C. | 可以与浓HBr溶液反应 | |
| D. | 一定条件下,1 mol该物质最多可与1 mol NaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H6 | B. | C2H4 | C. | C3H8 | D. | C3H6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com