
【题目】下列实验装置图,其中关于用途的描述,不正确的是( )
A. 装置:收集二氧化碳,从a口进气b口排气
装置:收集二氧化碳,从a口进气b口排气
B. 装置:用于石油的分馏
装置:用于石油的分馏
C.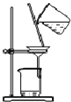 装置:用于分离Cl2与KI溶液反应生成的碘
装置:用于分离Cl2与KI溶液反应生成的碘
D. 装置:可用来制取氨气
装置:可用来制取氨气
【答案】C
【解析】
A. 二氧化碳密度比空气大;
B. 冷凝水下进上出;
C. 分离出Cl2与KI溶液反应生成的碘,碘单质易溶于有机物,在水中溶解度不大;
D. 氧化钙与水反应放热,结合氨水中存在的平衡分析。
A. 二氧化碳密度比空气大,可用向上排空气法收集,长进短出,A正确;
B. 为了充分冷凝,采用逆流原理,冷凝水下进上出,温度计水银球位于蒸馏烧瓶支管口处,测定蒸气温度,操作合理,B正确;
C. 因氧化性Cl2>I2,所以Cl2会把KI中的I-置换出来:Cl2+2KI=2KCl+I2,生成的碘能溶于水,用过滤的方法无法分离氯化钾和碘水,利用I2易溶于有机物,在水中溶解度不大,应该向其中加入CCl4或苯作萃取剂,然后再进行分液的方法,C错误;
D. 氧化钙与水反应放热,可促进一水合氨分解,产生氨气;二者反应产生的Ca(OH)2电离产生的OH-也促使平衡向产生氨气的方向移动,可用来制取氨气,D正确;
故答案选C。


科目:高中化学 来源: 题型:
【题目】现有①、②、③、④四种元素的基态原子的电子排布式如下:①![]() ;②
;②![]() ;③
;③![]() ;④
;④![]() 。则下列有关比较中不正确的是
。则下列有关比较中不正确的是
A.电负性:④>③>②>①
B.最高正化合价:③>②>①>④
C.原子半径:①>②>③>④
D.第一电离能:④>③>②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化妆品的组分 Z 具有美白功效,其原料从杨树中提取,现可用如下反应制备:
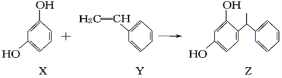
下列叙述正确的是( )
A.X、Y和Z均能使溴水褪色,且原理相同
B.只有Z中含手性碳原子
C.X和Z均能与Na2CO3溶液反应放出CO2
D.X、Y均可作加聚反应的单体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列化学用语的理解正确的是( )
A. 比例模型![]() 既可以表示甲烷分子,也可以表示四氯化碳分子
既可以表示甲烷分子,也可以表示四氯化碳分子
B. 电子式![]() H既可以表示烃基,也可以表示氢氧根离子
H既可以表示烃基,也可以表示氢氧根离子
C. 丙烯的最简式可表示为CH2
D. 结构简式(CH3)2CHCH3既可以表示正丁烷,也可以表示异丁烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A和B,只由C、H、O两种或三种元素组成,相同物质的量的A和B完全燃烧时,消耗氧气的物质的量相等,下列对A、B的判断错误的是
A.A与B互为同分异构体B.A与B的分子组成相差n个“H2O”
C.A与B的分子组成相差n个“CO2”D.A与B可能是同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下,11g CO2含有的共用电子对数为0.5NA
B. 1mol Na分别与足量的O2反应生成Na2O或Na2O2,失去的电子数均为NA
C. 通常状况下,39 g Na2O2固体中含有的离子总数为2NA
D. 滴加到沸水中的FeCl3溶液有5.6 g Fe3+发生水解,则生成的胶粒数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示的实验,能达到实验目的的是
A | B | C | D |
|
|
|
|
验证化学能转化为电能 | 研究催化剂对化学反应速率的影响 | 实验室制氨气 | 验证非金属性:Cl>C>Si |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。CO2可转化成有机物实现碳循环。在体积为1L的密闭容器中,充入 1mol CO2和3mol H2,一定条件下反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如下图所示。
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如下图所示。
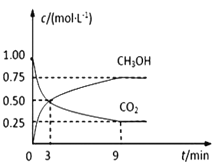
(1)从3 min到9 min,υ(H2)=________;
(2)能说明上述反应达到平衡状态的是____________(填编号)。
A.反应中CO2与CH3OH的物质的量浓度之比为1∶1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3mol H2,同时生成1mol H2O
D.CO2的体积分数在混合气体中保持不变
(3)平衡时CO2的转化率为______________。
(4)平衡时混合气体中CH3OH(g)的体积分数是__________________。
(5)一定温度下,第9分钟时υ逆(CH3OH) _______(填“大于”、“小于”或“等于”)第3分钟时υ正(CH3OH)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知室温时,0.1 molL-1某一元酸HA的电离平衡常数约为1×10-7,下列叙述错误的是
A.该溶液的pH=4
B.此溶液中,HA约有0.1%发生电离
C.由HA电离出的c(H+)约为水电离出的c(H+)的106倍
D.加水稀释,HA的电离平衡向右移动,HA的电离平衡常数增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com