
【题目】中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。CO2可转化成有机物实现碳循环。在体积为1L的密闭容器中,充入 1mol CO2和3mol H2,一定条件下反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如下图所示。
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如下图所示。
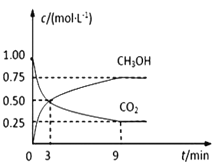
(1)从3 min到9 min,υ(H2)=________;
(2)能说明上述反应达到平衡状态的是____________(填编号)。
A.反应中CO2与CH3OH的物质的量浓度之比为1∶1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3mol H2,同时生成1mol H2O
D.CO2的体积分数在混合气体中保持不变
(3)平衡时CO2的转化率为______________。
(4)平衡时混合气体中CH3OH(g)的体积分数是__________________。
(5)一定温度下,第9分钟时υ逆(CH3OH) _______(填“大于”、“小于”或“等于”)第3分钟时υ正(CH3OH)。
【答案】0.125mol·L-1·min-1 D 75﹪ 30﹪ 小于
【解析】
(1)3min到9min,根据CO2浓度变化计算CO2化学反应速率,利用计量数之比得到v(H2);
(2)化学反应达到平衡状态时正逆反应速率相等,各物质的浓度不变,由此衍生的物理量不变;
(3)由图象可知平衡时CO2为0.25mol/L,可知消耗0.75mol/L,以此计算转化率;
(4)结合各物质的平衡浓度,利用三段式法计算;
(5)第9分钟时达到平衡,υ逆(CH3OH)=υ正(CH3OH),随着反应的进行,正反应速率逐渐减小.
(1)3min到9min,CO2浓度变化为0.5mol/L0.25mol/L=0.25mol/L,CO2反应速率为:0.25mol/L÷(9min3min)=0.256mol/(Lmin),v(H2)=3×v(CO2)=0.125mol/(Lmin),
故答案为0.125 mol/(Lmin);
(2)A.反应中CO2与CH3OH的物质的量浓度之比为1:1(即图中交叉点),浓度相等而不是不变,故A错误;
B. 反应前后,气体质量不变,容器体积不变,则气体密度始终不变,不能判断是否平衡,故B错误;
C. 单位时间内每消耗3molH2,同时生成1molH2O,从反应开始到平衡始终相等,不一定平衡,故C错误;
D. CO2的体积分数在混合气体中保持不变,说明正逆反应速率相等,达平衡状态,故D正确;
故答案为D;
(3)由图象可知平衡时CO2的为0.25mol/L,可知消耗0.75mol/L,则转化率为0.75×100%=75%,
故答案为75%;
(4) CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
起始(mol/L):1 3 0 0
转化(mol/L):0.75 2.25 0.75 0.75
平衡(mol/L):0.25 0.75 0.75 0.75
则平衡时混合气体中CH3OH(g)的体积分数为0.75÷(0.25+0.75+0.75+0.75)×100%=30%,
故答案为30%;
(5)第9分钟时达到平衡,υ逆(CH3OH)=υ正(CH3OH),随着反应的进行,正反应速率逐渐减小,则第9分钟时υ逆(CH3OH)小于第3分钟时υ正(CH3OH).,
故答案为小于。


 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.仅用![]() 溶液便可鉴别亚硝酸钠和食盐
溶液便可鉴别亚硝酸钠和食盐
B.重结晶时,溶液冷却速度越慢得到的晶体颗粒越大
C.乙酸与乙醇的混合液可用分液漏斗进行分离
D.可用![]() 的高锰酸钾溶液检验火柴燃烧后生成的气体中是否含有
的高锰酸钾溶液检验火柴燃烧后生成的气体中是否含有![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置图,其中关于用途的描述,不正确的是( )
A. 装置:收集二氧化碳,从a口进气b口排气
装置:收集二氧化碳,从a口进气b口排气
B. 装置:用于石油的分馏
装置:用于石油的分馏
C.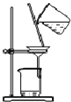 装置:用于分离Cl2与KI溶液反应生成的碘
装置:用于分离Cl2与KI溶液反应生成的碘
D. 装置:可用来制取氨气
装置:可用来制取氨气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在3个容积均为![]() 的恒容密闭容器中反应2H2(g)+CO(g)
的恒容密闭容器中反应2H2(g)+CO(g) ![]() CH3OH(g)达到平衡,下列说法正确的是 ( )
CH3OH(g)达到平衡,下列说法正确的是 ( )

A.该反应的正反应是吸热反应
B.达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的小
C.达到平衡时,容器Ⅱ中平衡常数小于容器Ⅲ中平衡常数
D.达到平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酰氯![]() 可用作杀虫剂,通常条件下为无色液体,熔点为
可用作杀虫剂,通常条件下为无色液体,熔点为![]() ,沸点为
,沸点为![]() 。在潮湿空气中“发烟”;
。在潮湿空气中“发烟”;![]() 以上开始分解,生成二氧化硫和氯气,长期放置也可分解,制备时以活性炭为催化剂,反应的热化学方程式为
以上开始分解,生成二氧化硫和氯气,长期放置也可分解,制备时以活性炭为催化剂,反应的热化学方程式为![]()
![]() ,所用装置如图所示。下列叙述错误的是
,所用装置如图所示。下列叙述错误的是![]()

A.球形冷凝管B应从a口进水b口出水
B.可通过观察D和E中气泡产生速率控制通入A中的![]() 和
和![]() 的体积比
的体积比
C.仪器C,D,E中盛放的试剂依次为无水氯化钙、浓硫酸、浓硫酸
D.长期放置的硫酰氯液体会发黄的原因是溶解了氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠俗称保险粉,可用于照相业作定影剂、纸浆漂白作脱氯剂等。实验室用SO2通入Na2S和Na2CO3的混合溶液中来制备硫代硫酸钠。本实验对Na2S纯度要求较高,利用项图所示的装置可将工业级的Na2S提纯。已知Na2S常温下微溶于酒精,加热时溶解度迅速增大,杂质不溶于酒精。提纯过程为:将已称量好的工业级Na2S放入圆底烧瓶中,加入一定质量的酒精和少量水。按下图所示装配所需仪器,向冷凝管通入冷却水,同时水浴加热。待烧瓶中固体不再减少时,停止加热。将烧瓶取下,立即趁热过滤,再冷却结晶,过滤。将所得固体洗涤、干燥,得到Na2S9H2O晶体。
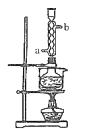
(1)下列说法不正确的是______。
A.将晶体转移至布氏漏斗时,若器壁上粘有少量晶体,应用冷水淋洗
B.抽滤时,为防止滤纸穿孔,可适当关小水龙头或多加一层滤纸
C.洗涤时,可用一定浓度的乙醇溶液洗涤晶体,目的是洗除晶体表面的杂质,易于得到干燥晶体
D.为加快产品的干燥,可高温烘干
E.在提纯过程中“趁热过滤”操作的目的是防止硫化钠结晶析岀而损失、去除杂质
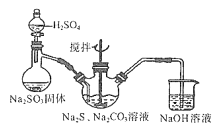
(2)用下图所示装置制取Na2S2O3,其中盛放Na2SO3固体的玻璃仪器名称是______,三颈烧瓶中发生反应的化学方程式______。
(3)保险粉样品中Na2S2O35H2O的纯度(质量分数)可通过氧化还原滴定法测定,相关反应方程式为2Na2S2O3+I2=2NaI+Na2S4O6,准确称取Wg样品于锥形瓶中,用适量蒸馏水溶解,并滴加淀粉溶液作指示剂。用0.1000mol/L碘的标准溶液进行滴定。请回答:
①到达滴定终点的标志______;
②滴定起始和终点的液面位置如图,则消耗碘的标准溶液体积为______,产品的纯度为______(设Na2S2O35H2O相对分子质量为M)。

③若滴定时振荡不充分,刚看到溶液局部变色就停止滴定,则会使样品中Na2S2O35H2O的纯度的测量结果______(“偏高”、“偏低”或“不变”)。
(4)某研究小组以硫代硫酸钠与硫酸反应来探究外界条件对反应速率的影响,设计实验如下:
实验 编号 | 实验温度 /℃ | Na2S2O3 | H2SO4 | 蒸馏水体积 /mL | ||
体积/mL | 浓度/mol/L | 体积/mL | 浓度/mol/L | |||
① | 25 | 10 | 0.1 | 10 | 0.1 | 0 |
② | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
③ | 25 | 5 | 0.2 | 10 | 0.2 | 5 |
④ | 50 | 5 | 0.1 | 10 | 0.1 | 5 |
⑤ | 50 | 10 | 0.2 | 5 | 0.2 | 5 |
下列有关说法不正确的是______。
A.该同学在实验中采用的研究方法是实验比较法
B.实验①和②探究其他条件不变时Na2S2O3浓度对相关反应速率的影响
C. 实验①和③溶液变浑浊的时间相同
D.其他条件不变时,探究温度对化学反应速率的影响,应选择实验③和实验⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用浓度为0.1000 mol·L-1的NaOH溶液滴定20.00 mL浓度均为0.1000 mol·L-1的三种酸HX、HY、HZ,滴定曲线如图所示。下列说法正确的是
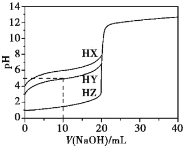
A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ<HY<HX
B.根据滴定曲线,可得Ka(HY)≈10—5
C.若将0.1000 mol·L-1酸HX加水稀释,其溶液中c(H+)·c(X-)增大
D.HY与HZ混合,达到平衡时:c(H+)=![]() + c(Z-)+c(OH-)
+ c(Z-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应C(s)+H2O(g)![]() CO(g)+H2(g)在一个体积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
CO(g)+H2(g)在一个体积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
①增加固体碳的量 ②保持压强不变,充入Ar使体系体积增大
②将容器压缩体积 ④保持体积不变,充入Ar使体系压强增大
A. ①③B. ①④C. ①②D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.氨水加水稀释后,溶液中c(NH3H2O)/c(NH4+)的值减小,c(H+)增大
B.因为合金在潮湿的空气中易形成原电池,所以合金耐腐蚀性都较差
C.一定温度下,增大反应2BaO2(s)![]() 2BaO(s)+O2(g)容器的体积,平衡不移动
2BaO(s)+O2(g)容器的体积,平衡不移动
D.反应TiO2(s) + 2Cl2(g)=TiCl4(g) + O2(g) ΔH>0能自发进行,其原因是ΔS>0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com