
【题目】诺卜醇可用于调制木香型化妆品及皂用香精,诺卜醇的一种制备方法如图所示。下列说法正确的是( )
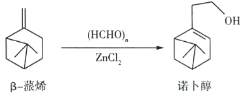
A.可用溴的![]() 溶液区别β-蒎烯与诺卜醇
溶液区别β-蒎烯与诺卜醇
B.β-蒎烯的饱和碳原子上的一氯代物最多有7种
C.β-蒎烯和诺卜醇分子中都有一个由5个碳原子构成的四面体
D.可用酸性高锰酸钾溶液鉴别β-蒎烯和诺卜醇
科目:高中化学 来源: 题型:
【题目】三氯硅烷(SiHCl3)在空气中极易燃烧,易与水反应生成两种酸,主要用于生产多晶硅、硅油等,熔点为-134℃、沸点为31.8℃。已知氯化氢气体在加热条件下可与单质硅反应得到三氯硅烷,某同学利用如图装置制备一定量的三氯硅烷(加热装置均省略)。
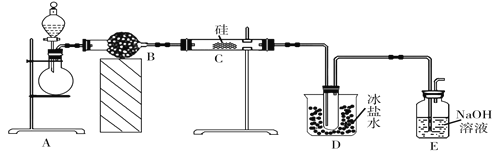
(1)制备HCl气体的方法之一是将浓硫酸与浓盐酸混合,下列性质与制备原理无关的是______(填字母),B装置的作用是_________________,冰盐水的作用是_________________
A.浓硫酸具有脱水性 B.浓硫酸具有吸水性
C.盐酸具有挥发性 D.气体的溶解度随温度升高而降低
(2)实验开始后,首先要通入一段时间的HCl气体后才能对C处试剂加热,目的是:①排出装置中空气,防止硅与氧气反应,② _____________________。该套实验装置有两处明显的错误:①E中会产生倒吸,② ____________________。E装置的用途是_______________________。
(3)加热条件下,C中发生的是置换反应,相应的化学方程式为________________________。
(4)制得的SiHCl3中含有少量SiCl4(沸点为57.6℃),提纯SiHCl3采用的适宜方法为__________,收集SiHCl3时温度应控制在_____________。
(5)设计一个实验证明C中产生的气体是H2:_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿色化学对化学反应提出了“原子经济性”(原子节约) 新概念及要求。理想的原子经济性反应是原料分子中的原子全部转变成所需产物,不产生副产物,实现零排放。下列反应符合“原子经济性”要求的是( )
A.乙醇与氧气在银的催化作用下反应制备乙醛
B.乙烷与氯气反应制备氯乙烷
C.以苯和乙烯为原料,在一定条件下反应生产乙苯
D.乙醇与浓硫酸共热制备乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨是人类科学技术上的一项重大突破,反应原理为N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ·mol-1。一种工业合成氨的简式流程图如下:
2NH3(g) ΔH=-92.4 kJ·mol-1。一种工业合成氨的简式流程图如下:
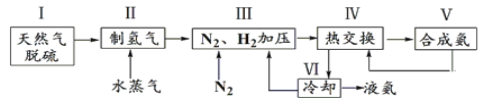
(1)①步骤Ⅱ中制氢气的原理如下:
a.CH4(g)+H2O(g)![]() CO(g)+3H2(g);K1
CO(g)+3H2(g);K1
b.CO(g)+H2O(g)![]() CO2(g)+H2(g);K2
CO2(g)+H2(g);K2
则反应CH4(g)+2H2O(g)![]() CO2(g)+4H2(g);K=___________(用含K1、K2的代数式表示)。
CO2(g)+4H2(g);K=___________(用含K1、K2的代数式表示)。
②T1温度时,对于反应:CO(g)+ H2O(g)![]() CO2(g)+ H2(g),向2 L的恒容密闭容器中通入一定量的CO和H2O(g)。若达到平衡后,反应放热Q kJ,保持其他条件不变,只是向原平衡体系中再通入0.20 mol H2O(g),则下列说法正确的是_____________。
CO2(g)+ H2(g),向2 L的恒容密闭容器中通入一定量的CO和H2O(g)。若达到平衡后,反应放热Q kJ,保持其他条件不变,只是向原平衡体系中再通入0.20 mol H2O(g),则下列说法正确的是_____________。
a.CO的转化率将增大 b.达到新平衡时的反应热ΔH > —Q
c.气体的密度将不变 d.H2O的体积分数增大
(2)将3 molH2和2 molN2充入某恒温恒压容器中,发生合成氨的反应:3H2(g) +N2(g) ![]() 2NH3(g),达平衡时NH3的浓度为c mol·L-1。保持温度不变,按下列配比分别充入该容器,平衡后NH3的浓度不为c mol·L-1的是_________。
2NH3(g),达平衡时NH3的浓度为c mol·L-1。保持温度不变,按下列配比分别充入该容器,平衡后NH3的浓度不为c mol·L-1的是_________。
a.6 molH2 + 4 molN2
b.0.75 molH2 + 0.75 molN2 + 0.5 molNH3
c.3 molH2+ 1 molN2 + 2 mol NH3
(3)H2O2作为氧化剂在反应时不产生污染物被称为绿色氧化剂,因而受到人们越来越多的关注。为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答下列问题:
①定性图甲可通过观察产生气泡的快慢的定性分析比较得出结论。有同学提出将FeCl3溶液改为Fe2(SO4)3溶液,你认为___________,(填合理或不合理)
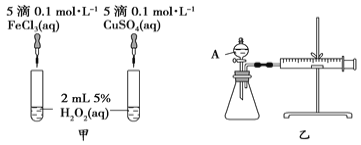
②定量如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。检查该装置气密性的方法是:关闭A的活塞,将注射器活塞向外拉出一段后松手,过一段时间后看__________,实验中需要测量的数据是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛矿工业中的硫酸酸性废水富含Ti、Fe等元素,其综合利用如下:
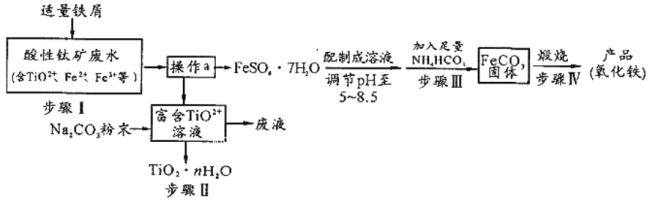
已知:TiO2+易水解,只能存在于强酸性溶液中。
(1)TiO2+钛的化合价为________________________。
(2)步骤Ⅰ中检验钛矿废水中加入铁屑是否足量的试剂是________________________。
(3)操作a是蒸发浓缩、冷却结晶、______________________________________________。
(4)步骤Ⅲ中发生反应的化学方程式为________________________;反应温度一般需控制在35℃以下,其目的是____________________________________。
(5)已知Ksp=[Fe(OH)2] = 8×10-16。步骤Ⅲ中,FeCO3达到溶解平衡时,若室温下测得溶液的pH为8.5, c(Fe2+) = 1×10-6mol/L。试判断所得的FeCO3中________(填“有”或“没有”)Fe(OH)2;步骤Ⅳ中,为了得到较为纯净的Fe2O3,除了适当的温度外,还需要采取的措施是_________________。
(6)向“富含TiO2+溶液”中加入Na2CO3粉末易得到固体TiO2 nH2O。请结合原理和化学用语解释其原因_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2 L的密闭容器中,加入1mol X(g)和2 mol Y(g)发生反应:X(g)+mY(g)![]() 3Z(g) ΔH<0,平衡时,X和Y的转化率都是10%。下列叙述不正确的是
3Z(g) ΔH<0,平衡时,X和Y的转化率都是10%。下列叙述不正确的是
A.m=2
B.达平衡时,Z的体积分数为10%
C.达平衡后,保持容器体积不变,加热,容器内压强将增大
D.将平衡后的容器体积压缩至1L,X的浓度为0.45mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①A的产量通常用来衡量一个国家的石油化工水平;②2CH3CHO+O2![]() 2CH3COOH。现以A为主要原料合成化合物E,其合成路线如图1所示。回答下列问题:
2CH3COOH。现以A为主要原料合成化合物E,其合成路线如图1所示。回答下列问题:

(1)写出下列物质的官能团名称:B:____________________;D:____________________。
(2)反应④的化学方程式为________________________________________________,反应类型:________。
(3)某学习小组设计物质B催化氧化的实验装置如下,根据图2装置回答问题。

①装置甲锥形瓶中盛放的固体药品可能为________(填字母)。
A.Na2O2 B.KClC.Na2CO3 D.MnO2
②实验过程中,丙装置硬质玻璃管中发生反应的化学方程式为_______________________________。
③物质B的催化氧化产物与葡萄糖具有相同的特征反应,将所得的氧化产物滴加到新制氢氧化铜悬浊液中加热,现象为______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物W用作调香剂、高分子材料合成的中间体等,制备W的一种合成路线如图.
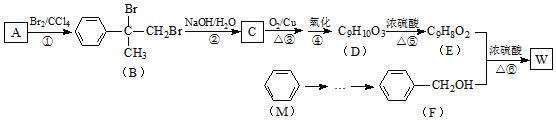
已知:![]()
![]()
![]()
![]()
![]()
请回答下列问题:
![]() 的化学名称是______,
的化学名称是______,![]() 的反应类型是______
的反应类型是______
![]() 中含有的官能团是_______
中含有的官能团是_______![]() 写名称
写名称![]() ,D聚合生成高分子化合物的结构简式为______
,D聚合生成高分子化合物的结构简式为______
![]() 反应
反应![]() 的化学方程式是______
的化学方程式是______
![]() 反应
反应![]() 的化学方程式是______
的化学方程式是______
![]() 芳香化合物N是A的同分异构体,其中核磁共振氢谱为三组峰的结构简式为______
芳香化合物N是A的同分异构体,其中核磁共振氢谱为三组峰的结构简式为______
![]() 参照有机物W的上述合成路线,设计以M为起始原料制备F的合成路线
参照有机物W的上述合成路线,设计以M为起始原料制备F的合成路线![]() 无机试剂任选
无机试剂任选![]() 示例:CH3CH2OH
示例:CH3CH2OH![]() CH2=CH2
CH2=CH2![]() BrCH2CH2Br]______
BrCH2CH2Br]______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.1 mol·L-1 CH3COOH溶液中存在如下电离平衡: CH3COOH ![]() CH3COO-+H+,对于该平衡,下列叙述正确的是( )
CH3COO-+H+,对于该平衡,下列叙述正确的是( )
A. 加入水时,平衡向逆反应方向移动
B. 加入少量NaOH固体,平衡向正反应方向移动
C. 加入少量0.1 mol·L-1 HCl溶液,溶液中c(H+)减小
D. 加入少量CH3COONa固体,平衡向正反应方向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com