
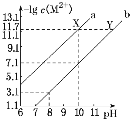
【题目】25℃时,Fe(OH)2和Cu(OH)2的饱和溶液中,金属阳离子的物质的量浓度的负对数[-lgc(M2+)]与溶液pH的变化关系如图所示,已知该温度下Ksp[Cu(OH)2]<Ksp[Fe(OH)2]。下列说法正确的是( )
A.曲线a表示Fe(OH)2饱和溶液中的变化关系
B.除去CuSO4溶液中含有的少量Fe2+,可加入适量CuO
C.当Fe(OH)2和Cu(OH)2沉淀共存时,溶液中c(Cu2+)∶c(Fe2+)=1∶104.6
D.向X点对应的饱和溶液中加入少量NaOH固体,可转化为Y点对应的溶液
【答案】C
【解析】
A. 难溶物Fe(OH)2和Cu(OH)2的构型相同,当溶液pH相同时,溶液中c(OH-)相同,固体物质的溶度积常数越小,其相应的金属阳离子浓度越小,离子浓度的负对数就越大。由于该温度下Ksp[Cu(OH)2]<Ksp[Fe(OH)2],所以c(Cu2+)<c(Fe2+),离子浓度负对数:Cu2+>Fe2+,故曲线a表示Cu(OH)2饱和溶液中的变化关系,曲线b表示Fe(OH)2饱和溶液中的变化关系,A错误;
B. 该温度下Ksp[Cu(OH)2]<Ksp[Fe(OH)2],Cu(OH)2更容易形成沉淀,所以向含有少量Fe2+的CuSO4溶液中加入适量CuO,不能形成Fe(OH)2沉淀,因而不能除去Fe2+,B错误;
C. 当溶液pH=10时,c(OH-)=10-4,此时溶液中c(Cu2+)=10-11.7,c(Fe2+)=10-7.1,溶液中c(Cu2+)∶c(Fe2+)=10-11.7:10-7.1=1∶104.6,C正确;
D. 向X点对应的饱和溶液中加入少量NaOH固体,反应产生Cu(OH)2沉淀,使溶液中c(Cu2+)降低,而根据图示可知从X点到Y点对应的溶液中金属离子浓度不变,D错误;
故合理选项是C。


科目:高中化学 来源: 题型:
【题目】在a L Fe2(SO4)3和CuSO4的混合溶液中加入b mol BaCl2,恰好使溶液中的SO42完全沉淀;如加入足量的NaOH溶液得沉淀c mol,则原溶液中的c(Fe3+)为( )
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究木炭与浓H2SO4反应的产物中是否存在CO2,某同学选用如图所示装置进行实验:
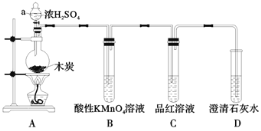
(1)组装好上述实验装置后,在装入药品之前必需的实验操作是__。
(2)写出A中发生反应的化学方程式___。
(3)装置B的作用是除去产物中的SO2,发生的反应为 MnO4-+ SO2+ H2O= Mn2++ SO42-+ H+;配平该反应方程式___,若用酸性KMnO4溶液吸收标况下22.4LSO2,则反应转移的电子数为___。
(4)装置C的作用是__。
(5)用物质的量浓度为18.4mol/L的浓硫酸配制500mL0.5mol/L的稀硫酸,主要仪器除量筒、烧杯、玻璃棒、胶头滴管外,还需要__,定容时由于仰视刻度线,则对所配溶液浓度产生的影响为__(填“偏大”,“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知伞形酮可用雷琐苯乙酮和苹果酸在一定条件下反应制得
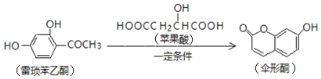
下列说法中正确的是( )
A.一分子反应物雷琐苯乙酮含有3个碳碳双键
B.苹果酸的一种缩聚产物是![]()
C.1mol产物伞形酮与足量NaOH溶液反应,最多可消耗2molNaOH
D.反应中涉及到的三种有机物都能跟FeCl3溶液发生显色反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知还原性:Fe2+>Br-。向100mLFeBr2溶液中通入3.36L(标准状况)Cl2,反应后的溶液中Cl-和Br-的物质的量浓度相等,则原溶液中FeBr2的物质的量浓度为( )
A. 2 mol·L-1 B. 1.5 mol·L-1 C. 1 mol·L-1 D. 0.75 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年5月9日,我国科学技术名词审定委员会等单位正式发布115号等4种人工合成的新元素的名称、元素符号,115号元素名称为“镆”,符号为Mc。下列有关说法正确的是
A.Mc的最低负化合价为-3B.Mc的最高价氧化物的化式为Mc2O 5
C.![]() 的中子数为115D.通过化学反应可使
的中子数为115D.通过化学反应可使![]() 转化为
转化为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨在人类的生产和生活中有着广泛的应用,某化学兴趣小组利用图一装置探究氨气的有关性质。
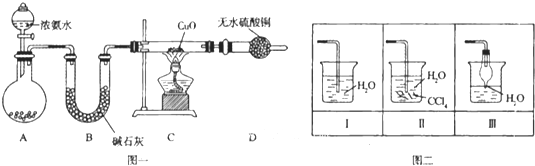
(1)装置A中烧瓶内试剂可选用 (填序号)。B的作用是
a.碱石灰 b.浓硫酸 c.生石灰 d.烧碱溶液
(2)连接好装置并检验装置的气密性后,装入药品,然后应先 (填I或Ⅱ).
Ⅰ.打开旋塞逐滴向圆底烧瓶中加入氨水 Ⅱ.加热装置C
(3)实验中观察到C中CuO粉末变红,D中无水硫酸铜变蓝,并收集到一种单质气体,则该反应相关化学方程式为 ,.该反应证明氨气具有 性.
(4)该实验缺少尾气吸收装置,图二中能用来吸收尾气的装置是 (填装置序号).
(5)氨气极易溶于水,若标准状况下,将2.24L的氨气溶于水配成0.5L溶液,所得溶液的物质的量浓度为 mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铷(![]() )是37号元素,其相对原子质量是85.5,与钠同主族,回答下列问题:
)是37号元素,其相对原子质量是85.5,与钠同主族,回答下列问题:
(1)铷位于第______周期,其原子半径比钠元素的原子半径______(填“大”或“小”)。
(2)铷单质性质活泼,写出它在氯气中燃烧的化学方程式:______。铷单质易与水反应,反应的离子方程式为______,实验表明,铷与水反应比钠与水反应______(填“剧烈”或“缓慢”)。
(3)同主族元素的同类化合物的化学性质相似,分别写出①过氧化铷与![]() 反应的化学方程式:______;②过量的
反应的化学方程式:______;②过量的![]() 与
与![]() 反应的离子方程式:______。
反应的离子方程式:______。
(4)现有铷和另一种碱金属形成的合金![]() ,当该合金与足量水反应时,可得到
,当该合金与足量水反应时,可得到![]() (标准状况下)氢气,则另一种碱金属可能是______(填序号)。
(标准状况下)氢气,则另一种碱金属可能是______(填序号)。
a ![]() b
b ![]() c
c ![]() d
d ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第四周期中的18种元素具有重要的用途,在现代工业中备受青睐。
(1)铬是一种硬而脆、抗腐蚀性强的金属,常用于电镀和制造特种钢。基态Cr原子中,电子占据最高能层的符号为__,该能层上具有的原子轨道数为__,电子数为__。
(2)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的,30Zn与31Ga的第一电离能是否符合这一规律?__(填“是”或“否”)。
(3)镓与第ⅤA族元素可形成多种新型人工半导体材料,砷化镓(GaAs)就是其中一种,其晶体结构如图所示(白色球代表As原子)。在GaAs晶体中,每个Ga原子与__个As原子相连,与同一个Ga原子相连的As原子构成的空间构型为__。
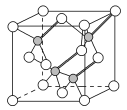
(4)与As同主族的短周期元素是N、P。AsH3中心原子杂化的类型__;一定压强下将AsH3和NH3、PH3的混合气体降温时首先液化的是__,理由是__。
(5)铁的多种化合物均为磁性材料,氮化铁是其中一种,某氮化铁的晶胞结构如图所示,则氮化铁的化学式为__;设晶胞边长为acm,阿伏加德罗常数的值为NA,该晶体的密度为__g·cm-3(用含a和NA的式子表示)。
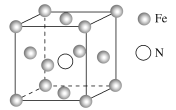
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com