
【题目】下列条件一定能使反应速率增大的是( )
① 增加反应物的物质的量 ② 升高温度 ③ 缩小反应容器的体积
④ 不断分离出生成物 ⑤加入MnO2
A.全部 B.①②⑤ C.②③ D.②
科目:高中化学 来源: 题型:
【题目】图甲表示的是H2O2分解反应过程中的能量变化。在不同温度下,分别向H2O2溶液(20g·L-1)中加入相同体积且物质的量浓度均为0.5mol·L-1的不同溶液,反应中H2O2浓度随时间的变化如图乙所示。
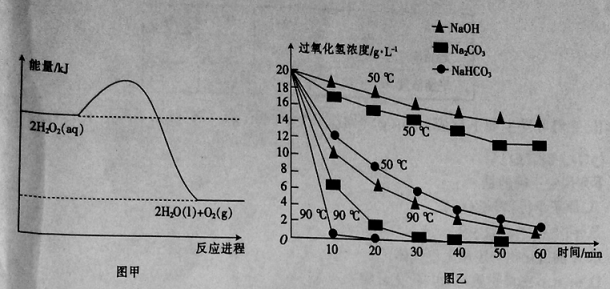
从图中得出的结论不正确的是
A.H2O2的分解反应为放热反应
B.断裂共价键所需的能量:2×E(O—O)<1×E(O=O)
C.加入相同物质时,温度越高,H2O2分解的速率越快
D.相同温度下,加入不同物质的溶液,碱性越强,H2O2分解的速率越快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道美国准备试验绿色航天推进剂-离子液体火箭推进剂AF-M315E,其主要成分是羟基硝酸铵,结构如图,它比肼燃烧释放能量更高,更安全、环保。下列说法不正确的是( )

A.羟基硝酸铵中各原子共平面
B.固态时羟基硝酸铵是离子晶体
C.羟基硝酸铵中含有离子键和共价键
D.9.6g羟基硝酸铵中含有0.2NA个离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向50mL Na2SO4和Na2CO3的混合溶液中加入过量的BaCl2溶液,得到14.51g白色沉淀,向白色沉淀中加入过量的稀HNO3,充分反应后,沉淀减少到4.66g,并有气体产生。
(1)原混合溶液中Na2SO4的物质的量浓度是多少?
(2)产生的气体在标准状况下的体积是多少?
(3)原溶液中Na+物质的量浓度是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】密闭容器中自由移动的活塞两边分别充入空气和H2、O2的混合气体,开始体积比为1:3,若将H2、O2的混合气体点燃引爆,恢复到原来温度(水为液态),活塞右滑停留于容器的正中央,则原来H2、O2的体积比可能为

A. 2:7 B. 5:4 C. 1:1 D. 7:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 1molO2的质量是32g/mol B. H2的摩尔质量是2g
C. 1molH+的质量是1g D. 对原子而言,摩尔质量就是相对原子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验对应的现象及结论均正确且两者具有因果关系的是
选项 | 实验 | 现象 | 结论 |
A | 将SO2通入BaCl2溶液, 然后滴入稀硝酸 | 白色沉淀,白色沉淀 不溶于稀硝酸 | 所得沉淀为BaSO3, 后转化为BaSO4 |
B | 浓硫酸滴入蔗糖中, 并搅拌 | 得黑色蓬松的固体并 有刺激性气味气体 | 该过程中浓硫酸仅体 现吸水性和脱水性 |
C | 向FeCl2溶液中加入足 量Na2O2粉末 | 出现红褐色沉淀和 无色气体 | FeCl2溶液部分变质 |
D | 向足量含淀粉的FeI2溶 液中滴加2滴氯水 | 溶液变蓝 | 还原性:I->Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,表中所列字母分别代表一种元素(NA为阿伏加德罗常数的值)。

(1)元素B位于元素周期表的 (填“s”、“p”或“d”)区。
(2)由A、X、K三种元素中的某两种形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质有 (填分子式)。
(3)只含A、E和镍三种元素的晶体具有超导性。该新型超导晶体的一个晶胞如图所示,该晶体的化学式为 。

(4)元素D和K形成的化合物中,每个阳离子周围距离最近且相等的阳离子有 个,若该化合物晶体的密度为a g/cm3,则晶胞的体积是 cm3。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com