
(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101 kPa时,32.0 g N2H4在氧气中完全燃烧生成氮气,放出热量624 kJ(25℃时),N2H4完全燃烧反应的热化学方程式是____________________________________________________________________。
(2)肼-空气燃料电池是一种碱性燃料电池,电解质是20%—30%的KOH溶液。写出肼-空气燃料电池放电时正、负极的电极反应式。
正极:________________________________,
负极:________________________________
(3)图2-2-5是一个电化学过程示意图。
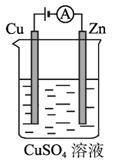
图2-2-5
①锌片上发生的电极反应是________________________________________________。
②假设使用肼?空气燃料电池作为本过程中的电源、铜片的质量变化128 g,则肼-空气燃料电池理论上消耗标标准状况下的空气___________L(假设空气中氧气体积含量为20%)
(4)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液。该反应的离子方程式是________________________________________。
解析:(1)注意32 g N2H4为1 mol,且ΔH应与化学方程式的计量数相对应。
(2)肼-空气燃料电池的电解质是KOH溶液,故电极反应为:正极:O2+2H2O+4e-====4OH-,负极:N2H4+4 OH--4e-====4H2O+N2↑。
(3)①此图为电解装置,铜片为阳极,锌片为阴极。故锌片上发生的电极反应是Cu2++2e-====Cu。②铜片减少128 g,即转移电子4 mol,根据O2+2H2O+4e-====4 OH-计算得,需要氧气1 mol,转化为空气则需要112 L(标况下)。
(4)依据氧化还原反应的规律,得到ClO-+2NH3====N2H4+Cl-+H2O。
答案:(1)N2H4(l)+O2(g)====N2(g)+2H2O(l);ΔH=-624 kJ·mol-1
(2)O2+2H2O+4e-====4OH
N2H4+4 OH--4e-====4H2O+N2↑
(3)①Cu2++2e-====Cu ②112
(4)ClO-+2NH3====N2H4+Cl-+H2O


 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案科目:高中化学 来源: 题型:
(2)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%-30%的KOH溶液。
肼-空气燃料电池放电时:
正极的电极反应式是____________________________________。
负极的电极反应式是____________________________________。
(3)下图是一个电化学过程示意图。

①锌片上发生的电极反应式是____________________________________。
②假设使用肼-空气燃料电池作为本过程中的电源,铜片的质量变化
(4)传统制备肼的方法,是以NaClO氧化NH3制得肼的稀溶液。该反应的离子方程式是____________________________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年黑龙江省高二上学期期中化学试卷(解析版) 题型:填空题
(8分)(1)肼(N2H4)是发射航天飞船常用的高能燃料。将NH3和NaClO按一定物质的量比混合反应,生成肼、NaCl和水,该反应的化学方程式是_____________________________。
(2)在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂过氧化氢,当它们混合时,即产生大量气体,并放出大量热。已知:H2O(l) H2O(g) ΔH= +44 kJ/mol。12.8 g液态肼与足量过氧化氢反应生成氮气和水蒸气,放出256.65 kJ的热量。
①请写出液态肼与过氧化氢反应生成液态水的热化学方程式______________________。
②则16 g 液态肼与足量过氧化氢反应生成液态水时放出的热量是___________________。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年福建省厦门市高三下学期期初考试化学试卷 题型:填空题
(10分)、Ⅰ:(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是 。
(2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%一30%的KOH溶液。肼—空气燃料电池放电时:正极的电极反应式是 。
Ⅱ:探究家庭制备次氯酸钠溶液的发生器如右图,原理是用石墨做电极电解饱和食盐水。
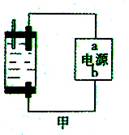
(1)若通电后,为使氯气被全部吸收,则电源的a极的名称是 。
(2)电解饱和食盐水的离子方程式为 ,所得的次氯酸钠溶液中加入几滴石蕊试液,观察到的现象是 ,
用离子方程式和简要文字说明理由 。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年山东省德州市高三上学期期末考试化学试卷 题型:填空题
(10分)
1:(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是 。
(2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%一30%的KOH溶液。肼—空气燃料电池放电时:正极的电极反应式是 。
Ⅱ:探究家庭制备次氯酸钠溶液的发生器如图,原理是用石墨做电极电解饱和食盐水。
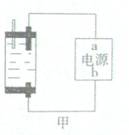
(1)若通电后,为使氯气被全部吸收,则电源的a极的名称是 。
(2)电解饱和食盐水的离子方程式为 ,所得的次氯酸钠溶液中加入几滴石蕊试液,观察到的现象是 ,用离子方程式和简要文字说明理由 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com