现有A、B、C、D四种短周期元素,A元素的原子半径是除稀有气体外半径最大的,B元素的原子最外层比次外层多3个电子,C元素是人体中质量分数最大的,D元素的一种核素质量数与质子数相等.请据此填空:
(1)A的原子结构示意图______;B2分子的电子式______.
(2)C元素常见单质的化学式为______、______.
(3)A与B形成的一种化合物中,A元素的质量分数为35.4%,该化合物的摩尔质量不超过70g?mol-1,则该化合物的化学式是______,其中可能有的化学键为______.
【答案】
分析:A、B、C、D四种短周期元素,A元素的原子半径是除稀有气体外半径最大的,则A为Na;B元素的原子最外层比次外层多3个电子,两个电子层符合电子排布规律,则B为N;C元素是人体中质量分数最大的,则C为O;D元素的一种核素质量数与质子数相等,H元素的一种核素氕符合,即D为H,以此来解答.
解答:解:A、B、C、D四种短周期元素,A元素的原子半径是除稀有气体外半径最大的,则A为Na;B元素的原子最外层比次外层多3个电子,两个电子层符合电子排布规律,则B为N;C元素是人体中质量分数最大的,则C为O;D元素的一种核素质量数与质子数相等,H元素的一种核素氕符合,即D为H,
(1)Na的原子结构中有3个电子层,最外层电子数为1,则原子结构示意图为
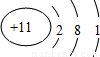
,N的最外层电子数为5,则N
2的电子式为

,
故答案为:
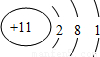
;

;
(2)氧元素形成的常见单质为O
2、O
3,故答案为:O
2;O
3;
(3)设化学式为Na
xN
y,则23x+14y≤70,
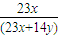
=35.4%,解得y≤3.2,
则x=1、y=3符合,所以化学式为NaN
3,该物质中N、N之间以共价键结合,钠离子与阴离子之间以离子键结合,
故答案为:NaN
3;离子键、共价键.
点评:本题考查原子结构与元素周期律,熟悉原子结构、元素的性质及元素形成的常见的单质、元素的常见核素、化学键等知识即可解答,难度不大.

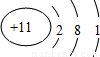 ,N的最外层电子数为5,则N2的电子式为
,N的最外层电子数为5,则N2的电子式为 ,
,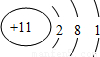 ;
; ;
;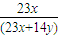 =35.4%,解得y≤3.2,
=35.4%,解得y≤3.2,
