
| A、可以利用BaCl2溶液来区分碳酸钾溶液和硫酸钾溶液 |
| B、22.4LO2中一定含有6.02×1023个氧分子 |
| C、在相同温度和压强下,相同体积的任何气体都含有相同数目的粒子 |
| D、0.5 molNaCl溶于0.5L水中得到的溶液的浓度是1.0mol/L |
| V |
| Vm |
| N |
| NA |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
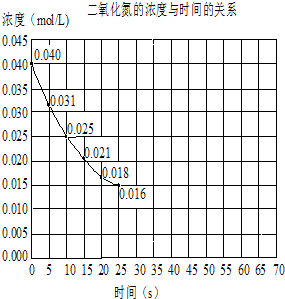 二氧化氮在加热条件下能够分解成一氧化氮和氧气.该反应进行到45s时,达到平衡NO2浓度约为0.0125mol/L.如图中的曲线表示二氧化氮分解反应在前25s内的反应进程.
二氧化氮在加热条件下能够分解成一氧化氮和氧气.该反应进行到45s时,达到平衡NO2浓度约为0.0125mol/L.如图中的曲线表示二氧化氮分解反应在前25s内的反应进程.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用酚酞溶液鉴别稀盐酸和稀氢氧化钠溶液 |
| B、用燃着的木条鉴别CO2和O2 |
| C、用稀硫酸鉴别锌片和铜片 |
| D、用加水溶解的方法即可鉴别食盐和白糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用激光笔检验某KI溶液中是否溶有淀粉 |
| B、配制一定物质的量浓度溶液时,容量瓶用蒸馏水洗涤后再用待装溶液润洗 |
| C、向AgCl沉淀中滴加少量KI溶液,可说明Ksp(AgCl)<Ksp(AgI) |
| D、配制硫酸亚铁溶液,是将绿矾晶体溶于蒸馏水再加入一定量的铁粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用淀粉溶液鉴别NaBr、KI溶液 |
| B、用KMnO4酸性溶液鉴别CH4、C2H4气体 |
| C、用AgNO3溶液鉴别Na2SO4、NaCl溶液 |
| D、用澄清石灰水鉴别Na2CO3、NaHCO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCl |
| B、MgSO4 |
| C、CuSO4 |
| D、NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
. |
| M |
A、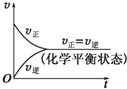 |
B、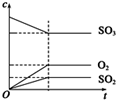 |
C、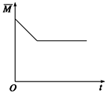 |
D、 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com