
【题目】芳香族化合物A(C9H12O)常用于药物及香料的合成,A有如下转化关系:
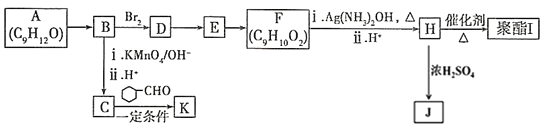
已知:①A的苯环上只有一个支链,支链上有两种不同环境的氢原子;
②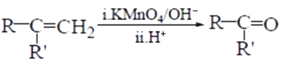 +CO2
+CO2
③RCOCH3+R′CHO![]() RCOCH=CHR″+H2O
RCOCH=CHR″+H2O
回答下列问题:
(1)A生成B的反应条件为______,由D生成E的反应类型为__________。
(2)C中所含官能团的名称为______,K的分子式为________。
(3)由E生成F的化学方程式为________。
(4)I的结构简式为_______,J为一种具有3个六元环的酯,1 mol J生成的同时生成______mol H2O。
(5)F的同分异构体中,属于芳香族化合物且能发生水解反应和银镜反应的有____种,其中核磁共振氢谱为4组峰,且峰面积比为6:2:1:1的为_______(写出其中一种结构简式)。
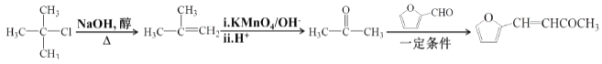
(6)糠叉丙酮(![]() )是一种重要的医药中间体,请参考上述合成路线,设计一条由(CH3)3CCl和
)是一种重要的医药中间体,请参考上述合成路线,设计一条由(CH3)3CCl和 ![]() 为原料制备糠叉丙酮的合成路线(无机试剂任用)_______。合成流程图示例如下:
为原料制备糠叉丙酮的合成路线(无机试剂任用)_______。合成流程图示例如下:![]()
【答案】浓硫酸、加热 取代反应(水解反应) 酮基(羰基) C15H12O 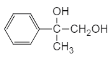 +O2
+O2![]()
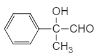 +2H2O
+2H2O 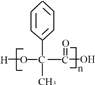 2 14
2 14
 或
或
【解析】
芳香族化合物A的分子式为C9H12O,其不饱和度为4,说明侧链上均为饱和碳原子,A的苯环上只有一个支链,支链上有两种不同环境的氢原子,则A为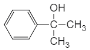 ,B可以与溴反应,能被碱性高锰酸钾氧化,可以推测A发生消去反应生成B,则B为
,B可以与溴反应,能被碱性高锰酸钾氧化,可以推测A发生消去反应生成B,则B为![]() ,则被碱性高锰酸钾氧化再酸化的产物C为
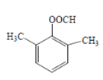
,则被碱性高锰酸钾氧化再酸化的产物C为![]() ,C与苯甲醛发生类似信息③的反应生成的K为
,C与苯甲醛发生类似信息③的反应生成的K为![]() ;B与溴发生加成反应生成D为
;B与溴发生加成反应生成D为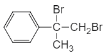 ,根据F生成H的反应条件可知F中含有醛基,所以E生成F应为羟基的催化氧化,所以D发生水解反应生成E为
,根据F生成H的反应条件可知F中含有醛基,所以E生成F应为羟基的催化氧化,所以D发生水解反应生成E为 ,F为
,F为 (该羟基相连的碳原子上没有氢原子,不能被氧化);F中醛基被银氨溶液氧化再酸化生成H为
(该羟基相连的碳原子上没有氢原子,不能被氧化);F中醛基被银氨溶液氧化再酸化生成H为 ;H同时含有羟基和羧基,脱水缩合生成高分子化合物I为
;H同时含有羟基和羧基,脱水缩合生成高分子化合物I为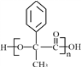 ;J为一种具有3个六元环的酯,应为两分子H发生酯化生成,J为
;J为一种具有3个六元环的酯,应为两分子H发生酯化生成,J为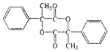 。
。
(1)A生成B为羟基的消去反应,反应条件为浓硫酸、加热;D中溴原子被羟基代替生成E,属于取代反应(水解反应);
(2)C为![]() ,其官能团为(酮基)羰基;K为
,其官能团为(酮基)羰基;K为![]() ,其分子式为C15H12O;
,其分子式为C15H12O;
(3)E发生催化氧化生成F,化学方程式为 +O2
+O2![]() 2
2 +2H2O;
+2H2O;
(4)根据分析可知I为 ;两分子H发生酯化生成J,J的结构简式为
;两分子H发生酯化生成J,J的结构简式为 ,所以1molJ生成的同时会生成2molH2O;
,所以1molJ生成的同时会生成2molH2O;
(5)F为 ,其同分异构体中,属于芳香族化合物且能发生水解反应和银镜反应说明含有苯环和甲酸形成的酯基,当有一个取代基时,取代基可以是:—CH2CH2OCHO、—CH(CH3)OCHO共2种;有2个取代基时,取代基可以是:—OCHO和—CH2CH3、—CH2OCHO和—CH3,每一组都有邻间对3种结构,共6种;有3个取代基时,取代基可以是:2个—CH3和—OCHO,有6种,所以共有2+6+6=14种同分异构体;其中核磁共振氢谱为4组峰,且峰面积比为6:2:1:1的为
,其同分异构体中,属于芳香族化合物且能发生水解反应和银镜反应说明含有苯环和甲酸形成的酯基,当有一个取代基时,取代基可以是:—CH2CH2OCHO、—CH(CH3)OCHO共2种;有2个取代基时,取代基可以是:—OCHO和—CH2CH3、—CH2OCHO和—CH3,每一组都有邻间对3种结构,共6种;有3个取代基时,取代基可以是:2个—CH3和—OCHO,有6种,所以共有2+6+6=14种同分异构体;其中核磁共振氢谱为4组峰,且峰面积比为6:2:1:1的为 和
和 ;
;
(6)根据信息③的反应可知![]() 可以由
可以由![]() 和
和![]() 在一定条件下反应生成,而
在一定条件下反应生成,而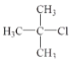 可以发生消去反应生成
可以发生消去反应生成![]() ,继而发生信息②的反应可以转化为
,继而发生信息②的反应可以转化为![]() ,所以合成路线为
,所以合成路线为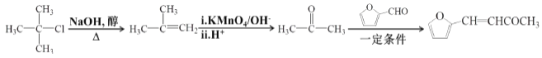 。
。


科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是![]()
![]()
①质子数相同的微粒一定属于同一种元素![]()
②同位素的性质相同![]()
③质子数相同、电子数也相同的微粒,不可能是一种分子和一种离子![]()
④电子数相同的微粒不一定是同一种元素![]()
⑤一种元素只能有一种质量数![]()
⑥某种元素的相对原子质量取整数,就是其质量数![]()
⑦![]() 中
中![]() 与
与![]() 的原子个数之比与NaCl中的
的原子个数之比与NaCl中的![]() 与
与![]() 的原子个数之比相等
的原子个数之比相等
A.②③⑤⑥⑦B.①②④⑤C.①②⑤⑥D.③④⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】星型聚合物SPLA可经下列反应路线得到(部分反应条件未注明)。

已知:SPLA的结构简式为: ,其中R为
,其中R为 。
。
(1)淀粉是___糖(填“单”或“多”);A的名称是___。
(2)生成D的化学反应类型属于___反应;D结构中有3个相同的基团,且1 mol D能与2 mol Ag(NH3)2OH溶液反应,则D的结构简式是___;D→E反应的化学方程式为___。
(3)B的直链同分异构体G的分子中不含甲基,G既不能与NaHCO3溶液反应,又不能与新制Cu(OH)2悬浊液反应,且1mol G与足量Na反应生成1 mol H2,则G的结构简式为___。
(4)B有多种脱水产物,其中两种产物的结构简式为______和______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(ClNO)常用作催化剂和合成洗涤剂,某学习小组在实验室中用下图所示装置制备ClNO。查阅资料:亚硝酰氯(ClNO)的熔点为-64.5℃、沸点为-5.5℃,气态呈黄色,液态时呈红褐色,遇水易反应生成一种氢化物和两种氮的常见氧化物,其中一种呈红棕色。
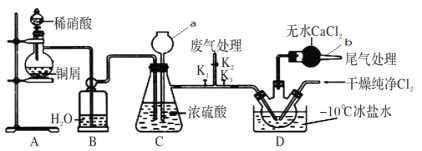
回答下列问题:
(1)仪器a的名称为________,b的作用是________。
(2)ClNO分子中各原子均满足8电子稳定结构,则ClNO的电子式为__________;ClNO与水反应的化学方程式为__________。
(3)实验开始时,先打开K1、K2,关闭K3,再打开分液漏斗活塞滴入适量稀硝酸,当观察到C中_________________时关闭K1、K2;向装置D三颈瓶中通入干燥纯净Cl2,当瓶中充满黄绿色气体时,再打开K1、K3,制备ClNO,D中发生的反应方程式为________。
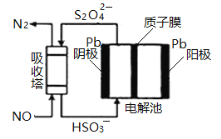
(4)NO可用间接电化学法除去,其原理如下图所示。电解池阴极的电极反应式为________;吸收塔内发生的离子方程式为_______。
(5)亚硝酰氯(ClNO)纯度的测定:将所得亚硝酰氯(ClNO)产品13.10g溶于水,配制成250mL溶液;取出25.00mL,以K2CrO4溶液为指示剂,用0.87mol·L-1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为 20.00mL。(已知:Ag2CrO4为砖红色固体),则亚硝酰氯(ClNO)的质量分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钒(23V)是我国的丰产元素,广泛用于催化及钢铁工业。回答下列问题:
(1)钒在元素周期表中的位置为_______,其价层电子排布图为____________。
(2)钒的某种氧化物的晶胞结构如图1所示。晶胞中实际拥有的阴、阳离子个数分别为____、_____。
(3)V2O5常用作SO2转化为SO3的催化剂。SO2分子中S原子价层电子对数是__对,分子的立体构型为___;SO3气态为单分子,该分子中S原子的杂化轨道类型为____;SO3的三聚体环状结构如图2所示,该结构中S原子的杂化轨道类型为___;该结构中S—O键长有两类,一类键长约140pm,另一类键长约为160pm,较短的键为__(填图2中字母),该分子中含有___个σ键。

(4)V2O5溶解在NaOH溶液中,可得到钒酸钠(Na3VO4),该盐阴离子的立体构型为___;也可以得到偏钒酸钠,其阴离子呈如图3所示的无限链状结构,则偏钒酸钠的化学式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某离子晶体的晶胞示意图如图所示,其摩尔质量为Mg/mol,阿伏加德罗常数的值为NA,晶体的密度为dg/cm3下列说法中正确的是
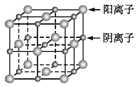
A.晶体晶胞中阴、阳离子的个数都为1
B.晶体中阴、阳离子的配位数都是4
C.该晶胞可能是NaCl的晶胞
D.该晶体中两个距离最近的阳离子的核间距为4M/(NAd)cm
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机物分子的叙述不正确的是( )
A. 乙烯分子中有一个sp2-sp2σ键和一个p-p π键
B. 乙炔每个碳原子都有两个未杂化的2p轨道,它们之间可形成两个π键
C. 乙烷两个C原子均是sp3杂化,分子中一共有6个σ键
D. 苯分子每个碳原子均是sp2杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中发生反应:xA(g)+yB(g)![]() zC(g),平衡时测得A的浓度为0.50mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度0.30mol/L。下列有关判断正确的是( )
zC(g),平衡时测得A的浓度为0.50mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度0.30mol/L。下列有关判断正确的是( )
A.x+y<z
B.平衡向正反应方向移动
C.A的转化率降低
D.C的体积分数增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com