
| ���ӷ��� | K+ | SO42- | Cl- |
| ���ʵ���Ũ�ȣ�mol?L-1�� | 9.0 | 4.0 | 9.0 |

| n |
| V |
| n |
| c |
| n |
| V |
| n |
| c |
| n |
| c1 |
| 1.6mol |
| 8.0mol/L |
| n |
| c2 |
| 1.6mol |
| 1.6mol/L |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����������ƹ��������ֽ�ϳ��� |
| B����100 mL��Ͳ��ȡ8.5 mL����ˮ |
| C����ȡ����ʱ���ö���������Ũ�����ڳ����·�Ӧ��������ˮ�������ռ� |
| D�������Ȼ�����Һʱ����һ�����Ȼ����ܽ��ڽ�Ũ�������У�����ˮϡ�͵�����Ũ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Ư�� | B������ |
| C��ˮ���� | D��̼���Ʒ�ĩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �����£���l00mL 0.01mol?L-1HA��Һ����μ���0.02mol??L-1MOH��Һ����ͼ����ʾ���߱�ʾ�����Һ��pH�仯�������Һ����仯���Բ��ƣ�������˵���У���ȷ���ǣ�������
�����£���l00mL 0.01mol?L-1HA��Һ����μ���0.02mol??L-1MOH��Һ����ͼ����ʾ���߱�ʾ�����Һ��pH�仯�������Һ����仯���Բ��ƣ�������˵���У���ȷ���ǣ�������| A��HAΪһԪǿ�ᣬMOHΪһԪǿ�� |
| B��K����ʾ��Һ��c��A-����c��M+�� |
| C��N��ˮ�ĵ���̶�С��K��ˮ�ĵ���̶� |
| D��K���Ӧ����Һ��pH=10������c��MOH��+c��OH-��-c��H+��=0.005mol??L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ������CO2������������˵��µ�������¶������⣬����Ӱ�캣����̬������ij�о�С����ʵ���Ҳ�ò�ͬ�¶��£�T1��T2����ˮ��CO32-Ũ����ģ�������CO2Ũ�ȵĹ�ϵ���ߣ�����˵������ȷ���ǣ�������
������CO2������������˵��µ�������¶������⣬����Ӱ�캣����̬������ij�о�С����ʵ���Ҳ�ò�ͬ�¶��£�T1��T2����ˮ��CO32-Ũ����ģ�������CO2Ũ�ȵĹ�ϵ���ߣ�����˵������ȷ���ǣ�������| A��T1��T2 |
| B����ˮ�¶�һ��ʱ��������CO2Ũ�����ӣ���ˮ���ܽ��CO2��֮������CO32-Ũ�Ƚ��� |
| C����������CO2Ũ��ȷ��ʱ����ˮ�¶�Խ�ߣ�CO32-Ũ��Խ�� |
| D��������CO2��������ʱ����ˮ�е�ɺ���������ܽ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ʢ��Һ�����ƿ����ʱ����Ҫ�����Ƭ���ʯ |
| B��CCl4��ȡ��ˮ�е��ʵ�飬��Һʱ��ˮ��Ӧ�ӷ�Һ©���¿ڷų���CCl4���Ӧ�Ͽڵ��� |
| C��������ƿ������Һ������ʱ��ˮ�����˿̶��ߣ���������������� |
| D���ⶨ��ҺpHʱ��Ӧ�ø���ྻ�IJ�����պȡ��Һ����pH��ֽ�ϸ�����ɫ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 3 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����������Ũ������ȷ�Ӧ���Եõ����� |
| B��������NaAlSiO4?nH2O�ɸ�д����������ʽΪ��Na2O?Al2O3?2SiO2?2nH2O |
| C��ij��ˮ��Ʒ�ɼ������һ��ʱ�䣬pH��4.68��Ϊ4.28������Ϊˮ���ܽ��˽϶��CO2 |
| D��Al65Cu23Fe12��һ���⾧�����кϽ�������������ܣ���Ӳ�ȱȽ���A1��Cu��Fe���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
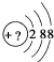 ��1�����������������������ķ�����
��1�����������������������ķ������鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com