
【题目】下列结论正确的是 ( )
①粒子半径:K>Cl>S ②氢化物稳定性:HF>H2S>PH3;
③离子还原性:S2->Cl->Br->I-④单质氧化性:Cl2>S>Si;
⑤酸性:H2SO4>HClO ⑥碱性强弱:KOH>NaOH>Mg(OH)2
A. ①④⑤ B. ③⑥ C. ②④⑤⑥ D. ①③④
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案科目:高中化学 来源: 题型:
【题目】实验室采用MgCl2、AlCl3的混合溶液与过量氨水反应制备MgAl2O4的主要流程如下:
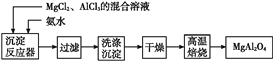
(1)制备MgAl2O4过程中,高温焙烧时发生反应的化学方程式为_____________。
(2)判断流程中沉淀是否洗净所用的试剂是__________________。
(3)在25 ℃下,向浓度均为0.01 mol·L-1的MgCl2和AlCl3混合溶液中逐滴加入氨水,先生成______沉淀(填化学式),生成该沉淀的离子方程式:_____________。{已知25 ℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Al(OH)3]=3×10-34}。
(4)无水AlCl3(183 ℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。
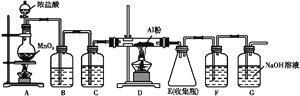
装置B中盛放饱和NaCl溶液,该装置的主要作用是______;F中试剂的作用是__________________________________________。
(5)将Mg、Cu组成的3.92 g混合物投入过量稀硝酸中,充分反应后,固体完全溶解时收集到还原产物NO气体1.792 L(标准状况),向反应后的溶液中加入4 mol·L-1的NaOH溶液80 mL时金属离子恰好完全沉淀。则形成沉淀的质量为____g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将几滴KSCN(SCN-是“类似卤离子”)溶液加入到酸性的含有Fe3+的溶液中,溶液变为红色,将该红色溶液分为两份:①向其中—份溶液中加入适量KMnO4溶液,红色褪去;②向另一份溶液中通入SO2,红色也褪去。下列说法中不正确的是
A. ①中红色褪去的原因是KMnO4将SCN-氧化,使Fe(SCN)3消失
B. ②中红色褪色的原因是SO2将Fe3+还原为Fe2+
C. ②中红色裡色的原因是SO2将SCN-还原
D. SCN-在适当条件下可失去电子被氧化剂氧化为(SCN)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】σ键可由两个原子的s轨道、一个原子的s轨道和另一个原子的p轨道以及一个原子的p轨道和另一个原子的p轨道以“头碰头”方式重叠而成.则下列分子中的σ键是由一个原子的s轨道和另一个原子的p轨道以“头碰头”方式重叠构建而成的是( )
A.H2
B.HCl
C.Cl2
D.F2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
A.在同温同压时,相同体积的任何气体单质所含的原子数目相同
B.常温常压下,32g氧气(O2)和32g臭氧(O3)都含有2NA个氧原子
C.500mL 0.2 mol/L Na2SO4溶液中含有NA个Na+离子
D.通常状况下,22.4 L的氨气和甲烷含有的电子数均为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表列出的有关物质的性质与用途具有对应关系的是
选项 | 物质的性质 | 用途 |
A | MgO难溶于水 | 耐火材料 |
B | SO2具有强的还原性 | 漂白纸张 |
C | CuSO4易溶于水 | 游冰池杀菌消毒 |
D | NaHCO3能与酸反应 | 治疗胃酸过多 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以Al(OH)3、H2SO4、工业硝酸铵(含FeSO4)为原料制备透明氧化铝陶瓷的工艺流程如下:

回答下列问题:
(1)氧化步骤中需加入稍过量的氧化剂,下列物质中最合适的是_____。
a. NaClO b.H2O2 c. KMnO4 d.K2Cr2O7
(2)选用上述氧化剂之后,需取少量溶液检验Fe2+是否己全部被氧化,所加试剂为_____(写名称)。
(3)如何检验中和液中的杂质离子己完全除尽?______________________________。
(4) 固体NH4Al(SO4)2·12H2O(相对分子质量453)在加热时,固体残留率隨温度的变化如图所示。由300℃加热至633℃时发生反应的化学方程式为_________________________________;(已知该反应为非氧化还原反应)975℃剩余固体成分的化学式为________________________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com