
| A. | 分液时,分液漏斗中的两层液体均从下口放出 | |
| B. | 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 | |
| C. | 称量NaOH固体时,将NaOH固体放在托盘天平左盘的纸上 | |
| D. | 不慎将浓碱沾到皮肤上,应立即用大量水冲洗,然后涂上硼酸溶液 |
分析 A.分液时,避免上下层液体混合;
B.蒸发溶液,不能蒸干;
C.NaOH易潮解,具有腐蚀性;
D.酸、碱都具有腐、蚀性.
解答 解:A.分液时,分液漏斗中上层液体从上口倒出,下层液体从下口流出,故A错误;
B.蒸发溶液,不能蒸干,应当出现较多固体时停止加热,利用余热加热,故B错误;
C.NaOH易潮解,具有腐蚀性,则称量NaOH固体时,将NaOH固体放在托盘天平左盘的小烧杯中,故C错误;
D.碱液沾到皮肤上,要用较多的水冲洗,再涂上硼酸溶液,不能用硫酸或盐酸冲洗,硫酸和盐酸也有腐蚀性,会造成二次伤害,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,涉及分液、蒸发、称量、危险处理等实验基本操作,侧重实验基本技能和基础知识的考查,注意实验操作的评价性、操作性分析,题目难度不大.


科目:高中化学 来源: 题型:解答题
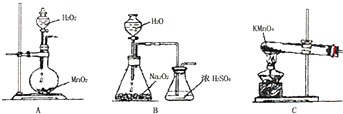
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 均为0.56 L | B. | ①=② | C. | ①>② | D. | ②>① |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
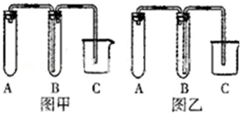 化学是一门以实验为基础的学科.
化学是一门以实验为基础的学科.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 阳离子 | Fe3+ | Fe2+ | Cu2+ |
| 开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 沉淀完全时的pH | 3.2 | 9.0 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能使甲基橙变红的溶液中:Fe2+、Al3+、NO3-、Cl-、S2- | |
| B. | 在pH=11的溶液中:Na+、AlO2-、NO3-、S2-、SO32- | |
| C. | 室温下,由水电离的c(H+)=10-10mol/L的溶液中:Cl-、HCO3-、NO3-、NH4+、F- | |
| D. | 0.1 mol•L-1 FeCl3溶液中:K+、Na+、AlO2-、SCN- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图是某学校实验室从化学试剂商店买回来的氢氧化钠试剂标签上的部分内容.某同学从该试剂瓶中取出4.0g固体,配成1L溶液,请计算:
如图是某学校实验室从化学试剂商店买回来的氢氧化钠试剂标签上的部分内容.某同学从该试剂瓶中取出4.0g固体,配成1L溶液,请计算:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com