
【题目】M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素.M基态原子L层中p轨道电子数是s电子数的2倍,R是同周期元素中最活泼的金属元素,X和M形成的一种化合物是引起酸雨的主要大气污染物,Z的基态原子4s和3d轨道半充满.请回答下列问题:
(1)R基态原子的电子排布式是 , X和Y中电负性较大的是(填元素符号).
(2)X的氢化物的沸点低于与其组成相似的M的氢化物,其原因是 .
(3)X与M形成的XM3分子的空间构型是 .
(4)M和R所形成的一种离子化合物R2M晶体的晶胞如图所示,则图中黑球代表的离子是(填离子符号).
(5)在稀硫酸中,Z的最高价含氧酸的钾盐(橙色)氧化M的一种氢化物,Z被还原为+3价,该反应的化学方程式是 .
【答案】
(1)1s22s22p63s1;Cl
(2)H2O分子能形成氢键,而H2S不能形成氢键
(3)平面三角形
(4)Na+
(5)3H2O2+K2Cr2O7+4H2SO4=Cr2(SO4)3+3O2↑+7H2O+K2SO4
【解析】M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素.M基态原子L层中p轨道电子数是s电子数的2倍,核外电子排布式为1s22s22p4 , 故M为O元素;由原子序数可知R、X、Y均处于第三周期,R是同周期元素中最活泼的金属元素,则R为Na;X和M形成的一种化合物是引起酸雨的主要大气污染物,则X为S元素,可知Y为Cl;Z的基态原子4s和3d轨道半充满,外围电子排布式为3d54s1 , 处于VIB族,故Z为Cr.
(1)R为Na,基态原子的电子排布式是1s22s22p63s1 , 同周期自左而右电负性增大,故Cl元素电负性大于S的,所以答案是:1s22s22p63s1;Cl;(2)H2O分子能形成氢键,使水的沸点升高,而H2S不能形成氢键,故硫化氢的沸点低于水的,所以答案是:H2O分子能形成氢键,而H2S不能形成氢键;
(3)X与M形成的SO3分子中S原子孤电子对数= ![]() =0,价层电子对数为3+0=3,故其空间构型为平面三角形,所以答案是:平面三角形;(4)M和R所形成的一种离子化合物为Na2O,晶胞中黑色球数目为8,白色球数目为8×
=0,价层电子对数为3+0=3,故其空间构型为平面三角形,所以答案是:平面三角形;(4)M和R所形成的一种离子化合物为Na2O,晶胞中黑色球数目为8,白色球数目为8×![]() +6×
+6×![]() =4,黑色球与白色球数目之比为2:1,故图中黑球代表的离子是Na+ , 所以答案是:Na+;
=4,黑色球与白色球数目之比为2:1,故图中黑球代表的离子是Na+ , 所以答案是:Na+;
(5)Z的最高价含氧酸的钾盐(橙色)为K2Cr2O7 , 与氧元素的氢化物发生氧化还原反应,该氢化物为H2O2 , 在稀硫酸中,Cr元素被还原为+3价,H2O2被氧化生成氧气,反应方程式为:3H2O2+K2Cr2O7+4H2SO4=Cr2(SO4)3+3O2↑+7H2O+K2SO4 ,
所以答案是:3H2O2+K2Cr2O7+4H2SO4=Cr2(SO4)3+3O2↑+7H2O+K2SO4 .


科目:高中化学 来源: 题型:
【题目】下列与实验相关的叙述正确的是( )
A.稀释浓硫酸时,应将蒸馏水沿烧杯内壁缓慢地注入浓硫酸中并不断搅拌
B.配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出
C.配制1molL﹣1 300mL NaCl溶液可以选择一个50mL的容量瓶和一个250mL的容量瓶
D.可以用如图装置进行氯气的尾气处理 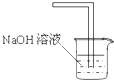
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 1mol H2SO4的质量为98gmol-1 B. SO3的摩尔质量为80gmol-1
C. 1molO就是1mol 氧气 D. SO2 的摩尔质量与其相对分子质量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用 X 射线对 BaSO4 穿透能力较差的特性,医学上在进行消化系统的 X 射线透视时,常用 BaSO4 作内服造影剂,这种检查手段称为钡餐透视.
(1)医学上进行钡餐透视时为什么不用 BaCO3?(用离子方程式表示)________________________________
(2)某课外活动小组为了探究 BaSO4 的溶解度,分别将足量 BaSO4 放入a.5mL 水 ;b.40mL 0.2molL-1Ba(OH)2 溶 液 c.20mL 0.5molL-1Na2SO4 溶 液 d.40mL 0.1molL-1H2SO4溶液中,溶解至饱和。
①以上各溶液中,Ba2+的浓度由大到小的顺序为_______________________________
A.b>a>c>d B.b>a>d>c C.a>d>c>b D.a>b>d>c
②已知 25℃时,Kap=1.1×10-10,上述条件下,溶液 b 中的 SO42-浓度为_________________molL-1,溶解 c中 Ba2+的浓度为_________________molL-1
③某同学取同体积的溶液 b 和溶液 d④直接混合,则混合液的 pH 为_________________(设混合溶液的体积为混合前两溶液的体积之和)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)0.4mol氨气和0.2mol硫化氢的质量之比为 , 所含分子数之比为 .
(2)现有NH3、H2S、HCl三种气体,它们分别都含有1mol氢原子,则三种气体的物质的量之比为 .
(3)以下物质:①碳酸钾 ②空气 ③二氧化碳 ④铜 ⑤食盐 ⑥氢氧化钠 ⑦硫酸铜溶液 ⑧酒精 ⑨蔗糖(C12H22O11).其中属于电解质的是(填序号).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:

(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应是______________。在X极附近观察到的现象是______________________________。
②Y电极上的电极反应式是______________。检验该电极反应产物的方法是______________。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是___________________,电极反应式是______________。
②Y电极的材料是___________________,电极反应式是______________。
(说明:杂质发生的电极反应不必写出)
③假若电路中有0.04摩尔电子通过时,阴极增重________克。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于取代反应的是( )
A.H2C=CH2+HCl→H3C﹣CH2Cl
B.2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
C.2C6H6+15O2 ![]() 12CO2+6H2O
12CO2+6H2O
D.CH3CH3+Cl2→CH3CH2Cl+HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯和溴的取代反应的实验装置如图所示,其中A为具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑. 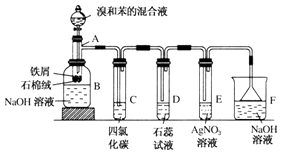
(1)填写下列空白: ①试管A中的反应方程式为
②试管C中四氯化碳的作用是: . 反应开始后,观察D和E两试管,看到的现象分别为:D管 , E管 . 写出E中反应的离子方程式
③反应2~3min后,在B中的NaOH溶液里可观察到的现象是 . 原因
(2)实验室制备硝基苯的主要步骤如下: a.配制一定比例的浓H2SO4与浓HNO3的混合酸,加入反应器中;
b.向室温下的混合酸中逐滴加入一定量的苯,充分振荡,混合均匀;
c.在55~60℃下发生反应,直至反应结束;
d.除去混合酸后,粗产品依次用蒸馏水和5%NaOH溶液洗涤,最后再用蒸馏水洗涤;
e.将用无水CaCl2干燥后的粗硝基苯进行蒸馏,得到纯净硝基苯.请填写下列空白:
①制备硝基苯的反应类型是
②配制一定比例的浓H2SO4和浓HNO3的混合酸时,操作的注意事项是: .
③步骤d中洗涤、分离粗硝基苯应使用的仪器是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com