
【题目】电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:

(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应是______________。在X极附近观察到的现象是______________________________。
②Y电极上的电极反应式是______________。检验该电极反应产物的方法是______________。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是___________________,电极反应式是______________。
②Y电极的材料是___________________,电极反应式是______________。
(说明:杂质发生的电极反应不必写出)
③假若电路中有0.04摩尔电子通过时,阴极增重________克。
【答案】 2H+ + 2e - = H2↑ 放出气体,溶液变红 2Cl - - 2e - = Cl2 ↑ 把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色 纯铜 Cu2+ + 2e - = Cu 粗铜 Cu - 2e - = Cu2+ 1.28
【解析】(1)①用惰性电极电解饱和NaCl溶液,X是电解的阴极,反应是2H+ + 2e - = H2↑,水电离的氢离子被反应,剩余氢氧根离子,所以显碱性,溶液变红。
②Y电极是电解的阳极,反应是2Cl - - 2e - = Cl2 ↑,检验氯气的常用试剂是湿润的淀粉碘化钾试纸,观察的现象是试纸会变蓝。
(2)电解精炼时,应该将纯度低的金属为阳极,纯度高的金属为阴极,含有该金属阳离子的溶液为电解液。所以X电极的材料是纯铜,电极反应式是Cu2+ + 2e - = Cu。Y电极的材料是粗铜,电极反应式是Cu - 2e - = Cu2+。若电路中有0.04mol电子通过,应生成0.02molCu,质量为1.28g。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】稀土元素号称“工业维生素”,科学家把稀土元素镧对作物的作用赋予“超级钙”的美称.已知镧(La)是一种活动性比锌更强的元素,它的氧化物的化学式为La2O3 , La(OH)3是不溶于水的弱碱,而LaCl3、La(NO3)3都可溶于水,下列说法中正确的是( )
A.La(NO3)3水溶液显酸性
B.LaCl3的水溶液加热蒸发灼烧,最终得到无水LaCl3
C.La和盐酸反应的离子方程式为:La+2H+=La3++H2↑
D.镧有两种核素: ![]() 和放射性
和放射性 ![]() ,由此可知镧元素的相对原子质量为138.5
,由此可知镧元素的相对原子质量为138.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列几种均属烃的含氧衍生物,请按要求作答:
(1)﹣定条件下①可转化为④,下列试剂中能实现该转化的是(填字母).
A.高锰酸钾溶液
B.H2
C.银氨溶液/H+
D.氢氧化钠溶液
(2)请写出满足下列条件的①的同分异构体 .
A.分子中除苯环外不含其它环状结构
B.苯环上一氯代物有三种
C.能与溴水中的Br2按1:4进行反应
(3)官能团是决定化合物特殊性质的原子或原子团,而有机物分子中基团间的相互影响也会导致物质性质的变化,依据此种观点回答以下问题:
①②③三种有机物溶解性由大到小的顺序(填字母),它们互为;
丙三醇、丙烷、乙二醇的沸点由高到低的顺序 .
醋酸、苯酚、苯甲酸的酸性由强到弱的顺序 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素.M基态原子L层中p轨道电子数是s电子数的2倍,R是同周期元素中最活泼的金属元素,X和M形成的一种化合物是引起酸雨的主要大气污染物,Z的基态原子4s和3d轨道半充满.请回答下列问题:
(1)R基态原子的电子排布式是 , X和Y中电负性较大的是(填元素符号).
(2)X的氢化物的沸点低于与其组成相似的M的氢化物,其原因是 .
(3)X与M形成的XM3分子的空间构型是 .
(4)M和R所形成的一种离子化合物R2M晶体的晶胞如图所示,则图中黑球代表的离子是(填离子符号).
(5)在稀硫酸中,Z的最高价含氧酸的钾盐(橙色)氧化M的一种氢化物,Z被还原为+3价,该反应的化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿色化学是“预防污染”的根本手段,它的目标是研究和寻找能充分利用的无毒害原材料,最大限度地节约能源,在化工生产各个环节中都实现净化和无污染.
(1)下列各项符合“绿色化学”要求的是 .
A.处理废弃物
B.治理污染点
C.减少有毒物
D.杜绝污染源
(2)在我国西部大开发中,某地为筹建一大型化工基地,征集到下列方案,其中你认为可行的是 .
A.建在西部干旱区可以脱贫致富
B.应建在水资源丰富和交通方便且远离城市的郊区
C.企业有权自主选择厂址
D.不宜建在人口稠密的居民区
(3)某化工厂排放的污水中含有Mg2+、Fe3+、Cu2+、Hg2+四种离子.某同学设计了从该污水中回收纯净的金属铜的方案.
在能制得纯铜的方案中,哪一步操作会导致环境污染? . 应增加哪些措施防止污染 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuCl广泛应用于化工和印染等行业.某研究性学习小组拟热分解CuCl22H2O制备CuCl,并进行相关探究.
【资料查阅】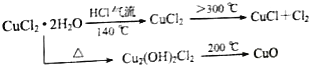
【实验探究】
该小组用如图所示装置进行实验(夹持仪器略).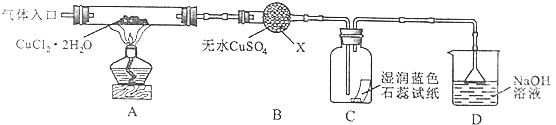
请回答下列问题:
(1)仪器X的名称是 .
(2)实验操作的先后顺序是a→→e(填操作的编号)
a.检查装置的气密性后加入药品
b.熄灭酒精灯,冷却
c.在“气体入口”处通入干燥HCl
d.点燃酒精灯,加热
e.停止通入HCl,然后通入N2
(3)在实验过程中,观察到B中物质由白色变为蓝色,C中试纸的颜色变化是 .
(4)装置D中发生的氧化还原反应的离子方程式是 .
(5)【探究反思】反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl2或CuO杂质,根据资料信息分析:
①若杂质是CuCl2 , 则产生的原因是 .
②若杂质是CuO,则产生的原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关少量食用油在低温下出现冻结现象后能否食用及解释合理的是
A. 不能,因为已经变质
B. 不能,因为含有杂质
C. 不能,因为含有水份
D. 能,因为那只是油脂主要成份在低温下结晶析出,是正常物理形态变化,并未变质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,有浓度均为1 mol·L-1的下列4种溶液:
①H2SO4溶液②NaHCO3溶液③NH4Cl溶液④NaOH溶液
(1)这4种溶液pH由大到小的顺序是 ,其中由水电离的H+浓度最小的是 。(均填序号)
(2)②中各离子浓度由大到小的顺序是 ,NaHCO3的水解平衡常数Kh= mol·L-1。(已知碳酸的电离常数K1=4×10-7,K2=5.6×10-11)
(3)向③中通入少量氨气,此时![]() 的值 (填“增大”、“减小”或“不变”)。
的值 (填“增大”、“减小”或“不变”)。
(4)若将③和④混合后溶液恰好呈中性,则混合前③的体积 ④的体积(填“大于”、“小于”或“等于”之一)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com