
【题目】写出下列反应的化学反应方程式:
(1)实验室制取乙炔_______________________;
(2)由甲苯制备TNT_______________________;
(3)实验室使用溴检验苯酚_________________;
(4)甲醛与银氨溶液的反应_________________。
【答案】 CaC2+2H2O![]() CH≡CH+Ca(OH)2
CH≡CH+Ca(OH)2 ![]() +3HO-NO2
+3HO-NO2 ![]()
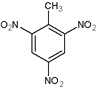 +3H2O
+3H2O ![]() +3Br2
+3Br2![]()
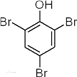 ↓ +3HBr HCHO + 4Ag(NH3)2OH
↓ +3HBr HCHO + 4Ag(NH3)2OH![]() 4Ag↓+ 6NH3↑+ (NH4)2CO3 + 2H2O
4Ag↓+ 6NH3↑+ (NH4)2CO3 + 2H2O
【解析】(1)实验室用碳化钙与水反应制取乙炔,反应的化学方程式为CaC2+2H2O→CH≡CH+Ca(OH)2,故答案为:CaC2+2H2O→CH≡CH+Ca(OH)2;
(2)由甲苯发生硝化反应制备TNT的化学方程式为![]() +3HO-NO2
+3HO-NO2 ![]()
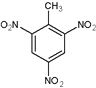 +3H2O,故答案为:
+3H2O,故答案为:![]() +3HO-NO2
+3HO-NO2 ![]()
 +3H2O;
+3H2O;
(3)实验室使用溴检验苯酚的化学方程式为![]() +3Br2→
+3Br2→ 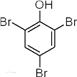 ↓ +3HBr,故答案为:
↓ +3HBr,故答案为:![]() +3Br2→
+3Br2→  ↓ +3HBr;
↓ +3HBr;
(4)甲醛与银氨溶液的反应的化学方程式为HCHO + 4Ag(NH3)2OH→ 4Ag↓+ 6NH3↑+ (NH4)2CO3 + 2H2O,故答案为:HCHO + 4Ag(NH3)2OH→ 4Ag↓+ 6NH3↑+ (NH4)2CO3 + 2H2O。


科目:高中化学 来源: 题型:
【题目】化合物A经李比希法和质谱法分析得知其相对分子质量为 136,分子式C8H8O2,A的核磁共振氢谱有4个峰且面积之比为1:2:2:3,A分子中只含一个苯环,且苯环上只有一个取代基,其红外光谱与核磁共振氢谱如图。关于A的下列说法中不正确的是

A. A分子属于酯类化合物,在一定条件下能发生水解反应
B. A在一定条件下可与3 mol H2发生加成反应
C. 符合题中A分子结构特征的有机物只有一种
D. 与A属于同类化合物的同分异构体只有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的( )
A. 酸性氧化物和碱性氧化物都是电解质
B. 将NaOH溶液,逐滴加入FeCl3溶液,可制备氢氧化铁胶体
C. 硫酸、氢氧化钠、氯化钠均为强电解质,都属于离子化合物
D. 离子键一定只存在于离子化合物中,共价键不一定只存在于共价化合物中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在乙烯分子中有5个σ键、一个π键,它们分别是( )
A.sp2杂化轨道形成σ键、未杂化的2p轨道形成π键
B.sp2杂化轨道形成π键、未杂化的2p轨道形成σ键
C.C—H之间是sp2形成的σ键,C—C之间未参加杂化的2p轨道形成的是π键
D.C—C之间是sp2形成的σ键,C—H之间是未参加杂化的2p轨道形成的π键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【华南师大附中2017届三模】CO2和甲烷催化合成CO和H2是CO2资源化利用的有效途径。主要反应为
Ⅰ:CH4(g)+CO2(g) ![]() 2CO(g)+2H2(g) △H=+247kJ/mol
2CO(g)+2H2(g) △H=+247kJ/mol
(1)已知CH4(g)+H2O(g) ![]() CO(g)+H2(g) △H=+206kJ/mol
CO(g)+H2(g) △H=+206kJ/mol
写出CH4和水蒸气反应生成CO2的热化学方程式_________。
(2)在恒温、恒容的密闭容器中发生反应I,下列选项能够说明反应I达到平衡状态的是______。
A.混合气体的密度不变
B.混合气体的总压强不变
C.CH4、CO2、CO、H2的物质的量之比为1:1:2:2
D.3V正(H2)=V逆(CH4)
E.混合气体的平均相对分子质量不变
(3)催化合成的温度通常维持在550-750℃之间,从反应速率角度分析其主要原因可能是_________。
(4)将CH4与CO2各1mol充入某密闭容器中,发生反应I。100Kpa时,反应I到达平衡时CO2的体积分数与温度的关系曲线如图所示。

①图中A、B、C三点表示不同温度、压强下达到平衡时CO2的体积分数,则______点对应的平衡常数最小,判断依据是________;__________点对应的压强最大。
②300℃,100Kpa下,该容器中反应I经过40min达到平衡,计算反应在0-40min内的平均反应速率为v(CO2)=_________mol/min(结果保留两位有效数字),该温度下的压强平衡常数Kp=________。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是( )
A. 铁与稀硫酸:2Fe +6H+=2Fe3++3H2↑
B. 石灰乳与Na2CO3溶液混合:Ca(OH)2 +CO32-= CaCO3↓+2OH-
C. 大理石溶于醋酸溶液的反应:CaCO3+ 2H+=Ca2++CO2↑+H2O
D. 向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O![]() Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学兴趣小组设计以下实验方案,测定小苏打样品(含有NaHCO3和Na2CO3)中Na2CO3的质量分数。(已知2NaHCO3![]() Na2CO3 + CO2 ↑+ H2O)
Na2CO3 + CO2 ↑+ H2O)
【方案一】称取一定质量的固体样品,加热至恒重后冷却,称量剩余固体质量,计算。
(1)下列仪器中,在灼烧固体样品时用到的是____(填序号)。

A B C D
(2)若加热过程中有晶体迸溅出来,则测得的结果____(填“偏大”、“偏小”或“不变”)。
(3)实验中需加热至恒重的目的是:______________________________________________。
【方案二】称取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量Ba(OH)2溶液,过滤,洗涤,干燥沉淀,称量固体质量,计算。
(1)请写出足量Ba(OH)2溶液和NaHCO3发生反应的离子方程式:_____________________。
(2)实验中判断沉淀是否完全的方法是____________________________________。
(3)实验中判断沉淀是否洗涤干净的方法是___________________________________。
【方案三】按如图所示装置进行实验:

(1)B装置内所盛试剂是____;D装置的作用是_____________。
(2)检查整套实验装置气密性方法是______________________________________。
(3)经检查装置气密性良好,但根据此实验测得的数据,测定结果有误差,因为该实验装置还存在一个明显缺陷是________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用控制n(H2S):n(FeCl3)=1:2反应得到的产物再用电解法制氢,其工作原理如图所示。下列有关的说法错误的是( )
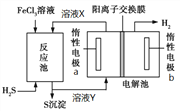
A. 惰性电极a为发生氧化反应
B. Fe(OH)3胶体中滴加溶液X,先有沉淀后沉淀溶解
C. 溶液Y加热蒸发灼烧最终得到Fe2O3
D. 电解池总反应的离子方程式为2Fe2++2H+![]() 2Fe3++H2↑
2Fe3++H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com