
【题目】写出以下反应的化学方程式:
(1)Na2O2与CO2反应:_______________
(2)加热使NaHCO3分解:____________
(3)Al与NaOH溶液反应:______________
(4)Fe(OH)2长时间露置于空气中:_____________
【答案】 2Na2O2 + 2CO2![]() 2Na2CO3 + O2 2NaHCO3
2Na2CO3 + O2 2NaHCO3 ![]() Na2CO3 + CO2↑ + H2O 2Al + 2NaOH + 2H2O
Na2CO3 + CO2↑ + H2O 2Al + 2NaOH + 2H2O![]() 2NaAlO2 + 3H2↑ 4Fe(OH)2 + O2 + 2H2O
2NaAlO2 + 3H2↑ 4Fe(OH)2 + O2 + 2H2O ![]() 4Fe(OH)3
4Fe(OH)3
【解析】(1)Na2O2与CO2反应生成碳酸钠和氧气,反应的化学方程式为:2Na2O2 + 2CO2![]() 2Na2CO3 + O2;(2)加热使NaHCO3分解生成碳酸钠、二氧化碳和水,反应的化学方程式为:2NaHCO3
2Na2CO3 + O2;(2)加热使NaHCO3分解生成碳酸钠、二氧化碳和水,反应的化学方程式为:2NaHCO3 ![]() Na2CO3 + CO2↑ + H2O;(3)Al与NaOH溶液反应生成偏铝酸钠和氢气,反应的化学方程式为:2Al + 2NaOH + 2H2O
Na2CO3 + CO2↑ + H2O;(3)Al与NaOH溶液反应生成偏铝酸钠和氢气,反应的化学方程式为:2Al + 2NaOH + 2H2O![]() 2NaAlO2 + 3H2↑;(4)Fe(OH)2长时间露置于空气中与氧气和水反应生成氢氧化铁,反应的化学方程式为:4Fe(OH)2 + O2 + 2H2O
2NaAlO2 + 3H2↑;(4)Fe(OH)2长时间露置于空气中与氧气和水反应生成氢氧化铁,反应的化学方程式为:4Fe(OH)2 + O2 + 2H2O ![]() 4Fe(OH)3。
4Fe(OH)3。


 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】将SO2分别通入下列4种溶液中,有关说法正确的是
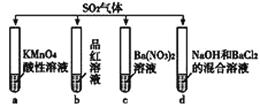
A. 试管a中实验可以证明SO2具有漂白性
B. 试管b中溶液褪色,说明SO2具有强氧化性
C. 试管c中能产生白色沉淀,该沉淀的成分为BaSO3
D. 试管d中能产生白色沉淀,该沉淀完全溶于稀盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(酸碱中和滴定是利用中和反应,用已知浓度的酸(或碱)来测定未知浓度的碱(或酸)的实验方法,其中溶液的pH变化是判断滴定终点的依据.
实验 | 消耗0.1000molL﹣1的 | 待测氢氧化钠 |
1 | 29.02 | 25.00 |
2 | 28.01 | 25.00 |
3 | 27.99 | 25.00 |
(1)如图所示A的pH范围使用的指示剂是;
(2)用0.1000molL﹣1的盐酸溶液滴定未知浓度的氢氧化钠溶液,重复三次的实验数据如表所示.则待测氢氧化钠的物质的量浓度是molL﹣1 . 在上述滴定过程中,若滴定前滴定管下端尖嘴中有气泡,滴定后气泡消失,则测定结果将(填“偏高”、“偏低”或“不影响”).
(3)下列关于上述中和滴定过程中的操作正确的是(填序号)
A.用碱式滴定管量取未知浓度的烧碱溶液
B.滴定管和锥形瓶都必须用待盛放液润洗
C.滴定中始终注视锥形瓶中溶液颜色变化
D.锥形瓶中的待测液可用量筒量取.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素.其中只有Z是金属,W的单质是黄色固体,X、Y、W在周期表中的相对位置关系如图.下列说法正确的是( ) 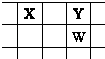
A.五种元素中,原子半径最大的是W
B.Y的简单阴离子比W的简单阴离子还原性强
C.Y与Z形成的化合物都可以和盐酸反应
D.Z与Q形成的化合物水溶液一定显酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用洁净的铂丝蘸取无色溶液,在无色灯焰上观察时看到黄色火焰,则下列有关叙述正确的是( )
A. 用铂丝做焰色反应实验,每次做完后都需要用硫酸洗涤
B. 该溶液一定含有Na+,也可能含有K+
C. 该溶液不含Na+,可能含K+
D. 该溶液可能含Na+或K+中的一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量是沟通宏观和微观的桥梁,请回答下列问题。
(1)同温同压下的两个相同容器中分别装有NO和NO2气体,则两瓶气体中,原子数之比是___,质量之比是___,密度之比是___分子数之比是___.
(2)下列所给出的几组物质中:含有分子数最少的是___;含有原子数最多的是___;标准状况下体积最小的是___.
①1gH2; ②2.408×1023个CH4; ③10.8gH2O; ④标准状况下6.72LCO2.
(3)设NA表示阿伏伽德罗常数,如果x g某气体含有的分子数是y,则z g该气体在标准状况下的体积是 _________________L(用含NA的式子表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向10 mL 0.40 mol·L-1 H2O2溶液中加入适量FeCl3溶液,不同时刻测得生成O2的体积(已折算为标准状况)如下表所示。( )
t / min | 0 | 2 | 4 | 6 |
V(O2) / mL | 0 | 9.9 | 17.2 | 22.4 |
资料显示,反应分两步进行:
①2Fe3++ H2O2 ![]() 2Fe2++O2↑+2H+
2Fe2++O2↑+2H+
② H2O2 + 2Fe2++2H+ ![]() 2H2O+2Fe3+
2H2O+2Fe3+
反应过程中能量变化如右图所示。下列说法不正确的是
A.0~6 min的平均反应速率:v(H2O2) = 3.33×10-2 mol·L-1·min-1
B.Fe3+的作用是加快过氧化氢的分解速率
C.反应①是吸热反应、反应②是放热反应
D.反应2H2O2(aq) ![]() 2H2O(l) + O2(g)的△H =E1-E2 < 0
2H2O(l) + O2(g)的△H =E1-E2 < 0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com