
 .
. .
. .
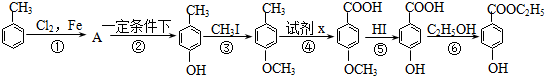
.分析 反应①是甲苯与Cl2在铁粉作催化剂的条件下发生苯环上的取代反应,从反应②的产物可知反应②是一个卤代烃的水解反应,可推出有机物A为 ,反应③是将酚羟基中氢被甲基取代,反应⑤是将甲氧基又变为酚羟基,比较
,反应③是将酚羟基中氢被甲基取代,反应⑤是将甲氧基又变为酚羟基,比较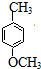 和
和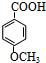 的结构可知,反应④是将甲基氧化成羧基的反应,所以试剂X为酸性高锰酸钾溶液,从④是氧化反应知,反应③和⑤的目的是保护酚羟基,防止被氧化,据此答题.
的结构可知,反应④是将甲基氧化成羧基的反应,所以试剂X为酸性高锰酸钾溶液,从④是氧化反应知,反应③和⑤的目的是保护酚羟基,防止被氧化,据此答题.
解答 解:反应①是甲苯与Cl2在铁粉作催化剂的条件下发生苯环上的取代反应,从反应②的产物可知反应②是一个卤代烃的水解反应,可推出有机物A为 ,反应③是将酚羟基中氢被甲基取代,反应⑤是将甲氧基又变为酚羟基,比较
,反应③是将酚羟基中氢被甲基取代,反应⑤是将甲氧基又变为酚羟基,比较 和
和 的结构可知,反应④是将甲基氧化成羧基的反应,所以试剂X为酸性高锰酸钾溶液,从④是氧化反应知,反应③和⑤的目的是保护酚羟基,防止被氧化,
的结构可知,反应④是将甲基氧化成羧基的反应,所以试剂X为酸性高锰酸钾溶液,从④是氧化反应知,反应③和⑤的目的是保护酚羟基,防止被氧化,
(1)根据上面的分析可知,A为 ,
,
故答案为: ;
;
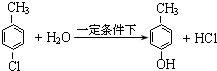
(2)反应②的化学方程式是: ,
,
故答案为: ;
;
(3)根据上面的分析可知,试剂x是酸性KMnO4溶液,反应⑥是羧基与乙醇反应生成酯基,所以其反应类型是酯化反应,
故答案为:酸性KMnO4溶液;酯化;
(4)反应⑤的化学方程式是 ,
,
故答案为: ;
;
(5)根据上面的分析可知,合成路线中设计③、⑤两步反应的目的是保护酚羟基,使之不被氧化,
故答案为:保护酚羟基,使之不被氧化.
点评 本题考查有机化学推断,难度注定要,题目中有一个隐含条件在推断过程中,即羟基与HI反应生成了甲氧基,此反应反过来也能发生,所以HI起到了能保护羟基的作用.在做此类题目的时候,注意发生反应的官能团以及官能团的位置.


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案科目:高中化学 来源: 题型:解答题
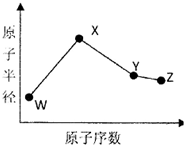 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为14,中子数为7;X的离子与NH4+具有相同的质子、电子数目:W与Y的氧化物均能导致酸雨的形成;Z的非会属性在同周期主族元素中最强.
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为14,中子数为7;X的离子与NH4+具有相同的质子、电子数目:W与Y的氧化物均能导致酸雨的形成;Z的非会属性在同周期主族元素中最强.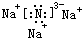 .
.| 时间 | 浓度(mo1/L) | ||
| c(W2) | c(B) | c(A) | |
| 第0min | 4.0 | 9.0 | 0 |
| 第10min | 3.8 | 8.4 | 0.4 |
| 第20min | 3.4 | 7.2 | 1.2 |
| 第30min | 3.4 | 7.2 | 1.2 |
| 第40min | 3.6 | 7.8 | 0.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④⑤⑦ | B. | 全部 | C. | ①③④⑤⑥ | D. | ①④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4能使酸性KMnO4溶液褪色 | |
| B. | 金属Na能与C2H5OH中的甲基反应生成H2 | |
| C. | 乙酸有强烈的刺激性气味,其水溶液称为冰醋酸 | |
| D. | CH3CH2CH2CH3与CH3CH(CH3)2互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
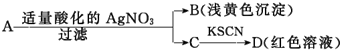
| A. | A一定是FeBr3 | B. | B为AgBr | ||
| C. | 滤液C中有Fe3+ | D. | D溶液中存在Fe(SCN)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | B | C | |
| D |
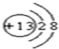
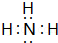 ,Y的结构式为
,Y的结构式为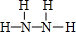 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaClO溶液的漂白原理与SO2相同 | |
| B. | 1 mol Cl2与足量NaOH溶液反应转移2 mol电子 | |
| C. | NaClO溶液的消毒原理是其强氧化性使蛋白质变性 | |
| D. | “84”消毒液与“洁厕灵”(盐酸)共同使用可达到既清洁又消毒的双重效果 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
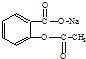 转变为
转变为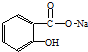 的方法正确的是( )
的方法正确的是( )| A. | 与足量的NaOH溶液共热后,再通入足量的CO2 | |
| B. | 与稀H2SO4共热后,加入足量的Na2CO3 | |
| C. | 与足量的NaOH溶液共热后,加入足量的稀H2SO4 | |
| D. | 与稀H2SO4共热后,加入足量的NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com