
将晶体X加热分解,可得A、B、D、E、F和水六种产物,其中A、B、D都是中学化学中常见的氧化物,气体E是单质F所含元素的氢化物。
(1)A能溶于强酸、强碱,写出A与强碱溶液反应的离子方程式_______________。
(2)B、D都是酸性氧化物且组成元素相同,D溶于水得强酸,则B、D分子中除氧元素外所含另一种元素在周期表中的位置是_______________。
(3)E能使湿润的红色石蕊试纸变蓝,实验室制取E气体的化学方程式为________________,制得的气体可用如图所示装置收集,则气体应从_______(填“A”或“B”)通入。
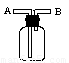
(4)由各分解产物的物质的量之比推测X的组成类似于明矾,则其化学式为___________,若向X的浓溶液中滴加浓NaOH溶液至过量,现象依次为_______________ 、___________ _、
_____________ 。
(5)取一定量的X晶体分解,若生成F 1 mol,则必同时生成_______ 物质_____ mol。
(1)Al2O3+2OH-=2AlO2-+H2O (2)第三周期,ⅥA族
(3)Ca(OH)2+2NH4Cl CaCl2+2NH3↑+2H2O; B
CaCl2+2NH3↑+2H2O; B
(4)NH4Al(SO4)2·12H2O;生成白色沉淀;生成刺激性气味的气体;白色沉淀又逐渐溶解
(5)SO2;3
【解析】
试题分析:(1)A能溶于强酸、强碱,且A是氧化物,所以A是氧化铝,氧化铝与强碱溶液反应的离子方程式为Al2O3+2OH-=2AlO2-+H2O。
(2)B、D都是酸性氧化物且组成元素相同,D溶于水得强酸,所以B是SO2,D是三氧化硫,因此则B、D分子中除氧元素外所含另一种元素是硫,硫元素在周期表中的位置是第三周期第ⅥA族。
(3)E能使湿润的红色石蕊试纸变蓝,则E是氨气,实验室制取E气体的化学方程式为Ca(OH)2+2NH4Cl CaCl2+2NH3↑+2H2O。氨气密度小于空气的,所以用如图所示装置收集氨气时应该从B口通入。
CaCl2+2NH3↑+2H2O。氨气密度小于空气的,所以用如图所示装置收集氨气时应该从B口通入。
(4)气体E是单质F所含元素的氢化物,所以F是氮气。即X分解产物是氧化铝、SO2、三氧化硫、氨气、氮气和水。又因为X的结构类似于明矾,所以根据明矾的化学式KAl(SO4)2·12H2O可知X的化学式为NH4Al(SO4)2·12H2O;向X的溶液中滴加浓氢氧化钠溶液,OH-首先结合Al3+生成白色沉淀氢氧化铝,然后与NH4+结合放出刺激性气味的气体氨气,最好再溶解氢氧化铝,白色沉淀消失,因此实验现象依次为生成白色沉淀;生成刺激性气味的气体;白色沉淀又逐渐溶解。
(5)X如果分解生成1mol氮气,则氮元素的化合价从-3价升高到0价,失去3个电子,即生成1mol氮气失去6mol电子。S元素的化合价从+6降低到+4价,得到2个电子,所以根据电子得失守恒可知生成SO2的物质的量是6mol÷2=3mol。
考点:考查氧化铝、SO2、三氧化硫性质;氨气制备;晶体化学式的确定以及氧化还原反应的计算等


 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案科目:高中化学 来源: 题型:
 化学选做题----物质结构
化学选做题----物质结构查看答案和解析>>
科目:高中化学 来源: 题型:
| 加热前质量 | 加热前质量 | 加热后质量 |
| W1(容器) | W2(容器+晶体) | W3(容器+无水硫酸铜) |
| 160(W2-W3) |
| 18(W3-W1) |
| 160(W2-W3) |
| 18(W3-W1) |
| 0.418×2.35 |
| 0.025 |
| 0.418×2.35 |
| 0.025 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组对氨气的制法进行了如下设计:
(1)下面是该小组同学提出的实验室制备氨气的几种方案:
A.硝酸铵固体与氢氧化钠固体共热
B.加热分解NH4Cl晶体
C.将浓氨水逐滴加到新制的生石灰中
你认为其中较为简便易行的方案有_______________(填写字母);其反应的化学方程式为__________________________________。

请从上图的仪器中选择制取氨气的发生装置(要求仪器少、合理)__________(写编号)。
(2)该小组需收集干燥后的氨气:
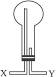
①如选用如右图所示的装置,则气体应由导管口_______(填“X”或“Y”)导入(集气瓶不能颠倒)。
②若用排液集气法收集氨气,可选用的试剂是_______(填字母)
A.H2O B.浓H2SO4 C.CCl4 D.NaCl饱和溶液
(3)用图示装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷的操作是___________
________________________。
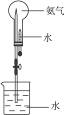
(4)若原烧瓶中氨气是充满的,进行喷泉实验后,烧瓶内溶液中溶质的物质的量浓度为_________(假定在标准状况下)。
查看答案和解析>>
科目:高中化学 来源: 题型:
将晶体X加热分解,可得A、B、D、E、F和水六种产物,其中A、B、D是中学化学常见的氧化物,气体E是单质F所含元素的氢化物。
(1)A能溶于强酸、强碱。写出A与强碱溶液反应的离子方程式: 。
(2)B、D都是酸性氧化物,且组成元素相同。B、D分子中除氧外所含另一种元素在两种化合物中的质量分数分别为50%和40%,则B、D分子中除氧外所含另一种元素在周期表中的位置为 。
 (3)E能使湿润的红色石蕊试纸变蓝,实验室制取E气体的化学方程式是
(3)E能使湿润的红色石蕊试纸变蓝,实验室制取E气体的化学方程式是
。制得的气体可用如图所示装置收集,则
气体应从 (填“A”或“B”)通入。E中所含化学键类型为
。(填“极性键”或“非极性键”)
(4)单质F的电子式为 。由各分解产物的物质的量之比推测X的组成类似于明矾,则X化学式为 。
(5)取一定量的X晶体分解,若生成F 1mol,则必同时生成 物质 mol.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com