
【题目】用托盘天平称取 10.1g NaOH 试样,下列操作中,正确的是
A. 将 NaOH 放在天平左边托盘中的纸片上
B. 将 NaOH 放入烧杯中(烧杯事先已称重),并放在天平右边托盘上
C. 用镊子取出标定为 10.1g 的砝码放在天平右边的托盘上
D. 用镊子取出标定为10g的砝码放在天平右边的托盘上,并将游码向右移到 0.1g位置上
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
【题目】将一小块钠投入到CuSO4溶液中,一定观察不到的现象是( )
A. 钠浮在溶液表面
B. 发出“嘶嘶”的响声,钠块四处游动,逐渐变小直至消失
C. 有蓝色沉淀生成
D. 有红色粉末生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在甲、乙、丙、丁四个烧杯里分别放入0.1mol的钠,氧化钠,过氧化钠和氢氧化钠,然后各加入100mL水,使固体完全溶解,则甲、乙、丙、丁的溶液中溶质的质量分数大小的顺序为
A.甲>乙>丙>丁 B.丁<甲<乙=丙
C.甲=丁<乙=丙 D.丁<甲<乙<丙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】淀粉通过下列转化可以得到C(以下反应部分条件略去): 淀粉 ![]() M
M ![]() N→A
N→A ![]() D
D ![]() C
C
A~F六种物质可以发生如图转化:
注:[O]表示足最常用氧化剂;C 常用于汽车的防冻液.
(1)A的官能团的结构简式为 , 其产量可以用来衡量一个国家石油化工的发展水平.N 生成A的反应条件为 , B的一种同分异构体的名称为 .
(2)①写出E生成F的离子方程式 . ②写出C2H2O2生成E的化学方程式([O]为含铜物质) .
(3)C与E一定条件下反应的生成物中相对分子质量最小的物质的摩尔质量为 .
(4)H分子含有4个碳,且为C2H2O2的同系物,H的同分异构体中含有 ![]() ,且无环状结构的同分异构体有种.(不考虑立体异构)
,且无环状结构的同分异构体有种.(不考虑立体异构)
(5)芳香化合物G仅含碳、氢、氧三种元素,相对分子质量为110.G能与碳酸钠反应,不能与碳酸氢钠反应,且G分子中烃基上的一氯取代物只有一种.则G的结构简式为 .
(6)已知: ![]() . 以乙烯为起始原料,选用必要的无机试剂合成正丁酸,写出合成路线(用结构简式表示有机物),用箭头表示转化关系,箭头上注明试剂和反应条件).
. 以乙烯为起始原料,选用必要的无机试剂合成正丁酸,写出合成路线(用结构简式表示有机物),用箭头表示转化关系,箭头上注明试剂和反应条件).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体X和气体Y 各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如下表,下列说法正确的是( )
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A.反应前2min的平均速率v(Z)=2.0×10﹣3 mol/(Lmin)
B.其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C.该温度下此反应的平衡常数K=1.44
D.其他条件不变,再充入0.2 mol Z,平衡时X的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据叙述,写出下列反应的热化学方程式.
(1)已知1mol Na的单质在足量O2中燃烧,恢复至室温,放出255.5kJ热量,写出该反应的热化学方程式:
(2)用NA表示阿伏伽德罗常数,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出650kJ的热量.其热化学方程式为 .
(3)已知拆开1mol H﹣H键、1mol N﹣H键、1mol N≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为 .
(4)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体.在25℃、101kPa下,已知该反应每消耗1mol CuCl(s),放热44.4kJ,该反应的热化学方程式是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na、Al、Fe、Cu是中学化学中重要的金属元素。它们的单质及其化合物之间有很多转化关系。下表所列物质不能按如图(“→”表示一步完成)关系相互转化的是( )
选项 | A | B | C | D |
|
a | Na | Al | Fe | Cu | |
b | NaOH | Al2O3 | FeCl3 | CuO | |
c | NaCl | Al(OH)3 | FeCl2 | CuSO4 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿矾是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
(1)在试管中加入少量绿矾样品,加水溶解,滴加少量稀硫酸将溶液酸化,滴加KSCN溶液,溶液颜色无明显变化。再向试管中通入空气,溶液逐渐变红。写出该过程的所有离子反应方程式:___________________________。
(2)为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1 g。将样品装入石英玻璃管中,再次将装置A称重,记为 m2 g。按下图连接好装置进行实验。
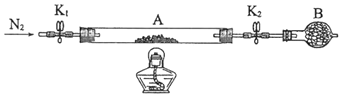
①仪器B的名称是______________。
②将下列实验操作步骤正确排序_______(填标号);重复上述操作步骤,直至A恒重,记为m3 g。
A.点燃酒精灯,加热
B.熄灭酒精灯
C.关闭K1和K2
D.打开K1和K2,缓缓通入N2
e.称量A
f.冷却至室温
③根据实验记录,计算绿矾化学式中结晶水数目x=_______________。(列式表示).若实验时按a、d次序操作,则使x__________(填“偏大”“偏小”或“无影响”)。
(3)测定硫酸亚铁的分解产物发现:一种产物为红棕色固体,另外两种产物为气体,反应产物中氧化产物与还原产物的物质的量相等,写出该过程的化学方程式:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等物质的量的Fe,Mg,Al分别与足量的物质的量浓度相同的盐酸完全反应,消耗盐酸的体积比为( )
A.2:3:1
B.2:2:3
C.3:2:1
D.1:3:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com